有关下列四个常用电化学装置的叙述中正确的是( )

A.图Ⅰ所示电池中,负极电极反应为Zn-2e- Zn2+ Zn2+ |
| B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 |
| D.图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中被还原为Ag |
下图中A、D均为碳棒,B为铝棒,C为铁棒,硫酸钠溶液在实验前采取了煮沸处理。B在实验时才插入溶液中。

(1)从装置的特点判断,甲、乙装置中_______是原电池,负极的电极反应式为_____________________。
(2)实验开始一段时间后乙池溶液中的现象是,_______________________,若用某电解质溶液代替硫酸钠溶液也能出现相同的现象,则此溶液可以是
A.NaOH溶液 B.AgNO3溶液
C.NaCl溶液 D.CuSO4溶液
(3)实验前煮沸硫酸钠溶液的目的是______________________________ 。
(4)在实验(2)的基础上,改变两电极的连接方式,A接D、B接C,此时D电极上的电极反应式为_________________。乙装置里除两电极有明显现象外,还可以看到的现象是________________________,产生该现象的化学方程式是_____________________________________。
下列四种装置中,溶液的体积均为250毫升,开始时电解质溶液的浓度均为0.10摩/升,工作一段时间后,测得导线上均通过0.02摩电子,若不考虑溶液体积的变化,则下列叙述正确的是
| A.工作一段时间后溶液的浓度①=②=③=④ |
| B.工作一段时间后溶液的pH:④>③>①>② |
| C.产生气体的总体积:④>③>①>② |
| D.电极上析出的固体的质量:①>②>③>④ |
在通风橱中进行下列实验:
| 步骤 |
 |
 |
|
| 现象 |
Fe表面产生大量无色气泡,液面上方变为红棕色 |
Fe表面产生少量红棕色气泡后,迅速停止 |
Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A.Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2==2NO2
B.进一步反应对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
C.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计如图装置:

(1)a和b用导线连接,Cu极为原电池_________极(填“正”或“负”),电极反应式为 Zn极发生_________(填“氧化”或“还原”)反应。溶液中H+移向____________(填“Cu”或“Zn”)极。
(2)无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻______g。
(3)有同学想把Ba(OH)2•8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行? (填“是”或“否”),理由是 。
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由强到弱的顺序是
| A.①③②④ | B.①③④② | C.③④②① | D.③①②④ |
纽扣式银锌电池的构造如图所示,电池的总反应为:Zn+Ag2O+H2O=Zn(OH)2+2Ag,下列说法不正确的是
| A.Zn作负极 |
| B.电子经外电路流向Ag2O极 |
| C.K+向Zn极移动 |
| D.正极反应:Ag2O+H2O+2e-=2Ag+2OH- |
已知反应Cu(s) + 2Ag+ (aq) = Cu2+(aq) + 2Ag (s)为一自发进行的氧化还原反应,将其设计成如图所示原电池。下列说法中正确的是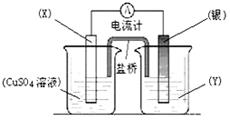
| A.银电极质量逐渐减小,Y溶液中c(Ag+)增大 |
| B.实验过程中取出盐桥,原电池仍继续工作 |
| C.电极X是正极,其电极反应为Cu-2e- = Cu2+ |
| D.当X电极质量减少0.64 g时,外电路中有0.02 mol电子转移 |
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是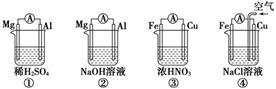
| A.①②中Mg作负极,③④中Fe作负极 |
| B.②中Mg作正极,电极反应式为:2H2O+2e-= 2OH-+H2↑ |
| C.③中Fe作负极,电极反应式为Fe-2e-= Fe2+ |
| D.④中Cu作正极,电极反应式为2H++2e-= H2↑ |
某原电池总反应的离子方程式为2Fe3++Fe=3Fe2+,能实现该反应的原电池是
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| B.正极为C,负极为Fe,电解质溶液为FeSO4溶液 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Cu,电解质溶液为CuSO4溶液 |
如图所示,电流表G发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液。则A、B、C为
A. A是Zn,B是Cu,C是稀H2SO4
B. A是Cu,B是Zn,C是稀H2SO4
C. A是Fe,B是Ag,C是稀AgNO3溶液
D. A是Ag,B是Fe,C 是稀 AgNO3溶液
下列化学反应在理论上可设计成原电池是
| A.2Al(s) + 2NaOH(aq) +2H2O(l) ="=" 2NaAlO2(aq) + 3H2(g) △H<0 |
| B.HNO3(aq) + KOH(aq) ="=" KNO3(aq) + H2O(l) △H<0 |
| C.Ba(OH)2·8H2O(s) + 2NH4Cl(s) ="=" BaCl2(aq)+ 2NH3·H2O(aq)+ 8H2O(l) △H﹥0 |
| D.Na2O(s)+ H2O(l) ="=" 2NaOH(aq) △H<0 |
试题篮
()