有关电化学知识的描述正确的是
| A.CaO+H2O===Ca(OH)2ΔH<0,故可把该反应设计成原电池 |
| B.某原电池反应为Cu+2AgNO3==Cu(NO3)2+2Ag,装置盐桥中为装有含琼胶的KCl饱和 溶液 |
| C.原电池的两极一定是由活动性不同的两种金属组成 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
将银棒和锌棒用导线连接插入AgNO3溶液中,当导线中有0.2 mol电子通过时,负极质量的变化是( )
| A.增加6.5 g | B.减少6.5 g | C.增加21.6g | D.减少21.6g |
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中正确的是 
| A.燃料电池工作时,正极反应为:O2+2H2O+4e一=40H— |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
将铁片和银片用导线连接置于同一稀盐酸中,经过一段时间后,下列叙述正确的是
| A.负极有Cl2逸出,正极有H2逸出 | B.负极附近Cl-的浓度逐渐减小 |
| C.正极附近Cl-的浓度逐渐增大 | D.溶液中Cl-的浓度基本不变 |
常用的钮扣式银锌电池,放电时的电极反应式分别为:
Zn极:Zn+2OH-+2e- = Zn(OH)2 Ag2O极:Ag2O+H2O+2e- =2Ag+2OH-则下列说法中不正确的是( )
| A.放电过程中[OH-]不变 | B.Zn为负极而Ag2O为正极 |
| C.电解质溶液呈碱性 | D.电子从Ag2O流出经用电器流入Zn极 |
右图为一原电池装置,其中X、Y为两电极。对此装置的下列说法中正确的是( )
| A.若两电极都是金属,则它们的活动性顺序为:X>Y |
| B.外电路的电流方向是:X→外电路→Y |
| C.若两电极分别为锌棒和石墨棒,则X为石墨 |
| D.Y极上发生的是氧化反应 |
下列说法正确的是
| A.强电解质一定易溶于水 |
| B.钢铁在海水中发生电化腐蚀时,铁是负极被氧化 |
| C.对可逆反应,升高温度一定存在v(正)>v(逆) |
| D.相同浓度时,强酸中水的电离程度比弱酸的水的电离程度小 |
将下表中各组的两电极用导线相连后放入盛有对应该组的溶液中,能产生电流的是
| 序号 |
电极1 |
电极2 |
溶液 |
| A |
Cu |
Cu |
稀H2SO4 |
| B |
Ag |
Zn |
稀H2SO4 |
| C |
Cu |
Cu |
酒精 |
| D |
C |
C |
ZnSO4溶液 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如右。该电池工作时,下列说法正确的是( )
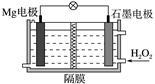
| A.Mg电极是该电池的正极 |
| B.H2O2在石墨电极上发生氧化反应 |
| C.石墨电极附近溶液的pH增大 |
| D.溶液中Cl-向正极移动 |
下图为水果电池的示意图,下列说法正确的是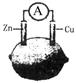
| A.锌片作负极,质量逐渐减少 | B.电子由铜片沿导线流向锌片 |
| C.铜电极逐渐溶解 | D.该装置能将电能转化为化学能 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙慢 |
试题篮
()