已知Fe(s)+H2SO4(aq)=FeSO4(aq)+H2(g) ΔH<0,则下列关于该反应的叙述不正确的是
| A.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| B.上述热化学方程式中的ΔH的值与反应物的用量有关 |
| C.该反应的化学能可以转化为电能 |
| D.此反应构成的原电池中,正极可以是碳棒、铜或锌 |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是
①每消耗1 mol CH4可以向外电路提供8 mole-
②负极上CH4失去电子,电极反应式为:CH4+10OH--8e-=CO+7H2O
③负极上是O2得电子,电极反应式为O2+2H2O+4e-=4OH-
④电池工作后,溶液的pH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应式为:Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
总反应式为Ag2O+Zn=ZnO+2Ag。根据上述反应式,判断下列叙述中正确的是
| A.在使用过程中,电池负极区溶液的pH增大 |
| B.在使用过程中,电子由Ag2O经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn极发生还原反应,Ag2O极发生氧化反应 |
下列各组的电极材料和电解液,不能组成原电池的是
| A.铜片、石墨棒,稀硫酸 | B.铜片、石墨棒,硝酸银溶液 |
| C.锌片、铜片,稀盐酸 | D.铜片、银片,FeCl3溶液 |
食品保鲜所用的“双吸剂”,是由还原铁粉、生石灰、碳酸钠、炭粉等按一定比例组成
的混合物,可吸收氧气和水。下列分析不正确的是
| A.“双吸剂”中的生石灰有吸水作用 |
| B.“双吸剂”吸收氧气时,发生了原电池反应 |
| C.吸收氧气的过程中,铁作原电池的负极 |
| D.炭粉上发生的反应为:O2 + 4e-+ 4H+====2H2O |
下列各变化中属于原电池反应的是
| A.在空气中金属铝表面迅速氧化形成保护层 |
| B.锌与稀硫酸反应时,加入少量NaHSO4固体时,可使反应速率加快 |
| C.红热的铁丝与冷水接触,表面形成蓝黑色保护层 |
| D.镀锌铁表面有划损时,仍然能阻止铁被氧化 |
下列关于反应4Li+2SOC12===4LiCl+S+SO2的叙述中,不正确的是
| A.SOCl2是氧化剂,Li是还原剂 |
| B.2 mol SOCl2参加反应,共转移4 mol电子 |
| C.将该反应设计成电池,SOCl2在正极发生反应 |
| D.若将该反应设计成电池,可用稀硫酸作电解质溶液 |
关于下列图示的说法中正确的是
| A.图①装置用于分离沸点相差较大的互溶液体混合物 |
| B.图②装置用于研究不同催化剂对反应速率的影响 |
| C.图③中电流计的指针不发生偏转 |
D.对反应: ;根据图④可以求出x=2 ;根据图④可以求出x=2 |
根据下列实验现象,所得结论错误的是

| 实验 |
实验现象 |
结论 |
| A |
Ⅰ烧杯中铁片表面有气泡,Ⅱ烧杯中铜片表面有气泡 |
活动性:Al>Fe>Cu |
| B |
试管中收集到无色气体 |
铜与浓硝酸反应产物是NO |
| C |
试管b比试管a中溶液的红色深 |
增大反应物浓度,平衡向正反应方向移动 |
| D |
长颈漏斗内液面高于烧瓶内液面,且保持不变 |
装置气密性良好 |
知反应:A(g)+B(g)=C(g)+D(g)的能量变化如图所示,下列说法正确的是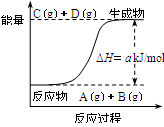
| A.若此反应过程中有电子转移,可设计成原电池 |
| B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应只有在加热条件下才能进行 |
某小组进行电化学研究,甲同学设计如下图的装置图,乙同学利用甲的装置和桌面其他的药品与材料,不能完成的实验是
| A.使甲同学的正极变为负极 | B.设计一个新的原电池 |
| C.在碳电极上镀锌 | D.使锌电极受到保护 |
【原创】某同学根据化学反应2Fe3++Fe 3Fe2+,设计原电池如下图,下列说法正确的是
3Fe2+,设计原电池如下图,下列说法正确的是
| A.Fe2+沿盐桥移向FeCl3溶液,FeCl2溶液浓度基本不变 |
| B.铁电极发生氧化反应,质量减少 |
| C.Fe3+在石墨电极上放电生成铁附着在石墨表面,使电极质量增加 |
| D.电池放电一段时间后,FeCl2溶液中增加的Fe2+的物质的量与FeCl3溶液中增加的Fe2+的物质的量相等 |
试题篮
()