航天飞机常用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4等可燃物质与O2一起构成的电池装置。它可直接将化学能转化为电能,甲烷电池以KOH溶液为电解质,其总反应的化学方程式为CH4+2O2+2OH-==CO32-+3H2O。
(1)负极上的电极反应为 。
(2)消耗16.8 L(标准状况下)O2时,有 mol 电子发生转移。
(3)开始放电时,正极附近溶液的氢氧根离子浓度 (填“增大”、“减小”或“不变”)。
某实验小组用以下几个实验装置探究电化学过程对金属与稀硫酸反应速率的影响, 烧杯中都盛有稀H2SO4。
试回答:
(1)B装置中Cu电极上的电极反应式为 ,D装置中Fe电极上的电极反应式为 ;
(2)D装置中的实验现象有 ,若用电流表测量反应时通过导线的电子流量为0. 2mol,则Fe电极的质量变化为 ;
(3)比较四个装置中Fe片被腐蚀的速率由快到慢的顺序是 (用A、B、C、D表示)。
设计出燃料电池使汽油氧化直接产生电流是本世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,回答如下问题:
(1)以丁烷(C4H10)为汽油代表,这个电池放电时发生的化学反应 ;
(2)这个电池负极发生的反应是:C4H10 + 13O2— + 26e-=4CO2+5H2O,正极发生的反应是: ;固体电解质里O2-的移动方向是: ;向外电路释放的电子的电极是: ;
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是: ;
(4)汽油燃料电池最大的障碍是氧化反应不完全产生 堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年,这正是新一代化学家的历史使命。
用导线将锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,此电池的负极是 ,正极的电极反应式是 ,负极的电极反应式是 ,总电极反应式是 。
(9分)将洁净的金属片Fe、Zn 、A、B 分别与Cu用导线连结浸在合适的电解质溶液里。实验并记录电压指针的移动方向和电压表的读数如表所示: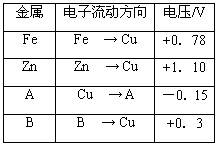
根据实验记录,完成以下填空:
(1)构成两电极的金属活动性相差越大,电压表的读数越 。(填“大”、“小”)。
(2)Zn、A、B三种金属活动性由强到弱的顺序是 。
(3)Cu与A组成的原电池, 为负极,
此电极反应式为 。
(4)A、B形成合金,露置在潮湿空气中, 先被腐蚀。
(5)铝热反应中的铝热剂的成分是
工业上常用的铝的冶炼的化学方程式为 。
氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电
极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定,请回答: 
(1) 氢氧燃料电池的能量转化形式主要是____ __,
(2) 在导线中电子流动方向为 ____ → __(用a、b表示)。
(3) 负极反应式为__________ ________。
(4) 电极表面镀铂粉的原因为_____ ____。
“阿波罗号飞船”所用的氢氧燃料电池的电极应为:负极:2H2+4OH--4e-=4H2O,则正极反应为 ;该电池工作时,通氢气的一极发生 反应(填氧化、还原),每转移4摩电子,电池内增加 摩水,负极附近溶液的PH值 ,(填升高、降低、不变),正极附近 [H+] (填升高、降低、不变)
原电池和电解池都能实现能量的置换。回答下列问题:
(1)可将化学能转化为电能是_________池;
(2)下列反应能设计成原电池的是:
① 2FeCl3+Fe=3FeCl2
② AlCl3+3NH3·H2O= Al(OH)3↓+3NH4Cl
③ NaOH+HC1=NaC1+H2O
(3)用FeCl3溶液腐蚀印刷电路铜板的离子方程式为: 。
(4)右图装置当闭合电键时,电表显示有电流通过。则Pt极的电极反应式: ; 当甲中产生0.1 mol气体时,乙中析出铜的质量应为________g。

下图A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。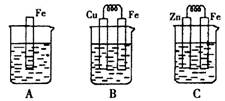
(1)A中反应的离子方程式是_______________________________________。
(2)B中Cu极的电极反应式是______________________________________。
(3)C中被腐蚀的金属是__________(填化学式),A、B、C中铁被腐蚀的速率,由快到慢的是顺序是_____________(用“>”表示)。
下列关于实验现象的描述,正确的是
① 由铜锌组成的原电池,电子是从锌经过导线流向铜
② 把铜片和锌片紧靠在一起浸入稀硫酸中,铜表面出现气泡
③ 把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
④ 把锌片放入盛盐酸的试管中,加入几滴氯化铜溶液,产生气泡的速率加快
为体现绿色世博、低碳世博、科技世博,上海世博会已经开始使用中国自己生产的燃料电池汽车,该车以氢气和空气中的氧气为燃料,KOH为电解质溶液,真正实现了“零排放”。该电池的负极反应式为 ,从能量角度分析氢气用作燃料电池与直接燃烧相比主要优点是 。
下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题: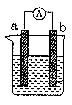
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,写出该原电池的总的离子反应反应方程式:
正极的电极反应式为:
当a极溶解的质量为5.4g时,有 mol电子通过导线
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,
该装置 (填“能”或“不能”)形成原电池,
若不能,请说明理由 (若能该空不作答),
若能,该原电池的正极为 ;该原电池总的化学反应方程式为:
(16分) 下图中甲、乙、丙的电极材料都是石墨和铁,其中丙是氯碱工业生产示意图。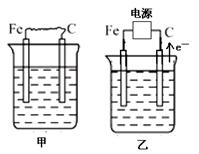

(1)若甲、乙两烧杯均盛放CuSO4溶液,
①甲中铁棒上的电极反应式为_______________________________________。
②乙装置工作一段时间后,向烧杯中加入适量的碱式碳酸铜【Cu2(OH)2CO3】,能使溶液恢复到起始状态,请写出这段时间内乙装置发生的所有反应的化学方程式
________________________________________________________________________。
(2)若甲、乙两烧杯均盛放饱和NaCl溶液,
①甲中石墨棒上的电极反应式为___________________。
②将湿润的淀粉碘化钾试纸放在乙烧杯______(填“Fe”或“C”)电极的上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应物Cl2和I2的物质的量之比为5∶1,且生成两种酸,则其对应的化学方程式为_________________________。
③假设产生的气体全部逸出溶液,当乙反应有0.01 mol电子转移后停止实验,此时烧杯中溶液的体积为100 mL,则溶液混合均匀后的pH = ____________。
④当乙中的反应用于工业生产时,为了阻止两极产物之间的反应,通常使用如丙图所示的装置,其中离子交换膜只允许Na+通过,Na+的移动方向如图中标注,则H2的出口是________(填代号)。
试题篮
()