如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42﹣═2PbSO4+2H2O.下列有关说法正确的是
| A.K与N相接时,能量由电能转化为化学能 |
| B.K与N相接时,Pb上发生反应为:Pb-2e- = Pb2+ |
| C.K与M连接时,所用电源的a极为负极 |
| D.K与M连接时,PbO2上发生反应为:PbO2+4e_+4H++SO42﹣═PbSO4+2H2O |
甲、乙、丙三个烧杯中分别装有稀硫酸、氯化铜溶液、饱和食盐水,把用导线连接的锌片和铜片插入甲,把分别与直流电源正、负极相连的C1、C2插入乙,把分别与直流电源正、负极相连的C3、铁片插入丙。则下列叙述正确的是( )
| A.甲、丙中是化学能转变为电能,乙中是电能转变为化学能 |
| B.C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 |
| C.C1和C3放出的气体相同,铜片和铁片放出的气体也相同 |
| D.甲、乙中溶液的pH逐渐升高,丙中溶液的pH逐渐减小 |
实验题
I.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有 ;
(2)实验室中现有Na2SO4、MgSO4、FeSO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是 ;
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 |
A |
B |
C |
D |
E |
F |
| 4mol/LH2SO4/mL |
30 |
V1 |
V2 |
V3 |
V4 |
V5 |
| 饱和CuSO4溶液/mL |
0 |
0.5 |
2.5 |
5 |
V6 |
20 |
| H2O/mL |
V7 |
V8 |
V9 |
V10 |
10 |
0 |
①完成此实验设计,其中:V1= ,V6= ,V9=
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
Ⅱ、某兴趣组进行下列实验测定某稀硫酸的质量分数,选用酚酞做指示剂。
操作①:取5.00 mL稀H2SO4溶液(密度为1.00 g/mL)置于锥形瓶中加水稀释;
操作②:用0.1000 mol/LKOH标准溶液滴定;
操作③:用同样方法滴定,4次消耗KOH溶液的体积分别为20.00 mL、19.98 mL、20.02 mL、20.40 mL。
请回答下列问题:
(4)如何判定滴定终点:______________________________________________。
(5)在上述实验中,下列操作会造成测定结果偏高的有________(填序号)。
A.锥形瓶用待测液润洗
B.量取稀H2SO4溶液的滴定管用蒸馏水洗净,未用稀H2SO4溶液润洗
C.滴定速度过快,又未摇匀,停止滴定后发现红色褪去
D.滴定前读数时平视,滴定终点读数时仰视
(6)分析数据,计算稀H2SO4溶液中溶质的质量分数为_________ (保留三位有效数字)。
工业上生产氯气,常用电解槽中电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分。下图(左图)为电解槽的示意图。
⑴这种阳离子交换膜,只允许溶液中的 通过。(填下列微粒的编号)
①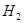 ②
②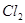 ③
③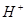 ④
④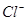 ⑤
⑤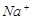 ⑥
⑥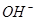
⑵写出在电解过程中阳极发生的电极方程式: 。
⑶已知某电解槽每小时加入10%的氢氧化钠溶液10kg,每小时能收集到标况下的氢气896L,而且两边的水不能自由流通。则理论上计算,电解后流出的氢氧化钠溶液的质量分数为 。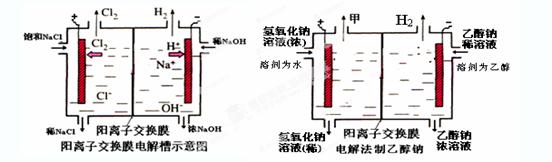
⑷某化学课外兴趣小组设计了用电解法制取乙醇钠的工业方法,所用的电解槽如上右图所示,设计要求:①所用的交换膜不能让分子自由通过;②电解过程中消耗的原料是氢氧化钠和乙醇。回答下列问题:
写出在电解过程中阳极发生的电极方程式 。
②最后从乙醇钠的乙醇溶液中分离得到纯净乙醇钠固体的方法是: 。
(5)如图所示的是一个燃料电池的示意图,当此燃料电池工作时,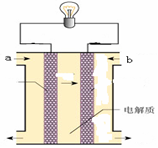
①如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则负极发生的电极方程式:
②如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则负极发生的电极方程式:
(共9分)如图所示,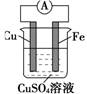
(1)该装置叫_____装置,可以将_____能转化为_____能。
(2)负极是 _______,电极反应为_______。
(3)正极是_______,电极反应为__ ,总反应为____。
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是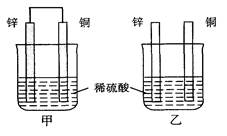
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均减小 |
| D.产生气泡的速度甲比乙快 |
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。回答下列问题: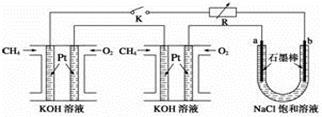
①甲烷燃料电池负极的电极反应为________________________。
②闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是____________(填化学式),电解氯化钠溶液的总反应方程式为_________________________;
③若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C · mol-1,列式计算),最多能产生的氯气体积为__________L(标准状况)。
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是
| 待测气体 |
部分电极反应产物 |
| NO2 |
NO |
| Cl2 |
HCl |
| CO |
CO2 |
| H2S |
H2SO4 |
A.上述气体检测时,敏感电极均作电池正极
B.检测分别含H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
C.检测H2S时,对电极充入空气,对电极上的电极反应式为O2 + 2H2O+ 4e- = 4OH-
D.检测Cl2时,敏感电极的电极反应式为:Cl2 + 2e-= 2Cl-
下图是一个化学过程的示意图。已知甲池的总反应式为:
2CH3OH+3O2+4KOH  2K2CO3+6H2O
2K2CO3+6H2O
(1)甲电池是 装置,A(石墨)电极的名称是 。
(2)写出电极反应式:
通入CH3OH的电极的电极反应式是 。
B(Ag)电极的电极反应式为 ,
(3)乙池中反应的总反应方程式为 。
(4)当乙池中A(Ag)极的质量增加5.40g时,甲池中理论上消耗O2
mL(标准状况下)。
如图为锌铜显示原电池装置图,下列说法不正确
| A.电子由Zn极流向Cu极 |
B.该装置的总反应 |
| C.一段时间后,A池带正电荷,B池带负电荷 |
| D.取出盐桥,电流计指针不再偏转 |
下图为铜锌原电池示意图,按该装置进行实验下列说法正确的是
| A.锌片逐渐溶解 |
| B.烧杯中溶液逐渐呈蓝色 |
| C.电子由铜片通过导线流向锌片 |
| D.该装置能将电能转变为化学能 |
直接NaBH4/H2O2燃料电池(DBFC)的结构如图,有关该电池的说法不正确的是( )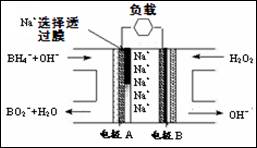
A.电极B材料中包含MnO2层,MnO2可起催化作用
B.电池负极区电极反应: BH4-+8OH--8e-=BO2-+6H2O
C.放电过程中,Na+从正极区向负极区迁移
D.在电池反应中,每消耗1L6mol/LH2O2溶液,理论上流过
电路中的电子为12NA个
硼化钒(VB2)—空气电池是目前储电能力最高的电池,电池示意图如下。
该电池工作时总反应为:4VB2 + 11O2= 4B2O3 + 2V2O5。下列说法正确的是
| A.硼化钒(VB2)为电池的正极 |
| B.电池持续反应过程中,选择性透过膜只能用阳离子交换膜 |
| C.电路中通过1mole−时消耗硼化钒6.6g |
| D.VB2极发生的电极反应为:2VB2 + 28OH--22e−= 2VO3- + 4B(OH)4-+ 6H2O |
银锌电池(钮扣式电池)的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;
Ag2O+H2O+2e- = 2Ag+2OH- ;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是( )
| A.锌为正极,Ag2O为负极 | B.锌为负极,Ag2O为正极 |
| C.原电池工作时,正极区PH减小 | D.原电池工作时,负极区PH增大 |
仔细观察下图,根据题意对图中两极进行必要的连接后填空:
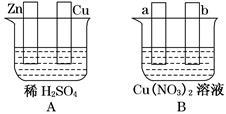
(1)若在图A中,使铜片上冒H2气泡。则加以必要的连接后的装置叫 。
(2)若在图B中,a、b为惰性电极,进行必要的连接后使b极析出1.28g铜,则a极析出的物质的物质的量为 ,反应的总反应方程式为 。
(3)若将图A中Zn、Cu两极与图B中a、b作必要的边接后,也能产生与(1)、(2)完全相同的现象,则Cu极连_______极(填a或b)。经过一段时间后,停止反应并搅匀溶液,图B中溶液的pH_________(填写“升高”、“降低”或“不变”),欲使溶液恢复至与反应前完全一致,则应加入的一定量的物质是_________。
| A.CuO | B.Cu(OH)2 | C.Cu2(OH)2CO3 | D.CuCO3 |
试题篮
()