如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42﹣═2PbSO4+2H2O.下列有关说法正确的是
| A.K与N相接时,能量由电能转化为化学能 |
| B.K与N相接时,Pb上发生反应为:Pb-2e- = Pb2+ |
| C.K与M连接时,所用电源的a极为负极 |
| D.K与M连接时,PbO2上发生反应为:PbO2+4e_+4H++SO42﹣═PbSO4+2H2O |
将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,若在一极析出0.3molCu,此时在另一极上产生的气体体积(标准状况)为
| A.3.36L | B.4.48L | C.5.6L | D.6.72L |
LiOH是制备锂离子电池的材料,可由电解法制备。工业上利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。下列说法正确的是
| A.B极区电解液为LiOH溶液 |
| B.电极每产生22.4L气体,电路中转移2mole- |
| C.电解过程中Li+迁移入B电极区、OH-迁移入A电极区 |
D.电解池中总反应方程式为:2HCl 2H2↑+Cl2↑ 2H2↑+Cl2↑ |
二氧化氯(ClO2)是一种广谱、高效的消毒剂,易溶于水,尤其在水处理等方面有广泛应用。以下是某校化学研究小组设计实验室制取ClO2的工艺流程图。下列有关说法正确的是
A.电解时发生反应的化学方程式为: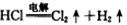 |
| B.由NaClO3溶液制取0.6mol ClO2时,至少消耗0.1mol NCl3 |
| C.将产生的混合气体通过盛有碱石灰的干燥器以除去ClO2中的NH3 |
| D.溶液X的成分为NaClO3和NaOH |
短周期主族元素A、B、C、D、E的原子序数依次递增,A的单质在常温下呈气态,D元素的单质既能与盐酸反应也能与NaOH溶液反应,B、C、E原子的最外层电子数之和为13,E原子的最外层电子数是B原子内层电子数的3倍或是C原子最外层电子数的3倍。下列说法正确的是
A.原子半径的大小顺序:r(B)>r(C)>r(A)
B.元素E的氧化物的水化物一定是强酸
C.D单质在一定条件下可以与氧化铁发生置换反应
D.工业上常用电解元素C、D的氯化物来制取它们的单质
某兴趣小组设计如图所示的微型实验装置,实验时,先断开K2,闭合K1,两极均有气泡产生,一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl- Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,铜电极附近溶液变红 |
| C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e-=2Cl- |
| D.断开K1,闭合K2时,石墨电极作正极 |
水处理主要包括水的净化、污水处理、硬水软化和海水淡化等。
(1)水处理技术的核心是减少或除去水中的各种杂质离子。目前,______________________和是主要的去离子方法。
(2)ClO2是一种性能优良的消毒剂,可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性离子氧化除去。写出ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式______________________________。
(3)地下水往往含有钙、镁的碳酸盐,自来水厂需要对地下水进行____________处理。把进行过离子交换的CaR2(或MgR2)型树脂置于_______________中浸泡一段时间后便可再生。
(4)海水的淡化是除去海水中所含的盐分,如图是利用电渗析法由海水获得淡水的原理图。已知海水中含有Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。
①阳离子交换膜是指_______________(填“A”或“B”);
②写出通电后阳极区的电极反应式____________。
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如下,下列说法不正确的是
| A.A为电源正极 |
| B.阳极区溶液中发生的氧化还原反应为:Cr2O72- +6Fe2+ +14H+ = 2Cr3+ +6Fe3+ + 7H2O |
| C.阴极区附近溶液pH降低 |
| D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O72-被还原 |
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2mol Cu(OH)2恰好恢复到电解前的浓度和pH.则电解过程中转移电子的总物质的量为( )
| A.0.2mol | B.0.4mol | C.0.6mol | D.0.8mol |
利用钠碱循环法可脱除烟气中的SO2。在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得。当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下: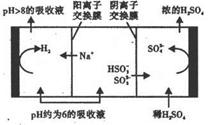
下列有关上述过程的说法错误的是
| A.NaOH溶液吸收SO2制得Na2SO3溶液的离子方程式:2OH-+SO2=SO32-+H2O |
| B.当吸收液呈中性时,溶液中的离子浓度满足:c(Na+)=2c(SO32-)+c(HSO3-) |
C.吸收液吸收SO2的过程中,pH与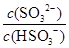 的大小成反比 的大小成反比 |
| D.HSO3-在阳极放电时的电极反应式:HSO3-+H2O-2e-=S042- +3H+ |
下图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量。接通电源后,d极附近显红色。下列说法正确的是
| A.电源B端是正极 |
| B.a、c电极均有单质生成,其物质的量之比为2:1 |
| C.欲用丁装置给铜镀银,N应为Ag,电解液为AgNO3溶液 |
| D.f极附近变红,说明氢氧化铁胶粒带正电荷 |
近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI + 3H2O  KIO3 + 3H2↑。下列有关说法正确的是
KIO3 + 3H2↑。下列有关说法正确的是
| A.电解时,石墨作阴极,不锈钢作阳极 |
| B.电解时,阳极反应是: I – – 6e – + 3H2O = IO3 – + 6H+ |
| C.溶液调节至强酸性,对生产有利 |
| D.电解前后溶液的pH几乎不变 |
如图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是( )

| A.该过程是电能转化为化学能的过程 |
| B.一段时间后,①池中n(KHCO3)不变 |
| C.一段时间后,②池中溶液的pH 一定下降 |
| D.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O |
如图装置电解一段时间,当某极析出0.32gCu时,I、Ⅱ、Ⅲ中溶液pH分别为 (溶液足量,体积均为100mL且电解前后溶液体积变化及气体的溶解忽略不计)( )

| A.13、7、1 | B.12、7、2 | C.1、7、13 | D.7、13、1 |
试题篮
()