氢化钠(NaH)是一种白色的离子化合物,其中钠元素显+1价;氢化钠与水反应放出氢气。下列叙述中,不正确的是
| A.NaH中存在-1价的氢离子,还原性比氢原子强 |
| B.NaH与H2O反应时水作氧化剂,反应放出热量 |
| C.NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 |
| D.微粒半径:H+>H>H- |
【化学—物质结构与性质】
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要作用。
请回答下列问题。
(1)砷原子外围电子排布式为 。
(2)熔沸点:NH3 PH3(>、<、=)原因是
(3)N、P、As三种元素电负性由小到大的顺序为 ,NCl3分子中中心原子的杂化方式为 。
(4)汽车尾气中CO和NO 经催化剂作用变成N2和CO
经催化剂作用变成N2和CO 2,此反应中三种元素第一电离能由小到大的顺序为 ,在这四种物质中含有极性键的非极分子内
2,此反应中三种元素第一电离能由小到大的顺序为 ,在这四种物质中含有极性键的非极分子内 键和
键和 键的比为 。
键的比为 。
(5)K3[Fe(CN)6]配合物中微粒的相互作用力有 ,配位体为 。
| A.氢键 | B.离子键 | C.共价键 | D.配位键[E.范德华力 |
(6)CO、NH3都能提供孤电子对与Cu+形成配合物。Cu+与NH3形成的配合物可表示为
[Cu(NH3)n]+。该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子 对,则[Cu(NH3)n]+中n的值为
对,则[Cu(NH3)n]+中n的值为  。
。
下列四种判断:①两种弱酸相互反应生成两种强酸;②两种弱酸盐相互作用后生成两种强酸盐;③一种弱酸和一种盐溶液作用后,得到一种强酸和一种盐;④两种酸溶液混合后,溶液的酸性减弱。其中有具体例证的是( )
| A.①②③④ | B.①②③ | C.②③④ | D.①③④ |
[化学——选修物质结构与性质](15分)
原子序数依次增大A、B、C、D、E、F(A、B、C、D、E、F分别代表元素符号)六种短周期元素。元素A的原子半径在短周期中最小,元素C的单质在空气中含量最多, 比
比 少一个电子层,E所在周期的各元素单质沸点变化如下图(元素按原子序数递增顺序连续排列),B、C两种元素分别能与A形成等电子的
少一个电子层,E所在周期的各元素单质沸点变化如下图(元素按原子序数递增顺序连续排列),B、C两种元素分别能与A形成等电子的 甲、乙两种分子,且两种
甲、乙两种分子,且两种
分子中各原子的个数见下表:
| 化合物 |
甲 |
乙 |
| 原子个数比 |
B:A=1:4 |
C:A=1:3 |
(1)元素F的基态原子的电子排布式为 。
(2)分子甲的空间构型为 ,该分子中B的
原子轨道发生的是 杂化。
(3)E单质属于 晶体,E与A元素形成 分子(填“极性”或“非极性”)
(4)D在F中燃烧的产物属于 晶体,其晶体中与 最近且等距离的
最近且等距离的 有 个。
有 个。
(5)C元素的第一电离能( ) 氧元素的第一电离能(
) 氧元素的第一电离能( )(填“<”或“>”或“=”)。
)(填“<”或“>”或“=”)。
已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2—离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2。
 请回答下列问题:
请回答下列问题:
⑴A、B、C、D四种元素中,电负性最大的是 ▲ (填元素符号)。
⑵B的氢化物的沸点远高于A的氢化物的主要原因是 ▲ 。
⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为 ▲ 。
⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有 ▲ 。
⑸最近发现,只含A、D、E三种元素的一种晶体(晶胞如右图所示)具有超导性。A原子的配位数为 ▲ ;该晶体的化学式为 ▲ 。
已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是 ( )
A.E、G、L、M都是10e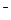 微粒 微粒 |
B.L、M都是极性分子 |
| C.L能使紫色石蕊试液变蓝色 | D.E离子中,质子数一定大于中子数 |
设NA代表阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol H2O和D2O组成的混合物中含有中子数是NA |
| B.28g N60(分子结构如右图所示)中含有的N—N键数目为1.5NA |
| C.25℃、1.01×105Pa时,16g氧气中所含的原子数为NA |
| D.常温下浓度都为0.1mol/L,体积相等的NaF和CH3COONa溶液中,离子数目都为0.2NA |
[物质结构与性质]现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1="738kJ/mol " I2 =" 1451" kJ/mol I3 =" 7733kJ/mol " I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5 为离子化合物,写出其电子式
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
该同学所画的电子排布图违背了
(4) G位于 族 区,价电子排布式为
(5) DE3 中心原子的杂化方式为 ,用价层电子对互斥理论推测其空间构型为
(6)检验F元素的方法是 ,请用 原子结构的知识解释产生此现象的原因是
原子结构的知识解释产生此现象的原因是
(7) F元素的晶胞如右图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,F原子的摩尔质量为M,则F原子的半径为 cm
共价键、离子键和分子间作用力是粒子之间的三种不同作用力。下列物质的品体中:①Na2O2 ②CO2 ③金刚石 ④NaCl ⑤白磷,含有上述两种作用力的是 ( )
| A.①②⑤ | B.①②③ |
| C.②④⑤ | D.②③⑤ |
NH3、H2O等是极性分子,CO2、BF3、CC14等是极性键构成的非极性分子。根据上述事实可推出ABn型分子是非极性分子的经验规律是( )
| A.在ABn分子中A原子的所有价电子都参与成键 |
| B.在ABn分子中A的相对原子质量应小于B的相对原子质量 |
| C.在ABn分子中每个共价键的键长都相等 |
| D.分子中不能含有H原子 |
【皖南八校2009届高三第二次联考12月】类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下表中有关推论正确的是
| |
已知事实 |
推论 |
| A |
Na2CO3溶液在空气中不易变质 |
水玻璃在空气中不易变质 |
| B |
乙烯分子内所有原子在同一平面上 |
丙烯分子内所有原子在同一平面上 |
| C |
乙烯在空气中燃烧有黑烟 |
苯在空气中燃烧产生的烟更浓 |
| D |
Na在空气中燃烧生成Na2O2 |
Li在空气中燃烧生成Li2O2 |
下列说法中错误的是()
| A. |
|
| B. |
在 |
| C. |
元素电负性越大的原子,吸引电子的能力越强 |
| D. |
原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
下列对有机物结构或性质的描述,错误的是
| A. |
一定条件下,
|
| B. |
苯酚钠溶液中通入
|
| C. |
乙烷和丙烯的物质的量各1
|
| D. |
光照下2,2-二甲基丙烷与
|
试题篮
()