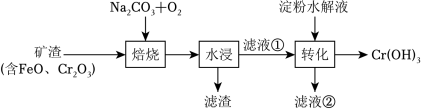
某工厂采用如图工艺制备 Cr(OH)3,已知焙烧后 Cr元素以 +6价形式存在,下列说法错误的是( )
| A. |
“焙烧”中产生 CO2 |
| B. |
滤渣的主要成分为 Fe(OH)2 |
| C. |
滤液①中 Cr元素的主要存在形式为 CrO42- |
| D. |
淀粉水解液中的葡萄糖起还原作用 |
某种镁盐具有良好的电化学性能,其阴离子结构如图所示。 W、X、Y、Z、Q是核电荷数依次增大的短周期元素, W、Y原子序数之和等于 Z, Y原子价电子数是 Q原子价电子数的 2倍。下列说法错误的是( )
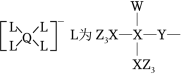
| A. |
W与 Y的化合物为极性分子 |
| B. |
第一电离能: Z>X>Y |
| C. |
Q的氧化物是两性氧化物 |
| D. |
该阴离子中含有配位键 |
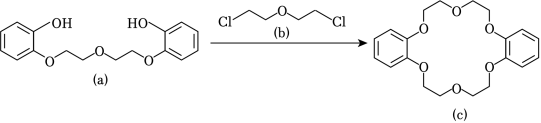
冠醚因分子结构形如皇冠而得名,某冠醚分子 c可识别 K+,其合成方法如图。下列说法错误的是( )
| A. |
该反应为取代反应 |
| B. |
a、b均可与 NaOH溶液反应 |
| C. |
c核磁共振氢谱有 3组峰 |
| D. |
c可增加 KI在苯中的溶解度 |
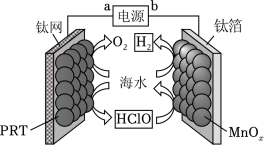
某无隔膜流动海水电解法制 H2的装置如图所示,其中高选择性催化剂 PRT可抑制 O2产生。下列说法正确的是( )
| A. |
b端电势高于 a端电势 |
| B. |
理论上转移 2mole﹣生成 4gH2 |
| C. |
电解后海水 pH下降 |
| D. |
阳极发生: Cl﹣+H2O﹣2e﹣═HClO+H+ |
在光照下,螺吡喃发生开、闭环转换而变色,过程如图。下列关于开、闭环螺吡喃说法正确的是( )
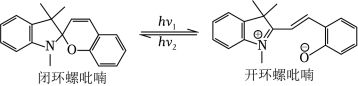
| A. |
均有手性 |
| B. |
互为同分异构体 |
| C. |
N原子杂化方式相同 |
| D. |
闭环螺吡喃亲水性更好 |
我国古代四大发明之一黑火药的爆炸反应为: S+2KNO3+3C═K2S+N2↑+3CO2↑。设 NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. |
11.2LCO2含 π键数目为 NA |
| B. |
每生成 2.8gN2转移电子数目为 NA |
| C. |
0.1molKNO3晶体中含离子数目为 0.2NA |
| D. |
1L0.1mol•L﹣1K2S溶液中含 S2﹣数目为 0.1NA |
下列鉴别或检验不能达到实验目的是( )
| A. |
用石灰水鉴别 Na2CO3与 NaHCO3 |
| B. |
用 KSCN溶液检验 FeSO4是否变质 |
| C. |
用盐酸酸化的 BaCl2溶液检验 Na2SO3是否被氧化 |
| D. |
加热条件下用银氨溶液检验乙醇中是否混有乙醛 |
下列有关物质的工业制备反应错误的是( )
| A. |
合成氨:
N2+3H2 |
| B. |
制
HCl:
H2+Cl2 |
| C. |
制粗硅:
SiO2+2C |
| D. |
冶炼镁:
2MgO |
下列化学用语或表述正确的是( )
| A. |
BeCl2的空间结构: V形 |
| B. |
P4中的共价键类型:非极性键 |
| C. |
基态 Ni原子价电子排布式: 3d10 |
| D. |
顺
﹣2﹣丁烯的结构简式: |
科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是( )
| A. |
利用 CO2合成了脂肪酸:实现了无机小分子向有机高分子的转变 |
| B. |
发现了月壤中的“嫦娥石 [(Ca8Y)Fe(PO4)7]”:其成分属于无机盐 |
| C. |
研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能 |
| D. |
革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀 |
如图为Fe(OH)3、Al(OH)3和Cu(OH)2在水中达沉淀溶解平衡时的pM﹣pH关系图{pM=﹣lg[c(M)/(mol•L﹣1)];c(M)≤10﹣5mol•L﹣1可认为M离子沉淀完全}。下列叙述正确的是( )
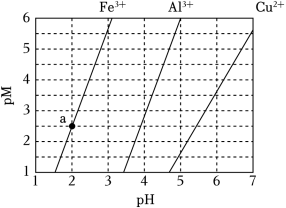
| A. |
由a点可求得 Ksp[Fe(OH)3]=10﹣8.5 |
| B. |
pH=4时 Al(OH)3的溶解度为 10-103mol•L﹣1 |
| C. |
浓度均为0.01mol•L﹣1的Al3+和Fe3+可通过分步沉淀进行分离 |
| D. |
Al3+、Cu2+混合溶液中c(Cu2+)=0.2mol•L﹣1时二者不会同时沉淀 |
用可再生能源电还原CO2时,采用高浓度的K+抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如图所示。下列说法正确的是( )
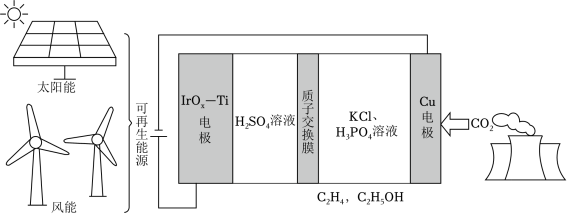
| A. |
析氢反应发生在IrOx﹣Ti电极上 |
| B. |
Cl﹣从Cu电极迁移到IrOx﹣Ti电极 |
| C. |
阴极发生的反应有:2CO2+12H++12e﹣═C2H4+4H2O |
| D. |
每转移1mol电子,阳极生成11.2L气体(标准状况) |
W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与其K层电子数相等,WX2是形成酸雨的物质之一。下列说法正确的是( )
| A. |
原子半径:X>W |
| B. |
简单氢化物的沸点:X<Z |
| C. |
Y与X可形成离子化合物 |
| D. |
Z的最高价含氧酸是弱酸 |
NA为阿伏加德罗常数的值。下列叙述正确的是( )
| A. |
0.50mol异丁烷分子中共价键的数目为6.5NA |
| B. |
标准状况下,2.24LSO3中电子的数目为4.00NA |
| C. |
1.0LpH=2的H2SO4溶液中H+的数目为0.02NA |
| D. |
1.0L1.0mol•L﹣1的Na2CO3溶液中 CO2-3的数目为1.0NA |
试题篮
()