有关下列物质分子结构特征描述正确的是
| A.乙烯容易与溴的四氯化碳溶液发生反应,且1mol乙烯完全加成消耗1mol溴单质,证明乙烯分子里含有一个碳碳双键 |
| B.苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构 |
C.和 属于同一种物质,不能用来解释甲烷是一种正四面体结构 属于同一种物质,不能用来解释甲烷是一种正四面体结构 |
| D.1mol CH3CH2OH与Na完全反应只生成0.5 mol H2,不能说明乙醇分子中有一个氢原子与其它氢原子不同 |
(共13分)从薄荷油中得到一种烃A(C10H16),叫α-非兰烃,与A相关反应如下:

(即碳碳双键的碳原子上若有一个氢原子,氧化后形成羧基,若无氢原子,则氧化后生成羰基)
(1)D→E的反应类型为 。
(2)B所含官能团的名称为 。
(3)G为含六元环的化合物,写出其结构简式 。
(4)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂的链节为 。
(5)写出E→F(已知F的分子式C3H3O2Na)的化学方程式 。
(6)A与Br2加成后的可能产物共有 种(不考虑立体异构)
(7)C的同分异构体有多种,写出一种满足下列条件的同分异构体的结构简式 。
①含两个—COOCH3基团
②核磁共振氢谱呈现2个吸收峰
已知:NH2COO-+2H2O HCO3-+NH3·H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示。以下分析正确的是
HCO3-+NH3·H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示。以下分析正确的是
| A.无法判断T1和T2的大小关系 |
| B.T1℃时,第6min反应物转化率为6.25% |
| C.T2℃时,0~6min ν(NH2COO-)=0.3mol·L-1·min-1 |
| D.往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小 |
下列说法正确的是
| A.常温下,0.1 mol/L的下列溶液①NH4Al(SO4)2;②NH4Cl;③NH3·H2O;④CH3COONH4⑤(NH4)2SO4中,c(NH4+)由大到小的顺序是:⑤>②>①>④>③ |
| B.常温下,0.4 mol/L HB溶液和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为: c(B—)>c(H+)>c(Na+)>c(OH—) |
| C.常温下,将CH3COONa、HCl两溶液混合后,溶液呈中性,溶液中c(Na+)大于c(Cl-)。 |
| D.pH相等的下列溶液:a.CH3COOK、b.NaHCO3、c.Na2CO3、d.NaOH,其物质的量浓度由小到大顺序 为:d<c<a<b |
乙烯与乙烷的混合气体共amol,与bmol氧气共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45g水,则下列说法错误的是
| A.当a=1时,乙烯和乙烷的物质的量之比为1:1 |
| B.当a=1时,且反应后CO和CO2的混合气体的物质的量为反应前氧气的2/3时,则b=3 |
| C.当a=1时,且反应后CO和CO2的混合气体的物质的量为反应前氧气的2/3时,则CO和CO2的物质的量之比为3:1 |
| D.a的取值范围为5/6<a<5/4 |
4.6g铜和镁的合金完全溶于浓硝酸,反应后硝酸被还原只生成4480mL的NO2气体和336mL的N2O4气体(气体体积都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为
| A.9.02g | B.8.51g | C.8.26g | D.7.04g |
在2 L的恒容密闭容器中,发生反应:A(g)+B(g) 2C(g)+D(s) △H=-a kJ·mol-1
2C(g)+D(s) △H=-a kJ·mol-1
实验内容和结果分别如下表和下图所示。下列说法正确的是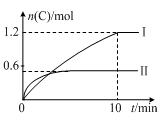
| 实验 序号 |
温度 |
起始物质的量 |
热量 变化 |
|
| A |
B |
|||
| Ⅰ |
600℃ |
1 mol |
3 mol |
96 kJ |
| Ⅱ |
800℃ |
0.5 mol |
1.5mol |
—— |
A.实验Ⅰ中,10 min内平均速率v(B)=0.06 mol·L-1·min-1
B.600℃时,上述方程式中a=160
C.600 ℃时,该反应的平衡常数是0.45
D.向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率不变
以NA表示阿伏加德罗常数的值,下列说法错误的是
| A.18g冰(图1)中含O—H键数目为2NA |
| B.28g晶体硅(图2)中含有Si—Si键数目为2NA |
| C.44g干冰(图3)中含有NA个晶胞结构单元 |
| D.石墨烯(图4)是碳原子单层片状新材料,12g石墨烯中含C—C键数目为1.5NA |
标准状况下两种等物质的量的可燃气体共1.68L,其中一种是烃,在足量氧气中完全燃烧。若将产物通入足量澄清石灰水,得到的白色沉淀质量为15.0g;若用足量碱石灰吸收燃烧产物,增重9.3g。则这两种混合气体可能为
| A.H2与C2H4 | B.CO与C2H4 | C.H2与C4H6 | D.CO与C3H6 |
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P="O" ckJ·mol—1、O=O dkJ·mol—1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
| A.(6a+5d-4c-12b)kJ·mol—1 | B.(4c+12b-6a-5d)kJ·mol—1 |
| C.(4c+12b-4a-5d)kJ·mol—1 | D.(4a+5d-4c-12b)kJ·mol—1 |
25℃时,浓度均为0.1mol·L-1的HA溶液和BOH溶液,pH分别是1和12。下列说法正确的是
| A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(OH-) |
| B.若将0.1mol·L-1BOH溶液稀释至0.001 mol·L-1则溶液的pH=10 |
| C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+) |
| D.若将上述两溶液按体积比l:2混合,则混合液中:c(B+)>c(A-)>c(OH-)>c(H+) |
某强酸性溶液X中含有NH4+、A13+、Ba2+、Fe2+、CO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行如下实验:
下列有关推断合理的是
| A.溶液中一定没有Ba2+、NO3-、CO32- |
| B.溶液中一定含有H+、NH4+、Fe2+、SO42-、Cl- |
| C.沉淀H为一定Al(OH)3和BaCO3的混合物 |
| D.若溶液X的体积为100 mL,产生标况下112 mL气体A,则X中c(Fe2+)=0.05mol·L-1 |
电离度是指弱电解质在溶液里达电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的)的百分数,下表中是三种酸在相同温度下的一些数据,有关判断正确的是
| 酸 |
HX |
HY |
HZ |
||
| 浓度(mol/L) |
0.12 |
0.2 |
0.9 |
1 |
1 |
| 电离度 |
0.25 |
0.2 |
0.1 |
0.3 |
0.5 |
| 电离常数 |
K1 |
K2 |
K3 |
K4 |
K5 |
A.在相同温度,从HX的数据可以说明:弱电解质溶液,浓度越低,电离度越大,且K1>K2>K3=0.01
B.室温时,若在NaZ溶液中加水,则c(Z-)/[c(HZ)• c(OH-)]的比值变小,若加少量盐酸,则比值变大
C.等物质的量的NaX、NaY和NaZ混合后,c(X-)+c(Y-)-2c(Z-)=2c(HZ)-c(HX)-c(HY),且c(Z-)<c(Y-)<c(X-)
D.在相同温度下,K5>K4>K3
煤气化的一种方法是在气化炉中给煤炭加氢,发生的主要反应为:C(s)+2H2(g) CH4(g)
CH4(g)
在VL的容器中投入a mol碳(足量),同时通入a mol H2,控制条件使其发生上述反应,实验测得H2的平衡转化率随压强及温度的变化关系如图所示。下列说法正确的是
| A.上述逆反应为吸热反应 |
B.在5MPa, 800K时,该反应的平衡常数为 |
C.在4MPa, 1200K时,图中X点 |
| D.工业上维持6 MPa、1000K而不采用10 MPa、1000K,主要是因为前者氢气的转化率高 |
试题篮
()