(17分)碳及其化合物与人类生产、生活密切相关。(1)在化工生产过程中,少量CO的存在会引起催化剂中毒,为了防止催化剂中毒,常用SO2将CO氧化,SO2被还原为S。
已知:C(s)+1/2O2(g)=CO(g)△H1=-126.4kJ·mol-1
C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
S(s)+O2(g)=SO2(g) △H3=-296.8kJ·mol-1
则SO2氧化CO的热化学反应方程式为____________。
(2)CO可用于合成甲醇,化学方程式为CO(g)+2H2(g) CH3OH(g) △H=-90.8KJ·mol-1。
CH3OH(g) △H=-90.8KJ·mol-1。
①在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是______℃;该温度下上述反应的化学平衡常数为_______。曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为___________;
②在密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状。当改变某一反应条件后,下列变化能说明平衡一定向正反应方向移动的是______(填序号)。
| A.正反应速率瞬间增大,后逐渐减小 |
| B.混合气体的密度增大 |
| C.化学平衡常数K值增大 |
| D.反应物的体积百分含量增大 |
(3)一种新型CO燃料电池工作原理如图所示。
①负极电极反应式为_______________________;
②电极A处产生的CO2有部分参与循环利用,其利用率为____________。
(17分)电化学原理在金属腐蚀、能量转换、物质合成等方面应用广泛。
(1)通常可用图l、图2所示的两种方式减缓海水埘钢闸门A的腐蚀,则图l中材料B通常选择_________(填字母序号),图2 中材料C最好选择_________(填字母序号)。
a.钠块 b.铜块 c.锌块 d.石墨
则图2中C上发生的主要电极反应式为___________________。
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①D为该燃料电池的________极(填“正”或“负”)。E电极上的电极反应式为_______。
②镁燃料电池负极容易发生自腐蚀使负极利用率降低,该过程中产生的气体a为_______(填化学式)。
(3)乙醇酸(HOOC—CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸。
①乙二醛(OHC—CHO)与M电极的气体产物反应生成乙醛酸,则反应的化学方程式为____________。
②该电解装置工作中若有0.5molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为____________mol。
【化学——选修3 物质结构与性质】选考下图为元素周期表的一部分,字母下方数值为该元素电负性,根据信息回答下列问题(用相应元素符号进行答题):
(1)b、h两元素可形成化合物bh2,写出其电子式: 。
(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为 ,eg3、e2g6中心原子e的杂化方式分别为 、 。
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式: 。
(4)f、g、h、i四种元素对应单质分子的键能如下表:
| 共价键 |
f—f |
g—g |
h—h |
i—i |
| 键能(kJ/mol) |
157 |
242.7 |
193.7 |
152.7 |
试从原子半径角度阐述f—f键键能反常的原因: 。
(5)c元素的元素符号是 ,价电子排布式为 ,下图是
一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图中勾画出该晶体的一个晶胞。计算出该合金的化学式为: 。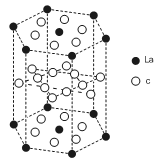
氯化硫酰(SO2Cl2)是一种无色液体,遇水剧烈水解,其熔点为-54.1 ℃,沸点为69.1 ℃,可用作氯化剂及锂电池正极活性物质。氯化硫酰可用下列反应制取:
SO2(g)+Cl2(g) SO2Cl2(l) △H=-97.3 kJ/mol。
SO2Cl2(l) △H=-97.3 kJ/mol。
(1)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是(用字母编号填写): 。
a.缩小容器体积 b.使用催化剂 c.提高SO2浓度 d.提高温度
(2)300 ℃时,在体积为1 L的密闭容器中充入16.20 g SO2Cl2,达到平衡时容器中含SO2 7.616 g,则300 ℃时合成SO2Cl2反应的平衡常数的为: 。
(3)某同学设计了下图所示装置制取氯化硫酰:
①有关该装置的说法正确的是(用字母编号填写): 。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性炭起催化作用
c.B处反应管的冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
②从化学平衡的角度分析,反应管通冷却水的目的是: 。
③氯磺酸(ClSO3H)受热分解也可制得氯化硫酰,并得到另外一种物质,该反应的化学方程式为______,分离产物的方法是: 。
(4)下图为GET公司开发的Li-SO2Cl2军用电池的示意图。已知该电池的总反应为:2Li+SO2Cl2=2LiCl+SO2↑,则该电池工作时的正极反应为:_______________________。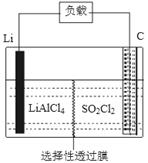
以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,用化学沉降法处理含砷废水,相关数据如下表。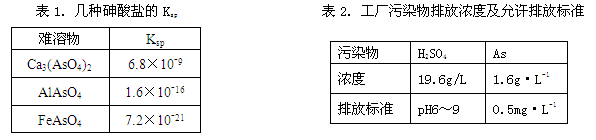
回答以下问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)= mol·L-1。
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]= ,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,c(AsO43-)的最大是 mol·L-1。
(3)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 。
(14分)氨的合成是最重要的化工生产之一。
Ⅰ.工业上合成氨用的H2有多种制取的方法:
① 用焦炭跟水反应:C(s)+H2O(g) CO(g) + H2(g);
CO(g) + H2(g);
② 用天然气跟水蒸气反应:CH4(g)+H2O(g)  CO(g)+3H2(g)
CO(g)+3H2(g)
已知有关反应的能量变化如下图,且方法②的反应为吸热反应,则方法②中反应的ΔH =___________kJ/moL。
Ⅱ.在3个1L的密闭容器中,同温度下、使用相同催化剂分别进行反应:
3H2(g)+N2(g)  2NH3(g)
2NH3(g)
按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
| 容 器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
3 mol H2、2 mol N2 |
6 mol H2、4mol N2 |
2 mol NH3 |
| 达到平衡的时间(min) |
t |
5 |
8 |
| 平衡时N2的浓度(mol·L-1) |
c1 |
3 |
c2 |
(1)下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)甲容器中达到平衡所需要的时间t 5min,表中c1 c2。(填“>”、“<” 或“=”)
(3)用氨合成尿素的反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)。工业生产时,原料气带有水蒸气。图1表示CO2的转化率与氨碳比
CO(NH2)2(s)+H2O(g)。工业生产时,原料气带有水蒸气。图1表示CO2的转化率与氨碳比 、水碳比
、水碳比 的变化关系。
的变化关系。
①曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是 。
②测得B点氨的转化率为30%,则x1= 。
Ⅲ.有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图2所示。
电池正极的电极反应式是 ,A是 。
[化学——选修3:物质结构与性质] 周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族,e的最外层只有1个电子,但次外层有18个电子。请填写下列空白。
(1)e元素基态原子的核外电子排布式为____________。
(2)b、c、d三种元素的第一电离能数值由小到大的顺序为____________(填元素符号),其原因是__________________。
(3)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;分子中既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写出两种)。
(4)已知c、e能形成晶胞如图甲和图乙所示的两种化合物,化合物的化学式为分别为:甲________,乙 ;甲高温易转化为乙的原因是__________________。
(5)这5种元素形成的一种1∶1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图丙所示)。该化合物中,阴离子为 ,该化合物加热时首先失去的组分是 ,判断理由是 。
[化学——选修2:化学与技术]铁、铝是现代金属材料的主角。但其腐蚀造成很大的经济损失,寻求金属制品抗腐蚀处理的方法意义重大。
(1)一种钢铁防腐的方法是将钢铁放在冷的浓硝酸中浸泡。但是加热或在稀HNO3中,铁与硝酸会不断反应。不同浓度的 HNO3与铁反应的还原产物很复杂,其分布曲线如图。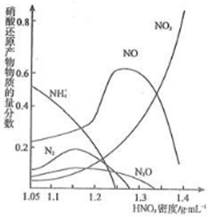
①钢铁在冷的浓硝酸中浸泡能防腐的原因是: 。
②工业上一般不用冷浓硝酸进行铁表面处理,其可能的原因是: 。
③由图示可知,密度等于1.35 g/mL 的硝酸与铁反应时,其还原产物主要是 ; 请用一句话概括该图反映出的基本结论 。
(2)以下为铝材表面处理的一种方法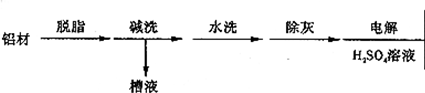
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是 (用离子方程式表示)。为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应为 。电解后的铝材再经氨洗的目的是 。
③取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是 。
氮化硅(Si3N4)是一种优良的高温结构陶瓷,在航天航空、汽车发动机、机械等领域有着广泛的用途。工业上有多种方法来制备氮化硅,常见的方法有:
(1)在1 300-l 400℃时,高纯粉状硅与纯氮气化合,其反应方程式为_________。
(2)在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl。
①已知:25℃,101 kPa条件下的热化学方程式:
3Si(s)+2N2(g)=Si3N4(s) △H= -750.2kJ/mol
Si(s)+2Cl2(g)=SiCl4(g) △H="-609.6" kJ/mol
H2(g)+Cl2(g)=2HCl(g) △H="--184.6" kJ/mol
四氯化硅气体与氮气、氢气反应的热化学方程式为____________________。
②工业上制取高纯硅和四氯化硅的生产流程如下:
已知:X,高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
上述生产流程中电解A的水溶液时,阳极材料能否用Cu?________(填“能”或“不能”)。写出Cu为阳极电解A的水溶液开始一段时间阴阳极的电极方程式。阳极: ;阴极: 。
(3)由石英砂合成氮化硅粉末的路线图如下所示
(把图中的①·⑤改为I-V)
①石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式表示其原因: 。
②图示I-V的变化中,属于氧化还原反应的是 。
③SiCl4在潮湿的空气中剧烈水解,产生白雾,军事工业中用于制造烟雾剂。SiCl4水解的化学方程式为___________________。
④在反应IV中四氯化硅与氨气反应生成Si(NH2)4和一种气体 (填分子式);在反应V中Si(NH2)4受热分解,分解后的另一种产物的分子式为 。
(15分)“优先反应思想”是一条重要的化学学科思想。根据所学知识及题目提供的相关数据,回答下列问题:
(1)向FeBr2溶液中滴加少量氯水,溶液变黄。你认为使溶液变黄的微粒其符号是用实验证明你的观点,简述实验操作及现象 。
(2)用惰性电极电解由等物质的量的NaBr,KI, NaCl组成的混合溶液,阳极首先发生的电极反应式是 。
(3)己知常温下一些电解质的相关数据见下表: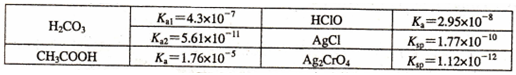
①向等物质的量浓度的Na2C03, CH3COONa, NaClO组成的混合溶液中逐滴加入稀硫酸,首先发生反应的离子方程式是 。
②向浓度均为0.010 mol/L的NaCl, Na2Cr04组成的混合溶液中逐滴加入浓度为0.010 mol-L -1AgN03溶液,首先生成的沉淀其化学式为 。
(4)分别向四份各100 ML,浓度均为2 mo1-L-1的FeC13溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
①根据表中的数据可求出粉末中铁、铜的物质的量之比为 。
②根据表中的数据分析I反应后的溶液中存在的金属阳离子有〔用离子符号表示) 。
(15分)
I.已知甲和乙在溶液中的转化关系如图所示:
请回答下列问题:
(1)若甲是10电子的单核微粒,乙是两性氢氧化物,则微粒甲的原子结构示意图为________________。
(2)若甲是10电子的阳离子,乙是碱性气体。lmol乙通人足量强酸溶液中与H+反应,反应过程中能量变化如图,该反应的热化学方程式是__________________________。
(3)若甲仅含有N03-、SO42-和X三种离子(不考虑水电离的H+、OH-),则X离子可能是_____________(填序号)。
| A.Fe2+ | B.HC03- | C.Ba2+ | D.Fe3+ |
(4)若甲是CO2,乙中HCO3-和CO32-的物质的量浓度相等,此时溶液的pH=a,则HCO3-的电离平衡常数Ka=___.
Ⅱ.在恒容密闭容器中通入X并发生反应:  ,温度
,温度
下X的物质的量浓度c(X)随时间t变化的曲线如图所示。
(5)温度 ___________
___________ (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(6)M点的正反应速率 __________N点的逆反应速率
__________N点的逆反应速率 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(7)该反应进行到M点放出的热量与进行到W点放出的热量相比:_____________(填“更多”、“更少”或“相同”)
选考[化学与技术]根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
(1)①废水I若采用CO2处理,离子方程式是______.
②废水Ⅱ常用明矾处理.实践中发现废水中的c(HCO3-)越大,净水效果越好,这是因为______.
③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++______═CH3Hg++_____
我国规定,Hg2+的排放标准不能超过0.05mg/L.对于含Hg2+的污水,可加入沉淀剂_______(填写化学式),使Hg2+除去,降低污染。
④废水Ⅳ常用Cl2氧化CN-成CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为______.
(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化刹的量,换算成氧的含量(以mg/L计).某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K2Cr2O7溶液.
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热.
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定.终点时消耗硫酸亚铁铵溶液V2 mL.
①I中,量取K2Cr207,溶液的仪器是______.
②Ⅲ中,发生的反应为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=______(用含c、V1、V2的表达式表示).
NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。
(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是 。
(2)Ⅱ中,2NO(g)+O2(g) 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(ρ1、ρ2)下随温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(ρ1、ρ2)下随温度变化的曲线(如图)。
①比较ρ1、ρ2的大小关系: 。
②随温度升高,该反应平衡常数变化的趋势是 。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
(1)已知:2NO(g) N2O4(g) ΔH1
N2O4(g) ΔH1
2NO2(g) N2O4(l) ΔH2
N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母) 。

②N2O4与O2、H2O化合的化学方程式是 。
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。为使电解产物全部转化为NH4NO3,需补充物质A。A是 ,说明理由 。
Al、Fe、Cu、S都是中学化学常见元素。
某混合物由Al2O3、Cu2O、Fe3O4组成,将该混合物进行如下处理:
①滤渣A的化学成分为____________(填化学式),则上述过程中,含“铜”物质发生反应的离子方程式为Cu2O+2H+ Cu+Cu2++H2O、__________________________;
②滤液A中有无Fe3+?___________(填“有”或“无”),验证方法是_____________(所述验证方法需与前一空的结论一致)
③向滤液A中加入过量NaOH溶液时Al3+发生反应的离子方程式为______________________。
(1)CuFeS2中Fe的化合价为_______价,CuFeS2与氧气反应可得产物Cu2S、FeS和SO2,则该反应的氧化产物为_______________________(填化学式)。
(2)SO2的排放会造成大气污染,可设计如图所示装置用SO2生产硫酸。写出SO2的电极反应方程式:________,也可用NaOH溶液吸收SO2,所得NaHSO3溶液pH<7,则该溶液中存在离子的物质的量浓度由大到小的顺序是____________________。
(16分)物质的类别和核心元素的化合价是研究物质性质的两个基本视角。
(1)图中X的电子式为 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O (填“强”或“弱”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下, ,得电子能力逐渐减弱。
(2)Na2S2O3是一种用途广泛的钠盐。
①下列物质用于Na2S2O3的从氧化还原反应的角度制备, ,理论上有可能的是 (填字母序号)。
a.Na2S+S b.Z+S c.Na2SO3+Y d.NaHS+NaHSO3
②已知反应:Na2S2O3+H2SO 4Na2SO4+S↓+SO2↑+H2O。研究其反应速率时,下列说法正确的是 (填写字母序号)。
4Na2SO4+S↓+SO2↑+H2O。研究其反应速率时,下列说法正确的是 (填写字母序号)。
a.可通过测定一段时间内生成SO2的体积,得出该反应的速率
b.可通过比较出现浑浊的时间,研究浓度、温度等因素对该反应速率的影响
c.可通过Na2S2O3固体与稀硫酸和浓硫酸的反应,研究浓度对该反应速率的影响
(3)治理含CO、SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体。
①已知:CO(g)+1/2O2(g)=CO2(g) △H=-283kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-296kJ·mol-1
则治理烟道气反应的热化学方程式为 。
②一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是 (填写字母序号)。
a.v(CO)∶v(SO2)=2∶1
b.平衡常数不变
c.气体密度不变
d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为 ,则SO2的转化率为 。
,则SO2的转化率为 。
(4)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式 。
(5)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表。
吸收CO2最合适的试剂是 (填“Ca(OH)2”或“Ba(OH)2”)溶液。
试题篮
()