下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题。
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
|
|
|
④ |
⑤ |
⑥ |
⑧ |
⑩ |
| 3 |
① |
|
|
|
|
⑦ |
⑨ |
|
| 4 |
② |
③ |
|
|
|
|
|
|
(1)在这10种元素中,化学性质最不活泼的是 (写序号),失电子能力最强的原子是_____(用元素符号表示)。
(2)在这10种元素中,最高价氧化物的水化物碱性最强的是 (填化学式),最高价氧化物的水化物酸性最强的是 (填化学式)。
(3)H分别与④、⑤、⑦、⑧、⑨形成的化合物中,最稳定的是 (填化学式);
(4)①、⑧、⑨三种元素单核离子半径由小到大的顺序是(用相应的离子符号表示):
(5)写出③和⑨形成的化合物的电子式 ,化学键类型为____ (“离子键”或“共价键”)。
已知可逆反应2A(g)+B(g) 2C(g),向容积为0.5L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得
2C(g),向容积为0.5L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得 ,放出热量Q1 kJ。
,放出热量Q1 kJ。
(1)能说明上述反应已经达到化学平衡状态的是______________(填字母编号)
a.v(C)=2v(B)
b.单位时间内生成2mol A的同时消耗1molB
c.容器内压强保持不变
d.容器内气体的密度保持不变
e.单位时间内生成1molB的同时生成2mol A
f.容器内气体的平均分子量保持不变
g.容器内气体的质量保持不变
h.容器内A物质的浓度是B物质的2倍
(2)上述反应中A的转化率a(A)= 。
(3)请写出上述反应的热化学方程式__________________。
(4)500℃时,上述反应的化学平衡常数K=____________________。
(5)一般,升高温度,化学反应的反应速率会增大。从以下图像中选择符合酶催化作用的化学反应速率随温度变化的特征 。
高炉炼铁过程中发生的主要反应为:Fe2O3(s) + 3CO(g) 2Fe(s) + 3CO2(g)。已知该反应在不同温度下的平衡常数列于表中:
2Fe(s) + 3CO2(g)。已知该反应在不同温度下的平衡常数列于表中:
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
64.0 |
50.653 |
42.875 |
(1)写出该反应的平衡常数表达式:K=____ _____。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率υ(CO2)= ;平衡时,c(CO)= 。
(3)欲提高(2)中CO的反应速率,可采取的措施是_____________。
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.提高反应温度
E.减小容器的体积
F.加入合适的催化剂
(4)在1L的密闭容器中,1300℃条件,下列达平衡状态的是 。
| n(Fe2O3) |
0.350 |
0.027 |
0.080 |
0.080 |
| n(CO) |
0.010 |
0.010 |
0.010 |
0.050 |
| n(Fe) |
0.100 |
0.064 |
0.080 |
0.080 |
| n(CO2) |
0.035 |
0.088 |
0.040 |
0.050 |
(5)铁是国家的工业基础,下列哪些装置可防止铁棒被腐蚀 ________。
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1)25℃下实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式
(2)合成氨反应:1/2N2(g)+3/2H2(g) NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成34 gNH3(g),放出92.2 kJ的热量。请回答下列问题:
NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成34 gNH3(g),放出92.2 kJ的热量。请回答下列问题:
该反应通常用铁作催化剂,加催化剂会使图中E变_____(填“大”或“小”),图中ΔH=_________
(3)由气态基态原子形成1mol化学键释放的能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 |
H-H |
N-H |
N≡N |
| 键能/kJ·mol-1 |
436 |
391 |
945 |
已知反应N2(g)+3H2(g) 2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值____。
2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值____。
(4)已知:△H2="+" 44 kJ·mol-1,△H3= -285.8kJ·mol-1
下图列出它们之间的转变关系。请计算298K时由H2O(g)生成1molH2(g)和1/2molO2(g)反应的△H1= (用△H2、△H3表示△H1计算等式), (计算△H1数据结果)。
(1)在下面元素周期表中全部是金属元素的区域为 。
(a)A (b)B (c)C (d)D
(2)短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍;Y元素单质为双原子分子,其氢化物水溶液呈碱性;1mol单质Z跟盐酸完全反应,能置换出22.4L的H2(标准状况);W元素原子核外M层电子数目比K层多1个;
①请写出元素X的一种核素的化学符号 ;
②写出元素Y在周期表中的位置 ;
③Z、W两元素相比较,金属性较强的元素是 (填元素符号),可以验证该结论的实验是 。
(a)比较两种元素单质的熔点
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)比较这两种元素的最高价氧化物对应水化物的碱性
(d)比较这两种元素的气态氢化物的稳定性
图表法是常用的科学研究方法,下表列出了同周期的四种短周期元素的部分性质(“电负性”即元素对应原子吸引电子能力的标度):
| 元素编号 |
A |
B |
C |
D |
E |
| 电负性 |
3.0 |
2.5 |
X[ |
1.5 |
0.9 |
| 原子半径(单位nm) |
0.099 |
0.102 |
0.110 |
0.143 |
0.186 |
| 主要化合价 |
-1,+7 |
-2,+6 |
-3,+5 |
+3 |
+1 |
请回答下列问题:
(1)写出E元素的离子结构示意图 ;
(2)X的值应为 (填字母);
A.3.6 B.3.1 C.2.1 D.1.4
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系 ;
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是: (用化学式表示)
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:
(6)D、E最高价氧化物对应水化物相互反应的离子方程式:
(14 分)碳及其化合物应用广泛。
I.工业上利用CO和水在沸石分子筛表面反应制氢气,CO(g)+H2O(g)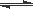 CO2(g)+H2(g)
CO2(g)+H2(g)
(1)向 1L恒容密闭容器中注入CO和H2O(g),830oC时,测得部分数据如下表。
| t/min |
0 |
1 |
2 |
3 |
4 |
5 |
| n(CO)/mol |
0.200 |
0.160 |
0.125 |
0.099 |
0.080 |
0.080 |
| n(H2O)/mol |
0.300 |
0.260 |
0.225 |
0.199 |
0.180 |
0.180 |
则该温度下反应的平衡常数K=
(2)相同条件下,向 1L恒容密闭容器中,同时注入1molCO、1molH2O(g)、2molCO2和2molH2,此时
v(正) v(逆)(填“>”“=”或“<”)
II.已知:CO(g)+1/2O2(g)=CO2(g) △H1=-141kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H2=-484kJ·mol-1
CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-726kJ·mol-1
(3)利用CO、H2化合制得液态甲醇的热化学方程式为
Ⅲ.一种新型氢氧燃料电池工作原理如下图所示。
(4)写出电极A的电极反应式 ,放电过程中,溶液中的CO32-将移向电极 (填A或B)
(5)以上述电池电解饱和食盐水,若生成0.2mol Cl2,则至少需通入O2的体积为 L(标准状况)
(1)1mol/L的①盐酸、②醋酸、③硫酸各1L,分别加入足量的铁。开始反应时产生氢气的速率__________,最终收集到的氢气的物质的量_______;若氢离子浓度相同的①盐酸、②醋酸、③硫酸各1L,分别加入足量的铁,开始反应时产生氢气的速率________,最终收集到的氢气的物质的量____________(填序号)。
(2)如果在稀氨水中进行下列操作,则下列指定微粒浓度如何变化?试用“增大”“减小”“不变”填写。
①通适量HCl气体时,c(NH3) ,c(H+) 。
②加入少量NaOH固体时,c(NH ) ,c(OH-) 。
) ,c(OH-) 。
(3)某温度下纯水中c(H+) = 2×10-7 mol/L,则c(OH-) = ,若温度不变,滴入稀盐酸使c(H+) = 5×10-6 mol/L,则此时溶液中的c(OH-) = 。
(4)用物质的量浓度为0.04mol/L的氢氧化钠溶液去中和H+浓度为10-3mol/L的某一元弱酸溶液20mL,消耗氢氧化钠溶液12.5mL,则此一元弱酸物质的量浓度为 ;电离度为 。
已知合成氨的热化学方程式为:N2(g)+3H2(g) 2NH3(g)ΔH= -92.2KJ·mol-1,下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
2NH3(g)ΔH= -92.2KJ·mol-1,下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
根据表中数据计算:
(1)反应进行到2小时时放出的热量为 KJ。
(2)1小时内N2的平均反应速率为
(3)此条件下该反应的化学平衡常数K= (保留两位小数)。
(4)反应达到平衡后,若往平衡体系中再加入1.50mol N2、4.50mol H2,化学平衡向 方向移动(填“正反应”或“逆反应”或“不移动”),达新平衡时,H2物质的量与原平衡相比 ,NH3的体积分数与原平衡相比 (填“增大”或“减小”或“不变”)。
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注
(1)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
①反应开始到平衡,H2的平均反应速率v(H2)=_________________mol/(L·min),
②H2的转化率为 ____________。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
| A.升高温度 |
| B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 |
| D.再充入1mol CO2和3mol H2 |
E、使用催化剂
F、缩小容器体积
(2)①反应进行到3 min时,同种物质的v正 与v逆的关系: v正 v逆 (填>,=,<)
②上述反应平衡常数的表达式为 ,经计算该温度下此反应平衡常数的数值为 。
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题: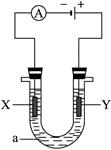
(1)若X、Y者是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中化学反应方程式为_____________,在X极附近观察到的现象是_________________。
②检验Y电极上反应产物的方法是_________________________。
③当导线中有0.1 mol的电子通过时,在标况下理论上两极可收集的气体的体积是__ __L。
(2)下图装置中,
①当A键断开,B、C闭合时,乙为 池;
②当A、C两键断开, B闭合时,乙中铁极增重1.6g,则被氧化的铁有 g;
③将乙中两极都换成石墨,硫酸铜溶液换H2SO4后断开B、C两键, 闭合A键,则乙为 池,当甲中锌极减轻6.5g时,乙中共放出气体 mL(标况)。
已知X、Y、Z、W、H五种元素原子序数依次增大,分布在元素周期表中的三个不同短周期。X、W同主族,Y、Z是同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。Z的阴离子与H的阳离子具有相同的电子层结构,H的单质能溶于W最高价氧化物的水化物溶液中。试推断:
(1)X、Y两种元素的名称:X 、Y ;
(2)H在元素周期表中的位置: ;
(3)由X、Y、Z所形成的属于强电解质的共价化合物M的化学式是 ,以金属铜和H的单质作电极,M的浓溶液为电解质溶液构成的原电池中,正极反应式 ,电池总反应的离子方程式 。
现有纯锌片、纯铜片和500 mL 0.1 mol·L-1的硫酸、导线、1 000 mL量筒。用如下图所示装置利用原电池原理,制备一定量的氢气。
(1)如上图所示,装置气密性良好,且1 000 mL量筒中已充满水,刚开始实验时,根据构成原电池必须满足的条件,首先要进行的操作是 ;
(2)a的电极材料为 ,作原电池的 极;电子经外电路由
(①a→b ②b→a 填序号,下同)
(3)b极上发生的电极反应为_________,反应时a极附近SO42-浓度 (填“逐渐增大”、“逐渐减小”或“始终不变”);
(4)假设反应过程中溶液体积不变,当硫酸浓度降低一半时,通过导线的电子的物质的量为 ,量筒中收集的气体体积最接近 mL
| A.400 | B.500 | C.600 | D.700 |
双酚A奶瓶(见下图)对幼儿健康可能造成危害的报道再次见诸各类媒体。
双酚A,也称BPA,是制造聚碳酸酯(PC)塑料的一种化学物质,广泛用于水瓶、食品容器和奶瓶的制造。化合物L是一种能使人及动物的内分泌系统发生紊乱,导致生育及繁殖异常的环境激素,它在一定条件下水解可生成双酚A和有机酸M。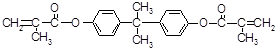 (化合物L)
(化合物L)
(1)1mol化合物L最多可以与 mol H2反应。
(2)双酚A的分子式为 ;其含有的官能团的电子式为
(3)下列关于双酚A的叙述中正确的是 (不定项选择)
A.与苯酚互为同系物
B.可以和Na2CO3溶液反应,放出CO2气体
C.该化合物与三氯化铁溶液会发生显色反应
D.分子中最多有8个碳原子在同一平面上
E.1mol双酚A与溴水反应时,最多可消耗Br2 4mol
(4)有机酸M与甲醇反应后得到的酯,能聚合生成一种生活中常见的高分子化合物,可用于制造高级光学仪器透镜,请写出该酯在一定条件下生成此高分子化合物的化学反应方程式: ,该反应的类型是 反应
(5)双酚A的另一重要用途是和光气(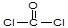 )合成Lexan聚碳酸酯(一种高强材料,可用于制作防弹窗户)。写出此合成反应的化学方程式:_______________________
)合成Lexan聚碳酸酯(一种高强材料,可用于制作防弹窗户)。写出此合成反应的化学方程式:_______________________
原子序数由小到大排列的四种短周期元素X、Y、Z、W四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)用电子式表示X与W组成的化合物的形成过程 。
(2)由X和Z组成的某化合物,常用于杀菌消毒,则该化合物的结构式为 。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液不能与铜反应、浓溶液能与铜反应,该反应的化学方程式为 。
(4)由X、Y、Z、W四种元素构成化合物A 。
①已知l mol A能与足量NaOH浓溶液反应生成标准状况下44.8 L气体。写出加热条件下A与NaOH溶液反应的离子方程式 。
②又知A既能与盐酸反应,又能与氯气反应,写出A与氯水反应的离子方程式: 。
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1mol B中含有6mol结晶水,对化合物物B进行如下实验:
取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解则B的化学式为 。
试题篮
()