草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:
称取Wg草酸晶体,配成100.00mL水溶液
(1)称25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定到KMnO4不再褪色为止,所发生的反应
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
试回答:(1)实验中不需要的仪器有(填序号)___________,还缺少的仪器有(填名称)___________________________________________________________________________。
a.托盘天平(带砝码,镊子)b.滴定管 c.100mL量筒 d.100mL容量瓶 e.烧杯
f.漏斗 g.锥形瓶 h.玻璃棒球 i.药匙 j.烧瓶
(2)实验中,标准液KMnO4溶液应装在_____________________式滴定管中,因为______________________________________________________________________。
(3)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,
则所测得的x值会__________________________(偏大、偏小、无影响)
(4)在滴定过程中若用amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的
量浓度为________________________mol·L-1,由此可计算x的值是____________。
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr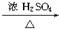 C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。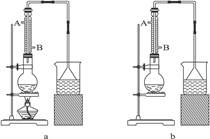
(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是 ( )
A.A进B出 B.B进A出 C.从A进或B进均可
(4)可能发生的副反应为:_______________、________________、________________
(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是________________。
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用一个月才充电一次.假定放电过程中,甲醇完全氧化产生二氧化碳被充分吸收生成CO32-.
(1)该电池反应的离子方程式为
(2)甲醇在 极发生反应(填“正”或“负”),电池中放电过程中溶液pH将 (填“下降”、“上升”或“不变”);若有16克甲醇蒸汽被完全氧化产生电能,并利用该过程中释放的电能电解足量的硫酸铜溶液假设能量利用率为80%。则将产生标准状况下氧气 L。
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一个电极通入汽油蒸汽。其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-离子(其中氧化反应发生完全)。以丁烷代表汽油。该电池的正极反应式为 ;
(4)放电时固体电解质里的O2-离子的移动方向是向 极移动(填“正”或“负”)。
Al-Mg在不同的电解质溶液中分别构成原电池A、B。如下图所示: 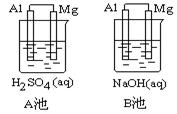
指出各池中的负极材料并写出其电极方程式。
①负极材料:
A池 ,B池 。
②电极反应式:
A池:正极 ,负极 。
B池:正极 ,负极 。
③从构成原电池的几个组成部分来看,判断原电池的负极,除了要考虑金属的活泼性外,还要考虑
请你选用下图所示仪器和药品,按实验室要求,设计一套完整的检验一氧化碳还原性和二氧化碳化学性质的实验,并回答下列问题: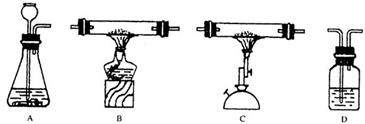
实验药品:盐酸、石灰石、氧化铜粉末、木炭粉、氢氧化钙溶液。
(1)实验装置连接顺序依次为(用字母表示)___________;
(2)A装置的药品是_________,发生反应的化学方程式为_______________________;
(3)B装置中产生的实验现象是_________,发生反应的化学方程式为____________
(4)C装置中发生反应的化学方程式为____________________________________;
(5)D装置中产生的现象是_________;
(6)尾气中含有毒气体,排放到空气中会造成污染,处理方法是_________。

提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为_________(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_________。
(2)用提纯的NaCl配制500 mL4.00 mol·L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有________(填仪器名称)。
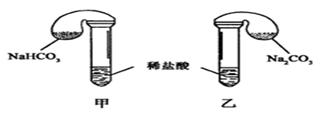
请回答:
(1)各组反应开始时, 装置中的气球体积先变大,该装置中反应的离子方程式是______。
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格。
| 组 数 |
试剂用量 |
实验现象 (气球体积变化) |
分析原因 |
| ① |
0.42 g NaHCO3;0.53g Na2CO3;3mL4 mol·L-1盐酸 |
甲中气球与乙中气球的体积相等 |
甲、乙盐酸均过量,n(NaHCO3)=n(Na2CO3),ν甲(CO2)=ν乙(CO2) |
| ② |
0.3 g NaHCO3;0.3 g Na2CO3;3mL4 mol·L-1盐酸 |
甲中气球比乙中气球的体积大 |
|
| ③ |
0.6 g NaHCO3;0.6 g Na2CO3;3mL 2mol·L-1盐酸 |
甲中气球比乙中气球的体积大 |
|
| 片刻后,乙中气球又缩小,甲中气球的体积基本不变 |
(用离子方程式表示) |
某学生课外活动小组利用右图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是 溶液;加热时溶液由红色逐渐变浅的原因是 。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是 溶液;加热时溶液由无色变为红色的原因是 。
Ⅰ.化学实验室制取氯化氢气体的方法之一是将浓硫酸滴入浓盐酸中。请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图中标明所用试剂。(仪器可重复使用,固定装置不必画出)。

Ⅱ.实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%-30%的稀硫酸溶液,在50℃-80℃水浴中加热至不再产生气泡。将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置、冷却一段时间后收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式:。
(2)硫酸溶液过稀会导致。
(3)采用水浴加热的原因是。
(4)反应时铁屑过量的目的是(用离子方程式表示)。
(5)溶液趁热过滤的原因是塞紧试管口的目的是
(6)静置冷却一段时间后,在试管中观察到的现象是。
50 mL 0.050 mol/L 盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中
进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:

⑴从实验装置上看,图中尚缺少的一种玻璃仪器是 。
⑵大小烧杯间填满碎纸条的作用是 。
⑶大烧杯上如不盖硬纸板,求得的中和热数值将 (填“偏大”、“偏小”、或“无影响”)。结合日常生活的实际该实验该在 中进行效果更好。
⑷实验中改用60 mL 0.050 mol/L 盐酸与50 mL 0.55 mol/L NaOH溶液进行反应与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”),简述理由 。
⑸用相同浓度、相同体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
(填“偏大”、“偏小”、或“无影响”);用50 mL 0.50 mol/L NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、或“无影响”)。
浓氨水可与新制生石灰作用生成氨气,干燥的氨气在高温下能被CuO氧化成N2实验室欲用图仪器装置和药品来制取纯净的氮气。
试回答下列问题:
(1)这些装置按气流方向自左向右的连接顺序是(填A、B、C……)____ ____。
(2)E中发生反应的化学方程式是____ ____。
(3)装置④中应当选用的干燥剂是(写名称)____ _______。
(4)装置①中发生氧化还原反应的化学方程式是___ ________。其中氧化剂是____ __,氧化产物是______ __(写化学式)。
(5)装置②中浓硫酸的作用是_____ ____。
由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、C1—、SO42—、CO32-。将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
| 实验序号 |
实验内容 |
实验结果 |
| 1 |
加AgNO3溶液 |
有白色沉淀生成 |
| 2 |
加足量NaOH溶液并加热 |
收集到气体1.12L(已折算成标准 状况下的体积) |
| 3 |
加足量BaC12溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6. 27g,第二次 称量读数为2.33g |
试回答下列问题:
(1)根据实验1对C1—是否存在的判断是 (填“一定存在”、“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
| 阴离子符号 |
物质的量浓度(mol·L—1) |
| |
|
| |
|
(3)试确定K+是否存在? ,判断的理由是
某兴趣小组同学共同设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质。请回答下列问题:

(1)利用装置I制取某些气体,制取气体的反应所具有的特点是___________________。
(2)利用装置Ⅰ、II制取气体(K2关闭,K1打开)。甲同学认为:利用装置Ⅱ可以收集H2、NH3等气体,但不能收集O2和NO,理由是
。
乙同学认为:利用装置II作简易改进(不改变仪器装置),可收集NO、O2,改进的方法是__________________ 。
丙学认为:利用装置II作简易改进(改变仪器装置),可收集NO2气体,改进的方法是_______________________ 。
(3)利用装置I、Ⅲ 验证物质的性质(K2打开,K1关闭)。如设计实验证明氧化性:KMnO4>Cl2>Br2,则在A中加浓盐酸,B中加________ __,C中加______________ ,观察到C中的现象是___________________ 。
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用 (选填序号)。
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(2)B装置的作用 ;E装置的作用 。
(3)通入C装置的两根导管左边较长、右边较短,目的是 。
(4)装置F中发生反应的化学方程式是 。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式: 。
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?
。
试题篮
()