(每空1分,共12分)
(1)某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
①写出A中有机反应的化学方程式_______________________________________
②已知上述有机反应是放热反应。观察到A中的现象是_________________及__________________。
③实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_______________________________________________,写出有关的化学方程式____________________________________________。
④C中盛放CCl4的作用是______________________________________。
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入A gNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入__________________,现象是___________________________________________。
gNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入__________________,现象是___________________________________________。
(2)乙炔的实验室制法
①反应原理______________________________________。
②选择合适的制取实验装置_______。
③实验中常用饱和食盐水代替水,目的是____________________________________。
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味。可以用________________溶液除去杂质气体。
某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式:________________________________________________;
(2)观察到A中的现象是______________________________;
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
______________________________,写出有关的化学方程式__ ________________;
________________;
(4)C中盛放CCl4的作用是________________________________________;
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入______________________________,现象是______________________________。
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯如不盖硬纸板,测得的中和热数值 (填“偏大 ”、“偏小”或“无影响”)
”、“偏小”或“无影响”)
(4)实验中改用60mL 0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热  (填“相等”或“不相等”),简述理由 。
(填“相等”或“不相等”),简述理由 。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会 (填“偏大”、“偏小”或“无影响”);用50mL 0.50mol/L NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”或“无影响”)。
下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。


(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为_________(填代号)。能验证CO氧化产物的现象是____________。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应_________,活塞b应_________,需要加热的仪器装置有_________(填代号),m中反应的化学方程式为____________。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有:____________ 。
。
②实验中观察到E内有红棕色气体出现,证明氨气具有_________性。
某中:学研究性学习小组为探究碳酸锄和碳酸氢钠两种物质的性质、制法和用途,进行了如下实验:
(1)若刚实验IV来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是 ,能说明碳酸钠比碳酸氢钠稳定的实验现象是 。
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,不能达到实验目的的是(填装置序号) 。其中能够说明泡沫灭火器中选择碳酸氢钠与酸反应制CO2而不选择碳酸钠的实验是____。
(3)若测定Na2CO3固体中混有的少量NaHCO3的质量分数,采用实验III能否达到实验目的?若能,请说明其计算所需的数据 ;若不能,请简要说明理由 。
实验二、将碳酸氢钠溶液与澄清石灰混合并充分反应。
(4)当碳酸氢钠过量时,反应的离子方程式为 。
(5)当碳 酸氢钠与氢氧化钙物质的量比之为1:1时,所得溶液中溶质的化学式为 。
酸氢钠与氢氧化钙物质的量比之为1:1时,所得溶液中溶质的化学式为 。
 实验
实验 室用下图装置制取少量溴苯,填写下列空白
室用下图装置制取少量溴苯,填写下列空白
(1).写出仪器A的名称 ;B的名称 ; (2).请你写出实验室制取溴苯的化学方程式 ;
(2).请你写出实验室制取溴苯的化学方程式 ;
(3).长导管的下口为什么不插入锥形瓶的液面下
(4).反应完后,向烧瓶中加NaOH  溶液的作用是:
溶液的作用是:
(5).冷凝水的进水口是(填m或n) ,
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入 ,目的是 。
(2)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是 。
(3)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物。下列框图是分离操作步骤流程图:
则试剂a是:____________,分离方法I是____________,试剂b是______________,分离方法III是____________。
(4)甲、乙两位同学欲将所得含有乙醇、乙酯和水的乙酸乙酯粗产品提纯,在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙 两人实验结果如下:甲得到了显
两人实验结果如下:甲得到了显 酸性的酯的混合物;乙得到了大量水溶性的物质;丙同学分析了上述实验目标产物后认为上述实验没有成功。试分析下列问题:
酸性的酯的混合物;乙得到了大量水溶性的物质;丙同学分析了上述实验目标产物后认为上述实验没有成功。试分析下列问题:
①甲实验失败的原因__________________________________________________________
②乙实验失败的原因是_________________________________________________________
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:(14分)
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水溶解、搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是___________________ ________________。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是___________________________ ____。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C 中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
依据实验过程回答下列问题:
( 3)、检查B装置的气密性操作是
3)、检查B装置的气密性操作是
(4)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有的作用是:____________________________ _____。
(5)下列各项措施中,不能提高测定准确度的是_____________(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A—B之间增添盛有浓硫酸的洗气装置
d.在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为________ _。
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是____________________  _____。
_____。
(17分) 某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如右图装置。倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入量气管气体的体积为VmL(已折算成标准状况)
由上述实验事实可知:
(1)①固体M中一定有的物质是______________(填化学式);
②其中一种物质的质量可以确定为___________g(用代数式表示)。
(2)B装置的名称是_______。写出B装置中反应的离子方程式__________________。
(3)C装置的作用是_________________________,如果实验中没有B装置,则C装置中产生的现象是_________________________________________________。
(4)稀硫酸和固体M反应后溶液中还残留淡黄色固体,该固体是_____________,要分离出该固体,在实验操作中,除烧杯外还需要用到的玻璃仪器是_________。
(5)通过进一步实验,测得固体M中各种成分的质量之和小于反应前铁粉和硫粉的质量之和,产生这种现象的原因可能是_____________
A M中有未反应的铁和硫
B 测定气体体积时水准管的水面高于量气管的水面
C A中留有反应生成的气体
D 气体进入D装置前未用浓硫酸干燥
用18.4mol/L的浓硫酸配制100mL浓度为1mol/L的稀硫酸。
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、 、 。
(2)其操作步骤可分解为以下几步:
A.用量筒量 取 mL浓硫酸
取 mL浓硫酸 ,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌
,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌
B.用约30mL蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都倒入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里
D.检查100mL容量瓶,是否漏水
E.将蒸馏水直接加入容量瓶,至液面接近刻度线
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切
请据此填写:
①完成上述步骤中的空白处。
②正确的操作顺序是(用字母填写):
( )→( )→( )→( )→( )→( )→( )。
③进行A步操作后,选用量筒的规格是
A.10mL B.50mL C.100mL D.1000mL
④如果对装有浓硫酸的量筒仰视读数,配制的稀硫酸浓度将 (填“偏高” 、“偏低”、“无影响”)
、“偏低”、“无影响”)
⑤进行A步骤操作时,必须 后,才能进行后面的操作。
已知HI是一种无色,有刺激性气味,极易溶于水的气体,HI的水溶液称之为氢碘酸,是一种强酸。
(1)请写出I元素在周期表的位置:第五周期 族
(2)将 HI气体通入一定量的浓硫酸中,产生的混合气体除含HI、少量的I2蒸气和水蒸气外,还可能有 气体。
HI气体通入一定量的浓硫酸中,产生的混合气体除含HI、少量的I2蒸气和水蒸气外,还可能有 气体。
(3) 小明拟对HI通入浓硫酸后的混合气体成分进行验证和探究。他设计了如下实验装置图
初步探究设计:
①其中直形玻璃管中所装的药品是 (写名称)
②足量四氯化碳的两个作用是: 。
进一步探究:
查阅资料:氧化性强弱KMnO4>HNO3>I2>SO42-,且较稀的硝酸不能氧化I2。
③小明拟对溶在水层的其它混合气体成分做进一步探究。请你从以下限选试剂中选择合适的试剂帮小明完成实验报告。
限选的试剂:石蕊试剂、品红溶液、酸性KMnO4溶液、0.1mol/L HNO3、淀粉溶液、BaCl2溶液
| 实验方案 |
可能的现象和相应的结论 |
| 取少量烧杯中的上层溶液分装入A、B两支试管中 |
|
| |
|
| |
|
常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是:
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法:
(3)经检验上 述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(结合化学方程式说明):
述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(结合化学方程式说明):
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是:
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如下图所
示的装置:
请简述实验操作及原理:
(12分)根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算 。为此,提供的实验仪器及试剂如下(根据需要
。为此,提供的实验仪器及试剂如下(根据需要 可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)=" a" g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
① CuO未完全起反应 ② CuO不干燥
③ CuO中混有不反应的杂质 ④碱石灰不干燥
⑤ NH4C1与Ca(OH)2混合物不干燥
NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或_______________和_______________达到实验目的。
用50m L0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
L0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: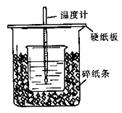
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”)
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
试题篮
()