某化学课外活动小组的同学为了测定某氮化镁样品中Mg3N2的质量分数,他们取氮化镁样品5.0g于烧杯中,加入100g某浓度的盐酸(足量),充分反应后(杂质不溶于水也不与盐酸反应),测得剩余固体的质量为1.0g。请计算:
(1)已知:Mg3N2与盐酸反应的生成物只有氯化镁和氯化铵,则在配平的该化学反应方程式中,HCl前面的化学计量数为 。
(2)氮化镁样品中Mg3N2的质量分数。(写出计算过程)
(3)此时所得溶液中氯化镁的质量分数。(写出计算过程)
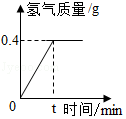
小英同学用某铁合金样品做了如下实验:称量11.4g样品,放入质量为40g的烧杯中,再往烧杯中加入200g稀硫酸,恰好完全反应(杂质不与酸反应,也不溶于水)。反应完毕后称量,烧杯及烧杯内物质总质量为251g。求:
(1)反应产生的氢气质量为 g;
(2)所用稀硫酸的溶质质量分数(写出计算过程)。
我国早在西汉时期,就有“曾青得铁则化为铜”的记载,即把铁片放入硫酸铜溶液中可以置换出铜。11.2g铁与足量的硫酸铜溶液反应,理论上可得到铜的质量是多少?
小兰进行水的电解实验时,在水中加入少许硫酸钠以增强导电性。她将2.7g硫酸钠固体加入52.7g水中充分溶解,倒入电解器中通电,当正极产生4.8g氧气时结束实验。忽略气体在水中的溶解,请计算(写出计算过程):
(1)负极产生氢气的质量;
(2)实验结束时所得溶液的溶质质量分数。
氧化钴(CoO)溶于盐酸可得到粉红色的氯化钴(CoCl 2)溶液。CoCl 2含结晶水数目不同而呈现不同颜色。利用蓝色的无水CoCl 2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的六水氯化钴晶体(CoCl 2•6H 2O)受热分解时,剩余固体质量随温度变化的曲线。
已知:①CoCl 2•6H 2O的相对分子质量为CoCl 2和6个结晶水的相对分子质量之和。

②CoCl 2•6H 2O受热分解完全脱水的化学方程式为:CoCl 2•6H 2O  CoCl 2+6H 2O。
CoCl 2+6H 2O。
请回答:
(1)CoCl 2的钴元素的化合价为 价。
(2)求物质A(CoCl 2•xH 2O)中的x值。
某研究性学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品5g,把 60g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质 不溶于水,也不与稀盐酸反应)。根据实验数据计算:
|
实验次数 |
1 |
2 |
3 |
4 |
|
加入稀盐酸的质量/g |
15 |
15 |
15 |
15 |
|
剩余固体的质量/g |
3.50 |
2.00 |
0.75 |
0.75 |
(1)石灰石样品中碳酸钙的质量分数为 。
(2)求原 60g 稀盐酸中溶质质量分数(要求书写计算过程)。
工业上常用熟石灰(主要成份:Ca(OH) 2)和纯碱(主要成份:Na 2CO 3)混合加工制取烧碱(化学式:NaOH)。请问:工业上制取40吨烧碱,需要消耗含Na 2CO 3质量分数为90%的纯碱多少吨?(计算结果保留一位小数)
为探究铁的化学性质,某学习小组做了如图甲所示实验。他们观察到试管a中铁粉全部溶解,产生大量气泡,溶液呈① 色,反应的化学方程式为② ;试管b中有③ 色固体生成,该反应的化学方程式为④ 。为进一步确定试管a所得溶液中的溶质成分和试管b所得固体的组成,他们进行了以下实验探究。
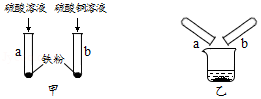
【提出猜想】(1)试管a中的溶质成分:猜想一:FeSO 4;猜想二:⑤ 。
(2)试管b中固体的组成:猜想三:Cu; 猜想四:Fe和Cu。
【实验探究】甲图所示实验结束后,将试管a、试管b内的物质全部倒入同一烧杯中(如乙图所示),他们惊奇地发现烧杯内溶液中产生大量气泡。
【总结交流】经过讨论,大家一致认为上述猜想中正确的是⑥ 。
【拓展探究】某混合溶液由硫酸铜和硫酸溶液组成。上述小组同学取192.4g该混合溶液于烧杯中,然后往其中加入33.6g铁粉,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
(3)原混合溶液中H 2SO 4的质量。(计算结果保留一位小数)
(4)原混合溶液中CuSO 4和H 2SO 4的质量比。
(5)完全反应后所得溶液中溶质的质量分数。(计算结果保留一位小数)
现有一瓶敞口放置在空气中的NaOH固体,欲知其组成成分,取样品9.3克向其中逐渐加入一定质量分数的稀盐酸,产生气体的质量与加入稀盐酸质量关系如图所示,试回答;
(1)产生二氧化碳气体的质量为 克。
(2)所用稀盐酸溶质质量分数。
(3)求样品中氢氧化钠的质量分数。(精确到0.1%)

高铁酸钠(Na 2FeO 4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO+2Fe(NO 3) 3+10NaOH=2Na 2FeO 4↓+3NaCl+6NaNO 3+5H 2O
(1)次氯酸钠(NaClO) 中Cl元素的化合价为 ;
(2)高铁酸钠(Na 2FeO 4)中铁元素和氧元素的质量比为 (填最简比);
(3)现要制得830kg含杂质20%的高铁酸钠,至少需要次氯酸钠的质量是多少?(列式计算)
某课外兴趣小组为了测定当地石灰石中CaCO 3的质量分数,取25g石灰石样品,粉碎后,将100g一定质量分数的稀盐酸分5次加入到该样品中,所测数据如下表所示(杂质不与稀盐酸反应,也不溶于水):
|
次数 |
一 |
二 |
三 |
四 |
五 |
|
加入稀盐酸的质量/g |
20 |
20 |
20 |
20 |
20 |
|
产生气体的质量/g |
2.2 |
4.4 |
6.6 |
8.8 |
8.8 |
(1)生成CO 2的质量为 g;
(2)第 次恰好完全反应;
(3)求石灰石样品中CaCO 3的质量分数。
氯化钠是一种重要的化工原料。电解氯化钠溶液可制得氯气、氢氧化钠和氢气,反应的化学方程式为2NaCl+2H 2O  Cl 2↑+H 2↑+2NaOH.现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,得到85.4g溶液,生成氢气的质量与时间的关系如图所示。请计算:
Cl 2↑+H 2↑+2NaOH.现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,得到85.4g溶液,生成氢气的质量与时间的关系如图所示。请计算:
(1)氯化钠完全反应时,生成氢气的质量是 g。
(2)氯化钠完全反应时,生成氢氧化钠的质量是 g。
(3)原氯化钠溶液中溶质的质量分数是多少?
用某含有CO 2、水蒸气的还原性气体(可能含有CO、H 2中的一种或两种)经过如图的装置来确定其成分及C装置中Fe xO y的化学式。
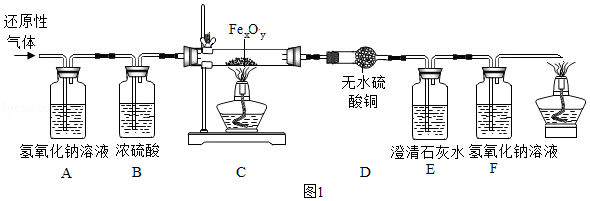
(1)B装置的作用是 ,D装置的作用 。
(2)实验过程中观察到D中无明显变化,若澄清石灰水变浑浊,则还原性气体是 ,当C中的Fe xO y完全反应后,测得E和F的总质量增加3.52g,C中剩余固体质量为3.36g,则Fe xO y的化学式为 ,若没有A装置,则测得的x和y的比值将 (填"偏大"、"偏小"或"不变")。
上述实验中生成的二氧化碳用氢氧化钠溶液吸收,某工厂也利用此原理吸收生产中排放的二氧化碳,再通过一定的方法将二氧碳释放、储存达到回收再利用的目的,具体流程如图1(部分反应条件和试剂未标出)
根据图2回答下列问题
(3)分离池中发生的化学反应方程式为 。
(4)B为 (填化学式)
(5)"人类只一个地球!"防止温室效应的根本对策是全球参与控制二氧化碳的排放量","低碳生活从我做起"。请举出一例"低碳"生活的例子 (合理即可)。 
某石灰水中含有氢氧化钙0.74g,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是多少?
试题篮
()