为了测定某石灰石样品中碳酸钙的质量分数,某兴趣小组的同学进行了如下实验:取12.5g 石灰石样品,放入盛有100g稀盐酸的烧杯中,石灰石中的碳酸钙与盐酸恰好完全反应(假设石灰石中的杂质不与盐酸反应也不溶于水),烧杯内物质质量变为108.1g。
求:(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 g.
(2)求该石灰石中碳酸钙的质量分数?
(3)将反应后的混合物过滤,求所得滤液的溶质质量分数?(计算结果保留一位小数)
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应)。课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
请计算:
(1)石灰石样品中杂质的质量为 g。
(2)所加盐酸的溶质质量分数。
世界上每年因锈蚀而报废的金属设备和材料,高达产量的20%~40%,某实验小组对铁的燃烧和锈蚀进行如下探究。
探究一:铁丝燃烧
如图1所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴杆,点燃火柴杆待快燃尽时,分别插入充满氧气的集气瓶中。观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比Ⅰ中的更剧烈;Ⅲ中铁丝没有燃烧。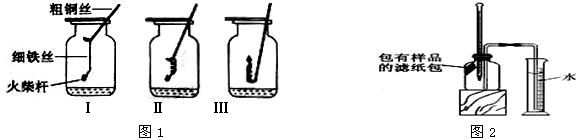
(1)集气瓶中加入少量水的作用: 。
(2)为什么Ⅲ中铁丝不能燃烧 。
(3)分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因 。
探究二:铁粉腐蚀的条件
如图2所示,将所有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进入广口瓶(容积为146 mL)。当温度恢复至室温,量筒内水面高度不变时读数(此时广口瓶内氧气含量几乎为零),记录量筒的起始和最终读数以及所需时间如下表:
| 序号 |
样 品 |
量筒起始读数/ mL |
量筒最终读数/ mL |
所需时间/ min |
| ① |
1.0g铁粉、0.2g碳和10滴水 |
100 |
72 |
约120 |
| ② |
1.0g铁粉、0.2g碳和10滴水和少量NaCl |
100 |
72 |
约70 |
| ③ |
|
|
|
|
(4)实验①和②说明NaCl可以 (填“加快”或“减慢”)铁锈蚀的过程。
(5)实验开始后,广口瓶温度上升,说明铁锈蚀是 (填“放热”或“吸热”)过程。
(6)实验①和③是探究碳对铁锈蚀速率的影响,实验③表格空白处样品的组成是 。
(7)该装置还可能用于测量空气中氧气的含量,根据上述数据计算得出空气中氧气的体积分数约是 %(精确到小数点后1位),试分析该实验结果出现误差的原因 。
(本题7分)某校化学兴趣小组经查阅资料得知:铝是重要的轻金属,广泛应用于航空、电讯和建筑等领域。铝也有其特殊的性质:①铝的熔点是660℃,氧化铝的熔点高达2054℃。②铝虽比锌活泼,但是将铝和锌分别投入稀硫酸中,铝比锌反应慢得多。③尽管铝表面致密的氧化膜能使铝与其周围的介质(空气、水)隔绝,但“奇怪”的是铝制容器仍不能用来盛放和腌制咸菜。为此该小组进行了“铝表面氧化膜”的探究实验,其过程如下,请完成填空:
【实验1】用坩埚钳夹住一块擦去氧化膜的铝片,放在酒精灯火焰上灼烧,铝片表面接触火焰的部分变暗片刻后变软;轻轻摇动,会左右摇晃,却不像蜡烛那样滴落。
问题:
(1)请写出在空气中灼烧铝片的化学方程式 ;
(2)铝片接触火焰的部分不像蜡烛那样滴落的原因是 。
【实验2】取2条未用砂纸打磨过的铝片,一片浸入CuCl2稀溶液中,其表面很快析出较多红色粉末状固体;而另一片浸入CuSO4稀溶液中现象一直不明显。
问题:试猜测产生这种现象差异的因素是
【实验3】用砂纸打磨一铝片使其表面较粗糙,再将其放入CuSO4稀溶液中,直到2-3分钟后,铝片表面才有少量红色固体附着。
问题:试写出铝片表面附着红色固体的化学方程式: ;
【实验4】向实验2的CuSO4稀溶液中滴入3-5滴NaCl稀溶液,铝片表面逐渐有红色固体析出。
【实验5】向实验2的CuSO4稀溶液中滴入3-5滴Na2SO4稀溶液,铝片表面现象一直不明显。
问题:根据实验2、3、4、5的现象可以得出的结论是 。
下列区分物质的方法不正确的是
| A.硬水和软水——加肥皂水,观察泡沫的多少 |
| B.碳酸氢钠溶液、碳酸钠溶液--加入稀盐酸,观察是否有气泡 |
| C.氧气、二氧化碳--插入带火星的木条,观察木条能否复燃 |
| D.涤纶、羊毛纤维--点燃,闻是否有烧焦羽毛的气味 |
为测定某石灰石样品中碳酸钙的含量,取10g石灰石样品,研碎加入烧杯中,将80g稀 盐酸分四次加入烧杯中。每次加入稀盐酸,充分反应后测定反应生成气体的总质量(与前面实验中产生的气体累加),数据记录如下表:(杂质不参加反应,不含钙元素.第二问要求作答)
| 序号 |
1 |
2 |
3 |
4 |
| 加入稀盐酸的质量(g) |
20 |
20 |
20 |
20 |
| 充分反应产生气体的总质量(g) |
1.1 |
n |
3.3 |
3.3 |
| 实验的次数 |
第1次 |
第2次 |
第3次 |
第4次 |
| 所加盐酸的质量/g |
20 |
20 |
20 |
20 |
| 产生气体的质量/g |
1.1 |
n |
3.3 |
3.3 |
(1)表中n的值为 。
(2)计算石灰石样品中碳酸钙的质量分数。
(3)第4次加入稀盐酸后,烧杯中钙元素的质量为 g
碳及许多含碳化合物不充分燃烧都要产生一氧化碳,一氧化碳是一种污染空气的有毒气体,它会使人中毒,通常采用燃烧法处理尾气中的一氧化碳。某同学对一氧化碳与一定量的氧气反应后所得的气体成分进行了如下实验探究:
【提出猜想】反应后气体的组成可能是:①CO和CO2;②只有CO2;③ 。
【实验探究】该同学为了验证自己的猜想,用下列装置进行实验:
①装置B中氢氧化钠溶液的作用是 ;
②装置A中出现的现象是 ;
发生反应的化学方程式是 ;用带火星的木条伸入D中出现的现象是 。
【实验结论】通过实验验证,猜想③成立。
某钙片的标签如下,且知钙片成分中只有碳酸钙中含有钙元素:

(1)请计算碳酸钙中钙元素的质量分数为 ;
(2)请通过计算推断此标签中的含钙量是 (填虚假或真实)的;
(3)某实验小组为测定其真实的含钙量做了如下实验,每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生的化学反应是:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑,充分反应后再称取烧杯和剩余物质的总质量,数据如下:
| |
物质的质量 |
| 反应前:烧杯+盐酸 |
22g |
| 10片钙片 |
8g |
| 反应后:烧杯+剩余物 |
26.7g |
请计算此钙片中碳酸钙的质量分数。
溶液是生产生活中常见的物质,依据相关信息回答问题:
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
| 温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
| 溶解度/g |
21 |
32 |
46 |
64 |
86 |
110 |
138 |
(1)农业上,硝酸钾用作水溶性肥料,为作物补充氮和钾元素。硝酸钾溶液中的溶质是______。
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。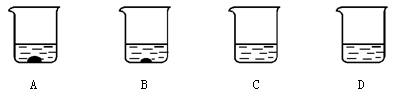
①(填字母序号) 中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为 g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是 (填字母序号)。
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(3)工业上利用电解饱和氯化钠溶液可制得重要化工产品氢氧化钠。氢氧化钠溶液可用于治理含二氧化硫的废气并回收二氧化硫,反应的主要流程如下: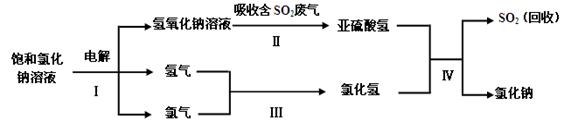
①实际生产中,在一定温度下,配制100t溶质的质量分数为25%的饱和氯化钠溶液,需水的质量为 t。
②以上流程中,可循环使用的物质是 。
③亚硫酸氢钠(NaHSO3)中硫元素的质量分数为 %(计算结果精确到0.1%)。
(漳州)图中甲、乙、丙是初中化学常见的物质,用“﹣”连接的两种物质在溶液中可发生化学反应,下列说法不正确的是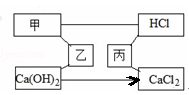
| A.甲可以为盐 |
| B.乙只能是氧化物或酸 |
| C.丙只能是金属单质、盐或碱 |
| D.其中一个反应能同时生成两种沉淀 |
2012年3月22日是第二十届“世界水日”。水与人类的生活和生产密切相关。
(1)下列做法有助于保护水资源的是 。
A.禁止向河流中排放废水
B.禁止向乱扔垃圾
C.节约用水
(2)水的硬度过大会影响生产和生活,区分软水和硬水常用的物质是 。生活中可以通过________的方法来降低水的硬度。
(3)自来水厂净水过程为:天然水→加絮凝剂→沉降→过滤→吸附→加消毒剂→自来水。通常使用的絮凝剂是 ;X是一种新型的自来水消毒剂,制取X的化学方程式为:C12+2NaClO2=2NaCl+2X,则X的化学式为 。
(4)下图为甲、乙(均不含结晶水)两种固体物质在水中的溶解度曲线。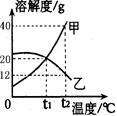
①溶解度随温度升高而增大的物质是 (填“甲”或“乙”);t1℃时,甲的溶解度_______乙的溶解度(填“大于”或“小于”或“等于”)。
②某同学在t1℃时开始如下实验,得到相应的溶液A、B、C。
在溶液A、B、C中,属于饱和溶液的是___________;与溶液C质量相等的是______。
在溶液C中再加入25g甲后,充分搅拌,恢复到t2℃,所得溶液的质量为______。
某学校实验小组的同学,在实验室里将稀硫酸和氯化钡溶液混合后,发现产生白色沉淀,他们将反应后的溶液进行过滤,得到滤液,滤液中溶质的成分是什么呢?于是他们进行了如下探究.
【提出问题】反应后滤液中溶质的成分是什么?
【猜想与假设】端端同学认为反应后滤液中的溶质是HCl
默默同学认为反应后滤液中的溶质是HCl、H2SO4
硕硕同学认为反应后滤液中的溶质是H2SO4和BaCl2
【探究与交流】(1)请说出端端同学猜想的理由_________________;
(2)上述哪位同学的猜想不正确 ;请说明理由_________________;
(3)默默同学为了证明自己的猜想,向反应后的滤液中加入几滴石蕊溶液,紫色石蕊溶液变红,于是认为自己猜想正确,请对他的结论进行评价_________________.
(4)经过同学们多次实验证明端端、默默的猜想都是错误的,滤液中的溶质应该是_________________.
现有木炭、二氧化碳、氧化铜、石灰水、稀硫酸和碳酸钾溶液六种物质.如图,已知硫酸的位置,请回答下列问题: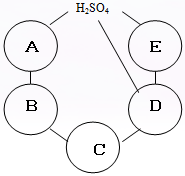
(1)请将另外五种物质的化学式填入圆内,使每个圆内的物质都能与其相连的圆内的物质反应;
(2)写出有木炭参加反应的化学方程式___________________;
(3)过量A与稀硫酸反应的实验现象为___________________________.
A~M均为初中化学常见物质,其中A是大理石主要成分,B是人体胃酸的一种主要成分,F是澄清石灰水主要成分,E是钠盐,它们之间有如图所示的相互转换关系(图中部分生成物已略去).请回答下列问题:
(1)E的俗称为 ,请画出K所含元素的原子结构示意图 .
(2)通电电解J时,通常加入少量烧碱或硫酸的目的是 ,电解一段时间后在相同条件下,生成气体L和气体K的体积之比约为 .
(3)请写出I在K中燃烧时的现象 ;⑥的基本反应类型为 .
(4)请写出⑤的化学方程式 .
试题篮
()