钠是一种活泼金属,常温下能与氧气、水等物质发生反应。钠与水反应的化学方程式为:2Na+2H2O═2NaOH+H2↑.在实验室,小亮先取定量的硫酸铜溶液于烧杯中,再取一小块钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤液的成分进行探究。
【提出问题】滤液中溶质的成分是什么?
【查阅资料】Na2SO4溶液呈中性
【猜想与假设】猜想一:Na2SO4
猜想二:Na2SO4和NaOH
猜想三:
猜想四:Na2SO4、CuSO4和NaOH
分析:小明认为猜想 不合理,理由是 (用化学方程式表示)。
【实验与验证】
实验 |
实验操作 |
实验現象 |
实验结论 |
实验一 |
取少量滤液于试管中,仔细观察现象 |
溶液为无色 |
猜想 不成立 |
实验二 |
向实验一所取滤液中滴入酚酞溶液 |
|
猜想二不成立 |
实验三 |
常温下,再取少量滤液,测溶液酸碱度 |
pH=7 |
猜想 成立 |
【拓展延伸】金属活动性顺序表中钠及前面的金属 (填“能”或“不能”)把位于后面的金属从它们盐溶液里置换出来。
某研究性学习小组设计了如图所示的装置,探究空气中氧气的体积分数,其中A是标有以cm为单位的刻度尺、且在0刻度正上方一圆状缺口处有一圆筒状玻璃容器(带橡皮塞B),C为能自由移动的活塞。

他们操作过程如下:
a.检查装置的气密性;
b.将两个可自由移动的活塞C分别调整到左右两边刻度的10 cm处;
c.将过量的铜粉平铺在惰性电热板上,塞上橡皮塞B;
d.通电加热铜粉,待充分反应后,冷却到原来的温度,记录两活塞C之间的距离为h;
e.根据数据h列出公式,计算空气中氧气的体积分数。
(注:A容器内的固态物质、惰性电热板、活塞部分所占体积忽略不计,活塞与玻璃容器之间的摩擦力也忽略不计)
(1)检查装置气密性的方法是分别移动两活塞C到左右两边刻度为10 cm处,塞紧橡皮塞B,双手将两活塞C向里推,使活塞之间的距离缩小,然后松手,活塞向外移动,直到两活塞C的距离为 cm时停止移动,说明装置气密性好。
(2)b~d的实验步骤中两活塞之间的距离h具体变化情况是 。
(3)空气中氧气的体积分数的计算公式(含字母h)为 。
(4)如果在操作d中惰性电热板没有冷却到原来温度,则e操作中计算出的实验结果比理论值偏 (“大”或“小”)。
(5)该装置和下图比,优点是 。

下列是初中化学部分重要的实验或实验装置,请按要求填空:
| A.水的电解实验 | B.测定空气里氧气含量 | C.探究二氧化碳性质 | D.气体制备装置 |
(1)A实验 玻璃管中产生的气体检验方法是 ;
(2)B实验如果实验数据小于21%,可能原因是 (写出一点);
(3)C实验说明二氧化碳具有的性质是 ;
(4)选择D装置制取气体的依据是 。
D装置可以制取那些气体 。
某化学兴趣活动小组为测定空气中氧气的含 量,进行如下探究实验:
如图所示,在一个具有刻度和可以滑动的活塞的玻璃容器中放入一粒白磷(白磷燃烧和红磷一样发生的是相同的反应,不同的是所需的最低温度为40℃),将玻璃容器固定好,放在盛有85℃热水的烧杯上。请回答下列问题:

实验中可以看到玻璃容器内白磷燃烧时的 现象是 ,该反应的文字表达式是 。实验结束后,恢复至常温,活塞应停在刻度__________处,出现该现象的原因是:白磷燃烧消耗了空气中气态的__________而生成了固态的________,从而使玻璃容器内的气体体积__________(填“增大”、“减小”或“不变”)。
此反应中白磷要过量,目的是_____________________________。
某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按如图所示装置进行实验(装置气密性良好:固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。

部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。
将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
Ⅱ.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 |
硬质玻璃管和样品 |
步骤Ⅱ硬质玻璃管和剩余固体 |
步骤Ⅲ硬质玻璃管和剩余固体 |
|
质量 |
m1 |
m2 |
m3 |
m4 |
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是 。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为 。
(3)样品中氧化铁的质量分数为 (用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将 (填“偏大”“偏小”或“不变”)
(4)有关样品,下列说法正确的是 (填字母标号)。
A.样品中氢元素的质量为 (m2﹣m3)
B.样品中铁单质和氧化铁的质量总和为m3﹣m1
C.样品中铁单质的质量为m4﹣m1
D.样品中氧元素的质量为m3﹣m4
有一包白色固体样品,可能含有NaOH、Na2CO3、K2SO4、BaCl2中的一种或几种,为确定其组成,进行如下实验:
步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,静置,有固体剩余。
步骤Ⅱ:取步骤I所得上层清液于试管中,滴入几滴酚酞溶液,溶液变红色;再滴入过量稀盐酸,无气泡产生,红色逐渐褪去,得到无色溶液。
步骤Ⅲ:取步骤Ⅱ所得溶液于试管中,滴入过量Ba(NO3)2溶液,无明显现象。
根据上述实验,回答下列问题:
(1)步骤Ⅱ中溶液的红色褪去,发生反应的化学方程式是 。
(2)分析上述实验过程,关于样品的组成,可以得到的结论是 。
(3)若要进一步确定样品的组成,还需进行的实验操作是 。
某课外活动小组通过网上资料得知:废弃的定影液中含有一定量的AgNO3。他们从摄影店收集到一些废弃的定影液,准备将其中的银以单质的形式全部回收。于是,他们进行了以下的实验活动:
(1)【设计方案】①加入比银活泼的金属单质 ②除去金属混合物中的杂质;
(2)【小组讨论】①选择加入的金属。
甲同学认为:向定影液中加入过量的铜粉,则得到的金属混合物含有银和铜;
乙同学认为:向定影液中加入过量的铁粉,则得到的金属混合物含有银和铁。
你认为 同学的方案更合理;
②除去银粉中混有的金属应向金属混合物中加入的试剂是 。
(3)【进行实验】过程如下:
①废弃定影液立金属混合物 + 溶液A ②金属混合物 Ag+溶液B (3)操作a,得金属Ag
请回答:操作a是 ,需要用到的玻璃仪器有:烧杯、玻璃棒和 。
(4)【产品验证】请你设计一种简单方法验证得到的银中是否还含有铁粉,方法是 。
水蒸气通过灼热的木炭后,流出气体的主要成分是CO 和H2,还有CO2和水蒸气等。请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气体中含有CO和H2。(假设每步反应均完全,加热装置和导管等在图中略去)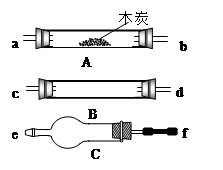
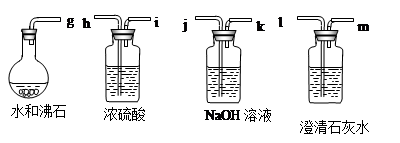
回答下列问题:
(1)盛浓H2SO4的装置用途是 ,盛NaOH溶液的装置用途是___。
(2)仪器 B中需加入试剂的名称(或化学式)是: ,
所发生反应的化学方程式是① ,
② 。
(3)固体干燥管 C 中需加入试剂的名称(或化学式)是: ,
其目的是 _____________ 。
(4)按气流方向连接各仪器,用字母表示接口的连接顺序:
g→ab→ 。
(5)能证明混合气中含有CO 的实验依据是 。
(6)能证明混合气中含有H2的实验依据是___________________ 。
小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究。
[查阅资料]这种“白色粉末”的主要成分是过碳酸钠(化学式为Na2CO4),常温下,与水反应生成氧气。
[实验1]小明选用如图所示装置中的 (选填序号)进行过碳酸钠与水的反应并收集产生的气体,经检验该气体是氧气,检验方法是
[提出问题]过碳酸钠与水反应后得到的溶液M中溶质的成分是什么?
[作出猜想]根据过碳酸钠与水的组成作出三种猜想。
猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH。
[实验2]小明取溶液M,滴加CaCl2溶液,观察到有白色沉淀生成,他认为白色沉淀是CaCO3,溶液中一定含有Na2CO3.小刚提出质疑,产生的白色沉淀不一定是CaCO3,他的理由是: 。
[实验3]小刚取溶液M,滴加稀HCl,观察到 ,证明溶液中一定含有Na2CO3,从而否定了猜想二。Na2CO3与稀HCl反应的化学方程式为 。
[实验4]为进一步确定溶液M中是否含有NaOH,他们向溶质M中滴加CaCl2溶液至不再产生沉淀为止,取上层溶液,加入 ,无明显现象。证明溶液中无NaOH溶液,猜想一正确。该实验中用CaCl2溶液而不用饱和石灰水,原因是: 。
[反思拓展]
(1)根据过碳酸钠的性质,保存时应注意防潮。
(2)检验A、B两种物质是否同时存在,一定要考虑二者性质的互相干扰问题。

当前,一次性筷子、一次性饭盒的安全问题受到社会关注。专家介绍说,正规的一次性筷子所用的原料都是质地较好的木材,不需特殊加工。但是很多小作坊为了降低成本,使用劣质木材,为了使筷子看上去更白、更新,他们常用硫磺熏制漂白,结果造成SO2严重超标,同时硫磺中含有铅、汞等重金属,也会造成人体铅中毒或汞中毒。
(1)一棵20年的大树仅可加工成一千多双一次性筷子,从珍惜资源和保护环境方面请给大家提一条合理化的建议。
(2)硫磺熏制的一次性筷子用水浸泡可降低SO2的含量,这说明SO2具有的物理性质是 ,为了研究SO2的性质,某同学做了如右图所示的实验:集气瓶中收集的是SO2,瓶内导管上系着瘪气球,通过胶头滴管向瓶中滴加紫色石蕊试液振荡,发现试液变红、气球膨胀,说明SO2可以跟 反应,化学方程式为 
(3)在制备一次性筷子的过程中要有“抛光”程序:加入滑石粉和木签一起搅拌,起到干燥、打磨作用,使筷子变得光滑,以免毛刺刺伤人的口腔。已知滑石粉是一种含水的具有层状结构的硅酸盐矿物,其化学式为:Mg3(Si4O10)(OH)2对于复杂的硅酸盐我们可以用氧化物的形式表示,如高岭土Al2(Si2O5)(OH)4可以表示为:Al2O3•2SiO2•2H2O ,则滑石粉用氧化物的表示形式为 。
构建知识网络是一种重要的学习方法。右图是有关铁的性质和获得的网络图。
(1)反应①的化学方程式为 。
(2)右图所示的六个反应中,一定属于置换反应的是 (选填序号)
(3)反应④可以通过铁制品锈蚀来实现(铁锈的主要成分是Fe2O3·xH2O),铁制品的锈蚀过程实际上是铁与 发生化学反应的过程。
(4)铜制品在空气中也会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3]。
①根据铜锈的主要成分中含有氢元素,可以判断出铜生锈需要空气中的 ;根据铜锈的主要成分中含有碳元素,可以判断出铜生锈需要空气中的 。
②某化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的氧气?”下图所示实验中(试管内的“ ”均为铜片),只需完成实验 和 即可达到探究目的(选填字母)。
”均为铜片),只需完成实验 和 即可达到探究目的(选填字母)。
有一包白色固体,可能含氯化钠、碳酸钠、硫酸钠、氢氧化钠、氢氧化钡中的一种或几种。某兴趣小组为探究其成分做了以下实验:
实验一:探究固体的组成

(1)向固体样品中加入过量稀硝酸,产生的气体是 。
(2)生成白色滤渣甲反应的化学方程式为 。
(3)原固体中一定不含有的物质是 。
实验二:进一步探究固体中是否含氯化钠

得出结论:原固体中一定含NaCl。
(4)试剂X是 溶液。
(5)滤液C中除含Fe(NO3)3外,一定还含有的溶质是 。
.以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;)
| 实验序号 |
过氧化氢溶液浓度/% |
过氧化氢溶液质量/g |
温度/℃ |
二氧化锰用量/g |
氧气体积/ml |
反应所需时间/s |
| ① |
5 |
12 |
20 |
0.2 |
125 |
11 |
| ② |
30 |
12 |
20 |
0.2 |
125 |
2 |
| ③ |
30 |
12 |
40 |
/ |
125 |
148 |
| ④ |
30 |
12 |
90 |
/ |
125 |
82 |
(1)通过实验①和②对比可知,化学反应快慢与 有关;
(2)通过对比实验 和 可知,化学反应快慢与温度的关系是
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是
(4)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:
NO和NO2具有下列不同的性质:
(1)通常情况下,NO是无色气体,难溶于水;NO2是红棕色气体,易溶于水。
(2)NO2与水反应的化学方程式为3NO2+H2O=2HNO3+NO。如下图,将一支充满NO2气体的试管倒立在烧杯中,试分析反应完全后可能出现的实验现象: 、
、 。
为了探究“水的净化”过程,某实验小组从护城河中取了水样,观察到:A.水样呈黄色,有异味 B.水样浑浊,有固体小颗粒。现对水样进行如下处理:①向水样中加入明矾搅拌溶解,静置一段时间后,进行 (填操作名称),除去固体小颗粒,再向滤液中加入活性炭,利用其 性除去水样中的颜色和异味,该过程属于 变化(填“物理”或“化学”)。②通入氯气杀菌消毒,得到自来水,发生的反应如下:Cl2+H2O=HCl+HClO(次氯酸)。请判断,次氯酸中氯元素的化合价为 。③请你设计一个实验检验经过上述步骤得到的水是纯净物还是混合物(写出实验步骤、现象、结论)
如果你再能设计两个正确实验检验将奖励你4分(总分不超过60分)
④为了判断得到的自来水是硬水或软水,可加入 进行检验。
试题篮
()