吴梁在距一支粉笔的粗端2cm处点上一滴蓝墨水,将粉笔插入盛有酒精的培养皿中。过了一段时间,吴梁发现随着酒精的上升,蓝墨水也在粉笔上不断移动,最后蓝墨水在粉笔上分为两个区域,上半部分是蓝色,下半部分是紫色(如右图所示)。根据上述现象回答下列问题:
(1)蓝墨水属于 (填“纯净物”或“混合物”);
(2)由此实验可以作出的推测是 (填序号)。
①用滤纸条代替粉笔重复上述实验,也能得到相似的实验现象
②不同分子在同种介质(如粉笔)中的运动速度不同
③不能用上述实验的原理分离混合物
下列是初中化学常见的四个实验,回答下列问题:
A B C D
(1)A实验中集气瓶内预先装少量水的目的是 。
(2)B实验中导致实验结果偏小的原因是 (只写一个)。
(3)C实验中该操作将导致所配溶液溶质质量分数 (填“偏大”、“偏小”或“不变”)。
(4)D实验中待 时,应停止加热。
质量守恒定律对科学发展具有重大意义。
(1)用如下图所示的3个实验验证质量守恒定律,其中不能达到实验目的的是_____(填序号),理由是_______________________。
(2)由质量守恒定律可知,化学反应前后一定不变的是 (填序号)。
① 原子种类 ② 原子数目 ③ 分子种类 ④ 分子数目 ⑤ 元素种类 ⑥ 物质种类
 (3)下图是某反应的微观示意图(其中“ ”和“ ”分别表示不同的原子)。
(3)下图是某反应的微观示意图(其中“ ”和“ ”分别表示不同的原子)。
① 反应后方框内应再填入 个“ ”微粒。
”微粒。
② 请从微观的角度分析化学变化的实质是_______________________________________。
下列是初中化学部分重要的实验或实验装置。请按要求填空:
| A.水的电解实验 | B.测定空气里氧气含量 | C.探究二氧化碳性质 | D.气体制备装置(1)A实验玻璃管②中产生的气体是;发生反应的方程式为 |
(2)B实验如果实验数据小于21%,可能原因是 (写出一点);
(3)C实验说明二氧化碳具有的性质是 ;
(4)D装置中长颈漏斗下端必须伸入液面以下,原因是
利用化学反应中气体产生的压力,可使多个化学反应依次发生,根据图示回答下列问题(A装置中的试剂足量,B、C、D中的试剂少量):
(1)打开A中分液漏斗的活塞,使稀盐酸逐滴滴下,A中的反应方程式是 。
(2)B中观察到的现象是 。
(3)C中开始和后来观察到的现象是 。
(4)D中发生反应的方程式 。
(5)E中的现象是 。
化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用是分不开的,结合下列实验装置图回答问题。试回答下列问题:
(1)写出图中有标号仪器的名称:
① ;② 。
(2)下列的几种途径都可以得到氧气。
写出实验室通过乙制取氧气的化学方程式 。
(3)实验室用加热高锰酸钾的方法制取氧气时,选用的发生装置是 (填字母代号)。用排水法收集氧气完毕后,停止加热前的操作是 。
(4)实验室制取二氧化碳时,可选用的发生装置是 (填字母代号)。收集二氧化碳时常用C装置,而不选用D或E装置,试从二氧化碳性质的角度分析其原因 。
某活动小组用废铜制取硫酸铜溶液,实验过程为:
⑴废铜在空气中加热后得到的氧化铜中含有少量铜,原因是________(填字母序号)。
a.加热时氧化铜易分解生成铜
b.铜与氧气没有完全反应
c.加热时铜不能与氧气反应
⑵操作Ⅰ的名称是 ,该操作用到的玻璃仪器有:玻璃棒、烧杯、 。
⑶盛放硫酸铜溶液不宜用铁制容器的原因是(用化学方程式解释) 。
⑷向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象可得,滤渣中一定含有 。
燃烧是一种发光、发热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
(1)物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,另外两个条件分别是: ; 。
(2)下面是验证燃烧条件的实验装置图。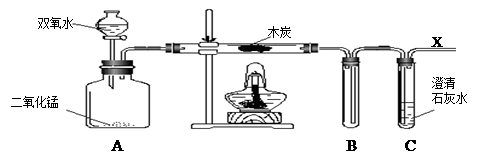
已知木炭是一种可燃物。请验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧(两个条件须分别验证),只有同时具备这两个条件才能燃烧。
某化学实验小组已经在完成气密性的检查后为你填装好了药品,并在整个装置中充满了氮气。
请你继续设计实验步骤完成后续探究,要求实验过程中不得拆、装仪器。
| 步骤 |
操作 |
预计现象 |
得出的结论 |
| ① |
a |
澄清石灰水 b |
说明燃烧需要氧气 |
| ② |
盖灭酒精灯,待仪器恢复到常温 |
|
|
| ③ |
打开活塞, c |
A中有气泡产生,C中石灰水 d |
e |
| ④ |
点燃酒精灯加热,继续通氧气 |
木炭燃烧,澄清石灰水 f |
g |
(3)①装置A中发生反应的化学方程式为 。
②装置B在“盖灭酒精灯,待仪器恢复到常温”这一步中的作用是 。
③小华同学认为,x处的气体不应直接排放到空气中去,大家经讨论后认为很有道理,你认为其中的道理是: 。
小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待的做起了这个实验:将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末。
⑴根据实验现象,我能写出该反应的化学方程式:____________________________________
⑵这个实验还引发了我对过去某些知识的反思,从而有些新的发现:
① _____________________________________;
②____________________________________。
氢氧化钠是一种重要的化工原料。
①少量氢氧化钠可用石灰石、水、纯碱(Na2CO3)为原料制取,流程如下:
Ⅰ.用化学方程式表示白色固体加入纯碱溶液后所有发生的化学反应 (10) 。
Ⅱ.滤液中存在少量的Na2CO3,用适量 (11) 试剂可以去除该物质。
②为测定某部分变质的氢氧化钠固体中氢氧化钠的质量分数,设计以下装置进行实验(假设每步实验都完全进行,浓硫酸具有吸水性)。
Ⅰ. 要确定该样品中氢氧化钠的质量分数,所需要的数据是 (12)
| A.固体样品的质量 |
| B.浓硫酸实验前后质量 |
| C.浓氢氧化钠溶液实验前后质量 |
| D.所用稀硫酸质量 |
E.仪器D中氢氧化钠固体实验前后质量
F.稀硫酸质量分数
Ⅱ. D装置的作用是 (13) 。没有D装置对氢氧化钠质量分数的测定结果影响是 (14) (填“偏大”“偏小”或“不变”)。
某同学用下图装置验证某混合气体中一定含有水蒸气、二氧化碳和一氧化碳三种气体(假设每步操作中,参加反应的气体都完全反应或吸收)。 
(1)该同学验证三种气体一定存在。实验进行时,若要气体从左向右流动,则这几种仪器的连接顺序应是:混合气体→ ( ) →( ) →D→( ) →( )(填A、B、C或E);
(2)B装置中观察到的现象为
(3)混合气体通过A装置发生反应的化学方程式为
寒假期间,小军给妈妈帮厨,发现一瓶没有标签的无色液体,小军问妈妈这是什么物质,小军妈妈要他猜一猜。
(1)小军打开瓶盖闻了闻,初步判断为白醋。请问小军是利用了白醋的 (填“物理”或“化学”)性质作出的判断。
(2)为进一步判断该液体是否为白醋,小军又进行了以下实验。
取少量该液体放入玻璃杯中,加入适量小苏打粉末(碳酸氢钠),观察,有气泡产生,说明该液体中含有 性(填“酸”、“碱”、“中”)物质。
(3)请你再设计一个简单实验,说明该液体的酸碱性(参照小军的实验方案,要求有简单的实验操作过程和现象,并得出结论)。
碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)是生活中常见的盐,有着广泛的用途,根据所学知识回答:
⑴碳酸钠和碳酸氢钠中阴离子对应的酸都是 (填化学式);
⑵碳酸钠常作食用碱,水溶液PH 7(填“>”“=”“<”)
⑶碳酸氢钠俗名 ,在医疗上用作治疗胃酸过多,反应的化学方程式为 ;
⑷碳酸钠固体中混有少量的碳酸氢钠,常用加热的方法除去碳酸氢钠,反应的化学方程式为2NaHCO3 Na2CO3+
Na2CO3+ ↑+H2O,则“
↑+H2O,则“ ”中的化学式为 ;
”中的化学式为 ;
⑸干粉灭火器利用碳酸氢钠来灭火,其灭火原理是 。
硫酸产量标志着一个国家化工业发展的水平。工业生产硫酸的主要流程为:
①煅烧黄铁矿4FeS2+11O2 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
②SO2转化为SO3 ③用浓H2SO4吸收SO3 请回答相关问题:
(1)如何利用流程①中形成的固体剩余物: 。
(2)SO2具有与CO2相似的化学性质。有人设计用熟石灰吸收尾气中的SO2,请写出此反应的化学方程式 。
(3)第②步反应是一个化合反应,请判断实现此反应的另一反应物是 。
(4)将SO2和Cl2通入水中至恰好完全反应,生成两种常见的酸,请完成下列化学方程式:Cl2+SO2+2H2O=== +2HCl
(5)实验室稀释浓硫酸的方法是:
。
氯化钡是一种可溶性重金属盐,广泛应用于化工领域,用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如下:
(1)毒重石要进行粉碎的目的是 ;气体X的化学式为 。
(2)操作Y的名称是 , 滤液2中可循环利用的物质除水外还有 。
洗涤氯化钡制品最适宜的洗涤剂是 (填字母)
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
试题篮
()