已知硝酸钾的溶解度随着温度的升高而增加,现有以下方法:
| A.加溶剂水 | B.加溶质硝酸钾 | C.升高温度 | D.降低温度 |
(1)能减小硝酸钾溶解度的方法是 。
(2)能使不饱和硝酸钾溶液变成饱和溶液的方法有 .
根据图1、图2中三种固体物质的溶解度曲线回答问题.
(1)分析图1,P点处A、B两种物质的溶解度关系是A B(填“>”、“<”或“=”);取一定质量的A的饱和溶液,将溶液温度从t℃降低到10℃,溶液中溶质的质量分数 (填“增大”、“减小”或“不变”)。
(2)分析图2,要使C的饱和溶液变成不饱和溶液,可采用的方法是:
① ;② 。
(3)10℃时,A、B、C的饱和溶液中溶质的质量分数由大到小的顺序是 。
(4)当A中含有少量B时,可以用 法提纯A。
在某温度下,NaCl 的溶解度为36g,求:
(1)在此温度下200g水最多可溶解 克NaCl
(2)2010g此温度下的饱和溶液里溶质的质量分数为 %(精确到0.1%)
下表是3种物质在不同温度时的溶解度,根据表格信息答题。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度/g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
| KNO3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
246 |
|
| Ca(OH)2 |
0.18 |
0.16 |
0.14 |
0.12 |
0.09 |
0.07 |
(1)某饱和溶液随温度升高有固体析出,则该饱和溶液的溶质是 (填化学式)。
(2)要配制20℃时的NaCl饱和溶液100g,需要NaCl的质量为 g(保留小数点后一位)。
(3)某KNO3晶体中有少量NaCl、Ca(OH)2杂质,要得到纯净KNO3的方法是:先加热溶解,然后 ,过滤、洗涤、干燥后得到KNO3晶体。
请根据下列实验和溶解度曲线回答问题: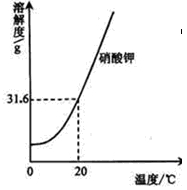
(已知水的密度约为1g/cm3)
| 实验操作 |
实验结果 |
| 取100mL水,加入25g硝酸钾,搅拌,恢复至20℃ |
全部溶解,得溶液① |
| 再加wg硝酸钾,搅拌,恢复至20℃ |
恰好饱和,得溶液② |
| 再加25g硝酸钾,搅拌,恢复至20℃ |
得溶液③ |
| 加热 |
全部溶解,得溶液④ |
| 冷却至20℃ |
析出晶体,得溶液⑤ |
(1)③中溶液的质量为 g;一定属于不饱和溶液的是(填序号,下同)
(2)析出晶体的质量为 。
A.25g B.(w+25)g C.(w+50)g
如下图①为甲、乙(均不含结晶水)两种固体物质的溶解度曲线。
(1)t1℃时,甲的溶解度 (填 “大于”“小于”或“等于”)乙的溶解度;若要从甲的饱和溶液中得到固体甲,则采用 方法。
(2)某同学在t1℃时开始进行如图②实验, 在烧杯A、B、C中能得到饱和溶液的是 (填编号),溶质质量分数最大的是 (填编号);
(3)烧杯C中再加入15g甲后,充分搅拌,恢复到t2℃时,所得溶液的质量是 g。
海水是种宝贵资源。
(1)“海水晒盐”所采用的方法是 (填写编号)。
I.冷却结晶 II.蒸发结晶 III.过滤
(2)海上航行缺乏饮用水时可采用下图装置获得淡水。用该装置将2000g含氯化钠3%的海水暴晒4小时后, 剩余海水中氯化钠的质量分数为4%,则收集到的可饮用水为 g。
(3)海水中的硼酸(化学式为H3BO3)可用于玻璃工业,下表为硼酸的部分溶解度数据。
| 温度(℃) |
0 |
20 |
40 |
60 |
80 |
| 溶解度(g/100g水) |
3 |
5 |
9 |
15 |
23 |
I.由表可知,硼酸的溶解度随着温度的升高而 (填“增大”或“减小”或“不变”)。
II.60℃时,100g硼酸饱和溶液中含有硼酸 g(保留整数)。
III.某同学设计如下实验探究“温度”及“固体溶质的形态”对溶解速率的影响。
a.上述三个烧杯中,所得溶液浓度的大小关系是 (用“①”、“②”、“③”表示);。b.若要达到实验目的,需改变实验①中的一个条件是 (从以下选项中选择)
A.将20℃的水改为80℃ B.将水的体积改为50mL C.将粉末状固体改为块状
甲图是氯化钠在水中的溶解度曲线,乙图是硝酸钾在水中的溶解度曲线,丙图是氯化钠在某有机溶剂中的溶解度曲线。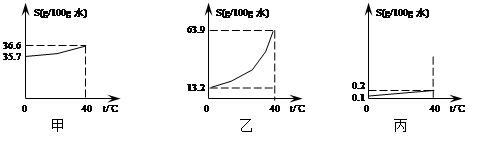
请将甲图分别与上述其它曲线对比,回答下列问题:
(1)由甲、丙得出影响固体物质溶解度的因素是 。
(2)由甲、乙得出影响固体物质溶解度的因素是 。因此欲除去硝酸钾溶液中混有的少量氯化钠溶液可采用 方法。
(3)40℃时,在50g水中加入30g硝酸钾,所得溶液是 (填“饱和”或“不饱和”)溶液,此时溶液的质量分数是 ;若将该溶液从40℃降温到0℃时,析出硝酸钾晶体质量为 g。
水是重要的自然资源,在化学实验中起重要作用。
Ⅰ.请根据以下实验回答问题:
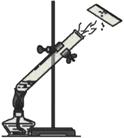
(1)从微观角度分析,下图所示实验1和实验2的本质区别是 。
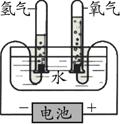
(2)由实验2可以得出水是由 组成的。
 |
 |
 |
 |
| 实验1 水的沸腾 |
实验2 电解水 |
图1 |
图2 |
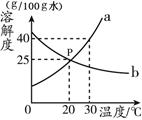
Ⅱ.水是很好的溶剂。图1所示是a、b两种固体物质在水中溶解度曲线,根据上图回答:
(3)曲线上P点的含义是 。
(4)a物质溶解度小于b物质溶解度的温度范围是 。
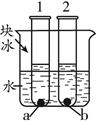
(5)上图2所示,试管1、2中分别盛有20℃时等质量的a、b物质饱和溶液,底部有等质量的a、b固体剩余,向烧杯的水中加入冰块,下列判断正确的是 (不考虑溶剂的蒸发,析出的固体不含水)
A.a物质溶液由饱和溶液变成不饱和溶液
B.试管2底部的b物质固体减少
C.变化后溶液中溶质质量分数:a > b
D.a、b物质的溶液中溶剂质量相等
下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
| 温度/℃ |
0 |
20 |
40 |
80 |
100 |
|
| 溶解度/ g/100g水 |
Ca(OH)2 |
0.173 |
0.165 |
0.121 |
0.094 |
0.076 |
| NaOH |
31 |
91 |
111 |
313 |
336 |
①从上表数据可以看出,氢氧化钙的溶解度随温度的升高而 。
②40℃时,将20g水配成氢氧化钠饱和溶液,需氢氧化钠的质量为 克。若将40℃时422克的氢氧化钠饱和溶液稀释为20%的溶液,需加水⒁克。
③80℃时含有Ca(OH)2和NaOH两种溶质的饱和溶液,若要从中得到较纯净的NaOH晶体,应采取的物理方法是 。
④现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液), 此时甲乙两杯溶液中 。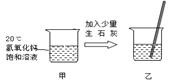
A.甲的溶质的质量分数与乙的相同
B.甲的溶质的质量分数大于乙的
C.甲的溶质的质量小于乙的
D.甲、乙都是饱和溶液
如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t1℃时,向两只盛有100g水的烧杯中,分别加入A、B两种物质至不能溶解为止,所得溶液的溶质质量分数较大的是 溶液(填“A”或“B””)。
(2)将t2℃的A、B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A B。
(3)将t2℃的A、B两种物质的饱和溶液升温至t3℃,欲使它们仍为饱和溶液,可采取的方法有 。(答一条即可)
根据如图A、B、C三种固体的溶解度曲线回答:
(1)要使C的饱和溶液变成不饱和溶液,可采用的一种方法是 ;
(2)将三种物质饱和溶液的温度分别从50 ℃降到20 ℃时,溶液中溶质的质量分数最大的是 。
水和溶液在生产、生活中十分常见。
(1)自然界的水往往会混有很多种杂质,若用如图所示装置净化水,其中活性炭的作用是 。
(2)图1是a、b两种固体物质(不含结晶水)在水中的溶解度曲线:
①a的溶解度小于b的溶解度的温度范围是 。
② 一只烧杯中盛有36g a物质,加入温度为30℃的水80g,充分搅拌,得到的溶液是 (填“不饱和溶液”或“饱和溶液”);溶液中溶质与溶液的质量比为 。
③如图2所示,试管1、2中分别盛有20℃时等质量的a、b物质的饱和溶液,底部有等质量的a、b物质剩余,向烧杯里的水中加入冰块,下列判断错误的是 (忽略溶剂的蒸发,析出的晶体不含结晶水)
| A.试管2底部的固体减少 |
| B.a的溶液由饱和溶液变成不饱和溶液 |
| C.a的溶液中溶剂质量等于b的溶液中溶剂质量 |
| D.变化后b的溶液中溶质质量分数大于a的溶液中溶质质量分数 |
学完溶液知识后,小明同学回家用蔗糖、洗洁精、花生油、大理石和水相互混合做了几个家庭小实验。
(1)在同一条件下,蔗糖易溶于水,难溶于花生油;大理石不溶于水,也不溶于花生油,由此说明物质的溶解能力与 有关。
(2)除(1)中的因素外,你认为固体物质的溶解能力还与 有关。请你举出一个生活中常见的例子,如 。
(1)小明绘制的三种固体物质的溶解度曲线如图所示.
①在t2℃时,甲物质的溶解度为 ;
②其不饱和溶液可以通过升温转变成饱和溶液的是 。
(2)目前市场上销售的汽水饮料大多数是碳酸饮料,其中溶有二氧化碳气体。打开汽水瓶瓶盖时,汽水会自动喷出来。这说明气体在水中的溶解度与 有关。喝了汽水后,常常会打嗝,这说明气体的溶解度还与 有关。
试题篮
()