下列说法中正确的是( )
A.凡是生成盐和水的反应都是中和反应
B.盐类物质中不一定含有金属元素
C.饱和溶液降温一定能析出晶体
D.碳酸饱和溶液的浓度比硼酸不饱和溶液的浓度大
如图所示,下列判断正确的是( )
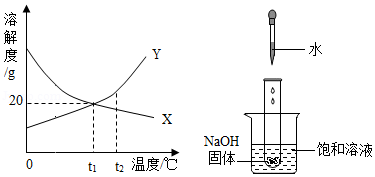
A.Y的溶解度比X的溶解度大
B.t1℃时,X、Y两种饱和溶液的溶质质量分数都是20%
C.若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D.t2℃时,若X、Y 的饱和溶液质量相等,则溶液中溶质的质量X<Y
KNO3和KCl的溶解度曲线如图所示:
(1)t3℃时,KNO3的溶解度为 。
(2)将t3℃时KCl的饱和溶液70.0g稀释成质量分数为20.0%的KCl溶液,需加水 g(精确到0.1g)。查阅相关物质的密度后,在实验室完成该实验通常需要的仪器有烧杯、量筒、 (填字母标号)。
A.托盘天平 B.药匙 C.胶头滴管 D.玻璃棒
(3)现有t2℃时KNO3的饱和溶液m1g和KCl的饱和溶液m2g.不考虑水的蒸发,下列关系一定成立的是 (填字母标号)。
A.两溶液中溶质的质量分数相等
B.分别降温到t1℃,析出KNO3的质量大于析出KCl的质量
C.分别升温至t3℃,所得溶液中溶质的质量分数相等
D.保持t2℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等

材料一:侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:
①20℃时,将CO 2通入含NH 3的饱和NaCl溶液中,生成 NaHCO 3晶体和NH 4Cl溶液。
②将①中的产物 NaHCO 3晶体充分加热分解,得到Na 2CO 3、H 2O和CO 2。
材料二:20℃时几种物质在水中的溶解度/g
| NaCl |
NH 4Cl |
NaHCO 3 |
| 36.0 |
37.2 |
9.6 |
请回答下列问题:
(1)在第①步反应中,有 NaHCO 3晶体析出,而没有NH 4Cl和NaCl晶体析出的原因是 。
(2)该生产过程中部分生成物可作为原料循环使用的是 ,同时得到的副产品NH 4Cl是一种氮肥。

X、Y、Z三种物质的溶解度曲线如图所示。下列说法正确的是( )

A.将T2℃时三种物质的饱和溶液降温到T1℃后,溶质质量分数大小关系为:Y>X>Z
B.Y的溶解度为50g
C.降低温度可使Z的不饱和溶液变成饱和溶液
D.T2℃时,50gH2O与50gX混合,可得到100gX的饱和溶液
作图法是常用的数据处理方法。如图是A、B、C三种物质的溶解度曲线图,请回答下列问题:
(1)P点的意义是 。
(2)t3℃时,A、B、C三种物质溶解度最大的是 。
(3)将某温度下C的不饱和溶液变成饱和溶液的方法是 (写一种)。
(4)在t3℃时,将A、B、C的饱和溶液分别降温到t1℃时,所得溶液溶质的质量分数由大到小的顺序是 。

请根据如图a、b、c三种固体的溶解度曲线,回答下列问题:
(1)P点的含义: 。
(2)若b物质中混有少量a物质,最好采用 的方法提纯b(填“降温结晶”或“蒸发结晶”)。
(3)下列说法正确的是 。
A.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减少
B.t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序c>b>a
C.将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减少

某同学对下表中的溶解度数据分析后,得出的结论错误的是( )
温度/℃ |
0 |
20 |
40 |
60 |
氢氧化钙的溶解度/g |
0.18 |
0.16 |
0.14 |
0.11 |
硝酸钾的溶解度/g |
13.3 |
31.6 |
61.9 |
110 |
氯化钠的溶解度/g |
35.7 |
36 |
36.6 |
37.2 |
A.升温可将20℃时不饱和的Ca(OH)2溶液变为饱和溶液
B.60℃,饱和KNO3溶液的质量分数约为52.4%
C.温度变化对NaCl的溶解度影响较小
D.NaCl的溶解度大于KNO3的溶解度
MgSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是( )

A.N点对应的MgSO4溶液升温或降温均都可能析出晶体
B.M点对应的MgSO4溶液是不饱和溶液
C.MgSO4饱和溶液的溶质质量分数随温度升高而增大
D.40℃时,MgSO4的溶解度为41g
甲、乙、丙三种固体(均不含结晶水)的溶解度曲线如图所示,请回答下列问题:
(I) t2℃时,甲、乙、丙三种物质溶解度大小关系是 。
(2)t3℃时,将20g物质丙加入50g水中充分溶解,井恢复到原温度,所得溶液的质量为 g。
(3)在不改变溶质质量分数的前提下,将甲的不饱和溶液转化为饱和溶液的方法是 。
(4)下列说法正确的是 。
A.甲中混有少量乙时,可用降温结晶的方法提纯甲;
B.t2℃时,甲、丙两物质饱和溶液中所含溶质质量相等;
C.将t3℃时的甲、丙的饱和溶液降低温度至t2℃,溶质的质量分数相等;
D.t1℃时,用甲、乙、丙三种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲>丙。

已知NaOH、Na2CO3、NaCl三种物质在不同温度下的溶解度(g)如表所示。
t/℃ 溶解度(g) 物质 |
NaOH |
Na2CO3 |
NaCl |
10 |
51 |
12.2 |
35.8 |
20 |
109 |
21.8 |
36.0 |
30 |
119 |
39.7 |
36.3 |
(1)分析表中数据,其中溶解度受温度影响变化最小的物质是 。
(2)20℃时,将三种物质各15g分别溶解在50g水中,其中可以形成饱和溶液的是 。
根据如图所示溶解度曲线判断,下列说法正确的是( )
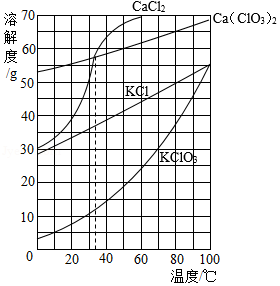
A.20℃时,将10 g KClO3加入100 g水中,溶液质量为110 g
B.30℃时,KCl饱和溶液中溶质的质量分数约为35%
C.分别将35℃的CaCl2和Ca(ClO3)2两种饱和溶液升温至40℃,CaCl2溶液中溶质的质量分数较大
D.除去CaCl2中混有的少量Ca(ClO3)2,可在较高温度配成饱和溶液,再降温结晶、过滤
a、b是常见的两种固体物质,根据图表的信息回答下列问题:

物质b的溶解度表
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| b的溶解度/g |
14 |
20 |
30 |
45 |
65 |
85 |
110 |
(1)60℃时,物质a的溶解度是 g;
(2)20℃时,将20g物质b加入到50g水中,充分溶解后得到溶液的质量为 g;
(3)将50℃时a、b两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数大小关系为a b(填">"、"="或者"<");
(4)下列说法正确的组合是 (填字母序号)。
①所有物质的溶解度都随温度的升高而增大
②30℃时,物质的溶解度a小于b
③物质b中含有少量a时,可以采用降温结晶的方法提纯b
④40℃时,分别将物质a、b的饱和溶液降温至10℃,析出物质的质量b大于a
A.①④B.①③C.②③D.②④
青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆咸水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。
(1)“夏天晒盐”中的“盐”其溶解度可用图中 来表示(填“a”、或“b”、或“c”)。
(2)在t1℃时,三种物质的溶解度大小关系是 。
(3)在t2℃时,将40g的a放入50g水中充分搅拌,所得溶液质量为 g。
(4)将t2℃时a、b、c的饱和溶液降温至t1℃时,溶质的质量分数由大到小的顺序为 。

试题篮
()