下表为甲、乙、丙三种物质的溶解度,请结合表中信息判断下列说法正确的是( )
温度/℃ |
0 |
10 |
20 |
T |
30 |
40 |
50 |
|
溶解度/g |
甲 |
13.3 |
20.9 |
31.6 |
39.1 |
45.8 |
63.9 |
85.5 |
乙 |
29.4 |
33.3 |
37.2 |
39.1 |
41.1 |
45.8 |
50.4 |
|
丙 |
35.7 |
35.8 |
36.0 |
36.2 |
36.3 |
36.6 |
37.0 |
|
A.三种物质的溶解度大小为:甲>乙>丙
B.随着温度变化,甲的溶解度变化最小
C.30℃时,100g丙的饱和溶液中,溶质的质量为36.3g
D.分别将50℃时甲、乙的饱和溶液降温至T℃,两种溶液中溶质的质量分数相等
下列图象不能正确反映其对应关系是( )
A. 等质量的镁粉和铝粉与足量的同种稀盐酸反应
等质量的镁粉和铝粉与足量的同种稀盐酸反应
B. 在一定温度下,向接近饱和的硝酸钾溶液加入硝酸钾固体
在一定温度下,向接近饱和的硝酸钾溶液加入硝酸钾固体
C. 敞口放置的浓盐酸
敞口放置的浓盐酸
D. 向含有硫酸和硫酸铜的溶液中滴加NaOH溶液
向含有硫酸和硫酸铜的溶液中滴加NaOH溶液
NaCl和KNO3,在不同温度时的溶解度如下:

温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解 度/g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
|
请回答下列问题:
(1)10℃时,在100g水里溶解 g KNO3时,溶液恰好达到饱和状态。
(2)如图为NaCl和KNO3的溶解度曲线,表示NaCl的溶解度曲线的是 (填“甲”或“乙”)。
(3)在温度为t℃时,甲、乙的溶解度大小关系为甲 (填“>”“=”或“<”)乙。
(4)若甲中混有少量乙,可用 结晶的方法提纯甲。
如图所示为①KNO3②NaCl③H3BO3的溶解度曲线,由图可知:
(1) 当温度为10℃时 ,KNO3、 NaCl 和 H3BO3 三种物质的溶解度由大到小的顺序为 (用序号作答)。
(2) 当温度为t℃时 , 在三种物质的饱和溶液中溶质的质量分数 由 大 到 小 的顺序为 (用序号作答)。
(3)要将P点处的KNO3溶液变成饱和溶液,可采取的措施有:加入KNO3固体、 等(任写一条)。

甲、乙两种固体物质的溶解度曲线如图所示,据图回答下列问题:
(1)乙物质的溶解度随温度的升高而 (填“增大”或“减小”).
(2)欲将t1℃甲物质的不饱和溶液变为该温度下的饱和溶液,可采取的方法: (任填一种).
(3)若甲物质中混有少量乙物质,可用 的方法提纯甲.
(4)等质量甲、乙两种物质分别配成t2℃时的饱和溶液,需要水的质量大小关系是
甲 乙(填“>”、“=”或“<”).

t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。
(1)烧杯②中的上层清液是否达到饱和状态? (填“是”“否”或“无法判断”);
(2)烧杯①中溶解的溶质是 (写名称或化学式);
(3)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水 g;
(4)关于图1中烧杯内的物质,下列说法正确的是 。
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)

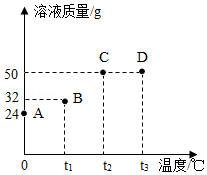
将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得0℃、t1℃、t2℃、t3℃时烧杯中溶液的质量分别如图中A、B、C、D点所示。回答下列问题:
(1)A、B两点对应的溶液中溶质的质量分数较大的是 (填字母编号)。
(2)0℃时,物质X的溶解度是 。
(3)A、B、C、D四点对应的溶液中,一定属于饱和溶液的是 (填字母编号)。
(4)下列说法正确的是 (填序号)。
①t1℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液为不饱和溶液
②若要从D点对应的溶液中得到全部固体X,可采用降温结晶的方法
③t2℃时,将物质X的饱和溶液变为不饱和溶液,溶质的质量可能增大
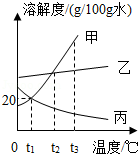
如图所示为①KNO3②NaCl③H3BO3 的溶解度曲线,下列说法错误的是( )

A.在 10℃时,三种物质溶解度的大小顺序为②>①>③
B.在t℃时,三种物质饱和溶液中溶质质量分数的大小顺序为①=②>③
C.将P点处的KNO3溶液蒸发适量水可变成饱和溶液
D.将P点处的KNO3溶液降温一定会析出KNO3晶体
如图所示是甲、乙、丙三种固体物质的溶解度曲线。
(1)t 2℃时,甲、乙、丙三种物质的溶解度大小关系是 ;
(2)t 1℃时,50g水中加入30g的甲物质充分溶解后,可得到 g溶液;
(3)下列说法正确的是(填序号) 。
①t 1℃时,甲、丙两溶液的溶质质量分数一定相等
②t 3℃时,向100g20%甲的溶液中加100g水,充分搅拌,溶液的溶质质量分数为10%
③t 2℃时,升高丙溶液的温度,一定有晶体析出
④t 3℃时,用等质量的甲、乙、丙分别配制成三种物质的饱和溶液,所需溶剂的质量为甲<乙<丙。
(1)下列是与水有关的几个描述,请根据所学知识填写完整:
①自然界中的水大多是 (选填"混合物"或"纯净物");
② (填物质名称)具有吸附性,可用于水的净化;
③电解H 2O时,与直流电源的 (选填"正"或"负")极相连的电极附近得到H 2.
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示,请据图回答下列问题:
④ ℃时,甲和乙两种物质的溶解度相等.
⑤t 3℃时,将甲、乙、丙的饱和溶液分别降温到t 2℃ (选填"甲"、"乙"或"丙")变为不饱和溶液.
⑥t 1℃时,甲、乙、丙三种饱和溶液的溶质的质量分数由大到小的顺序为 .

生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水,水是最常用的溶剂。
(1)电解水实验如图所示。x是电源的 极(填“正”或“负”),检验b试管中所得气体的方法是 。

(2)A、B两种物质的溶解度曲线如图1所示:20℃时,将A、B两种固体各50g,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图2所示;升温到50℃时,A、B两种固体在水中的溶解情况如图3所示,(A、B两物质均不含结晶水)
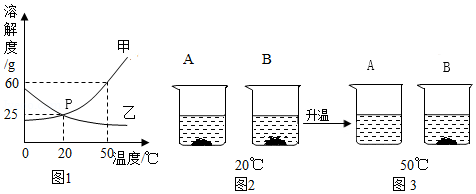
请回答下列问题:
①从20℃到50℃的变化过程中,一直处于饱和状态的是 (填“A”或“B”)的溶液。
②图1中能表示A物质溶解度随温度变化的曲线是 (填“甲”或“乙”)。
③图1中P点的含义 。
④图3中A溶液的溶质质量分数 (精确到0.1%)
A、B、C三种固体物质的溶解度曲线如图所示。请回答下列问题。
(1)t 1℃时,溶解度相同的物质是 。
(2)若保持溶液质量不变,将C的饱和溶液变为不饱和溶液的方法是 。
(3)t 2℃时,把50gA放入50g水中,所得溶液中溶质和溶液的质量比为 (填最简整数比)。
(4)将t 2℃时等质量的A、B、C三种物质的饱和溶液,降温度温至t 1℃时所得溶液中溶剂质量由大到小顺序为 。

如图是A、B两种固体物质的溶解度曲线。
(1)当温度为 ℃时,A.B两种物质的溶解度相等。
(2)欲使饱和状态的B溶液变成不饱和溶液,可采用的一种方法是 。
(3)t2℃时,将30gA物质加入50g水中,充分溶解后,所得溶液中溶质与溶液的质量比是 。
(4)将t2℃等质量的A、B饱和溶液降温至t1℃,所得溶液的质量关系A B(选填“>”。“<”或“=”)

溶液与人们的生产生活密切相关。
(1)下列常见物质不属于溶液的是 (填序号)。
A.生理盐水
B.糖水
C.医用酒精
D.牛奶
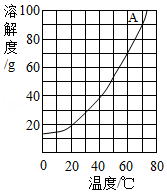
(2)如图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。
| 温度/℃ |
B物质溶解度/g |
| 0 |
32 |
| 20 |
35 |
| 40 |
40 |
| 60 |
45 |
| 80 |
55 |
①60℃时,A物质的溶解度是 g。
②50℃时,向100g水中加入40g B物质,充分溶解后得到的是 (填"饱和"或"不饱和")溶液,此时溶液的溶质质量分数是 (结果保留两位小数)。
③请根据表格数据,在A物质溶解度曲线图上绘出B物质的溶解度曲线。
④A、B两种物质溶解度相同时的温度是 ℃。
(3)生活中常用75%酒精消毒液对手和皮肤进行消毒。请分析酒精浓度与杀死细菌的时间对比表(如下)中的数据,酒精消毒液的最合适浓度应为 。根据酒精的物理性质,你认为两者浓度差异的主要原因是 。
| 酒精浓度(%) |
大肠杆菌 |
金黄色葡萄球菌 |
溶血性链球菌 |
| 90 |
15小时 |
30分钟 |
5分钟 |
| 80 |
1小时 |
30分钟 |
5分钟 |
| 70 |
30秒 |
5分钟 |
10秒 |
| 60 |
20秒 |
30分钟 |
10秒 |
| 50 |
20秒 |
2小时 |
20秒 |
| 40 |
22分钟 |
4小时 |
2分钟 |
试题篮
()