2015年4月13日,西昌市动物疫病预防控制中心堆放在仓库中浓度为21%的过氧乙酸消毒液发生泄漏.经查阅资料可知:过氧乙酸是无色液体.有强烈刺激性气味,易挥发,温度稍高即分解为乙酸和氧气。请回答下列问题:
(1)请任写一条过氧乙酸的物理性质: 。
(2)乙酸和过氧乙酸都是无色液体,都有刺激性气味。区分这两种液体可采用的方法是: 。
化学与生活息息相关,化学物质对生活、生产起到很重要的作用
(1)氧气在生活、工业上都有重要用途,下列氧气的用途是利用氧气可以维持呼吸的是
| A.动植物呼吸 | B.医疗急救 | C.潜水 | D.气割、气焊 |
(2)液氢是火箭发射的重要燃料,其燃烧时放出大量的热,请写出液氢燃烧的文字或符号表达式 ;
(3)硫在空气燃烧的产物对环境有危害,会导致酸雨,实验室进行硫燃烧的实验时,先在集气瓶中 放少量的水,水的主要作用是 ,此操作说明硫燃烧的产物 (填可溶或不溶)于水,硫燃烧的文字或符号表达式为 。
(1)下列物质:①洁净的空气 ②食醋 ③海水 ④五氧化二磷 ⑤人呼出的气体 ⑥氮气 ⑦加碘食盐 ⑧高锰酸钾 ⑨冰水混合物。属于纯净物的是: (填序号,下同)
属于混合物的是: ;
(2)下列描述:
| A.铁丝能在氧气中燃烧 | B.木材制成家具 |
| C.食品变质 | D.液态氧是淡蓝色的。 |
其中描述物理变化的是____,描述化学变化的是____,描述物理性质的是_____,描述化学性质的是_ ___。(均填编号)
合成氨是人类科学技术上的一项重大突破,对社会发展与进步做出了巨大贡献。合成氨的工艺流程图如下:

(1)该工艺流程中能循环利用的物质是_____________。
(2)写出变化②中N2、H2反应生成NH3的符号表达式:_________________________。
(3)将沸点不同的气体分离开来,常采用液化分离法。如本流程中将产物NH3与N2、H2分离开来的最适宜的温度是-33.35℃。则根据下表判断,变化①将空气中N2与O2分离时最适宜的温度是________℃。变化①属于__________变化。
| 物质 |
H2 |
N2 |
O2 |
NH3 |
| 沸点/℃ |
-252 |
-195.8 |
-183 |
-33.35 |
新版《生活饮用水卫生标准》(简称新国标)中水质检测指标从原来的35项增加到106项.对供水各环节的水质提出了相应的要求.
(1)新国标在无机物指标中修订了镉、铅等的限量.这里的镉、铅指的是 (填序号).
| A.原子 | B.分子 |
| C.元素 | D.单质 |
(2)新国标中对水的pH的规定为6.5≤pH≤8.5.实验室用pH试纸测得自来水的pH=8,说明该自来水显 (填“酸”、“碱”或“中”)性.
(3)新国标中消毒剂由1项增至4项,加入了对用臭氧、二氧化氯和氯胺消毒的规定.①臭氧(O3)在消毒过程中转化为氧气.臭氧转化为氧气属于 (填“物理”或者“化学”)变化.②二氧化氯消毒过程中产生的次氯酸根离子(ClO﹣)也有消毒作用.ClO﹣中氯元素的化合价为 价③氯胺(NH2Cl)由 (填数字)种元素组成.用氯胺消毒时,反应的化学方程式是NH2Cl+X=NH3+HClO,其中X的化学式为 .
甲、乙、丙、丁、戊是5种常见物质,由氢、氧、硫、钙4种元素中的1一3种组成。
(l)甲是无色有刺激性气味的气体,也是空气污染物之一,则甲的化学式是 。
(2)乙是一种无色液体,将人体呼出的气体吹人乙中出现浑浊现象,则液体乙是 。
(3)丙在一定条件下发生反应的微观示意图如下,在方框中补全相应微粒的图示。
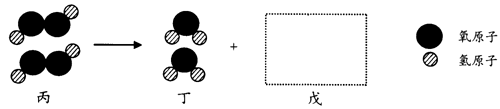
(4)丁在一定条件下反应生成戊,该反应的文字表达式为 。
(5)下列说法正确的是 (填字母序号)。
| A.甲、丁、戊都是氧化物 |
| B.甲、丙、戊中都含有氧分子 |
| C.丁和戊在一定条件下可以相互转化 |
| D.(3)和(4)中发生的反应都是分解反应 |
、
、
、
都是初中化学的常见物质,它们存在如下图所示的转化关系("-"表示两端的物质间能发生化学反应,"→"表示物质间存在转化关系。部分反应物、生成物及反应条件已略去)。
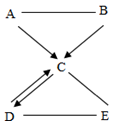
其中
、
为单质且
是可供动植物呼吸的气体;
是一种盐,
是常用于改良酸性土壤的碱。请回答下列问题:
(1)
的俗名是,
是。
(2)在一定条件下,
既可以转化成
,也可以与
发生化学反应。写出
和
反应的化学方程式。
(3)写出
与
反应的化学方程式。
烧杯中盛装一定质量的碳酸钠粉末,试管中是一定质量的稀盐酸,反应前称得总质量为M1。将稀盐酸倒入烧杯中,待反应完全后,称得总质量为M2。
(已知:Na2CO3+2HCl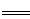 2NaCl+CO2↑+H2O)
2NaCl+CO2↑+H2O)
(1)实验现象除了产生大量气泡外,M1______M2。(填“>”,“<”或“=”)产生这种现象的原因____________________
(2)该反应__________(“遵守”或“不遵守”)质量守恒定律。
(3)若要用该实验来验证质量守恒定律,实验需在_______________容器中进行。
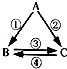
已知A、B、C是初中化学的常见物质,其相互关系如图所示.若A、B是组成元素相同且常温下都为液态的氧化物,C为供给呼吸,则A的化学式为 ,C为化学式为 ,反应①的化学方程式为 .
在用白磷探究质量守恒定律的实验中,同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示.请回答下列问题: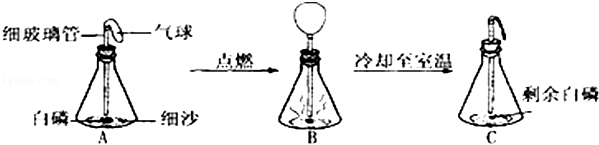
(1)图中瓶底铺细沙的作用是: .
(2)白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡.结论是质量不守恒.待锥形瓶冷却后,重新放到托盘天平上称量,天平保持平衡.结论是:质量守恒.你认为结论正确的是 ( 填“前一种”或“后一种”).而导致另一种结论错误的原因是 ..
(3)实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是:
(4)由质量守恒定律可知,化学反应前后,一定不变的是 .(填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类.
将新鲜的鸡蛋浸泡在饱和石灰水中可使鸡蛋贮存6~7个月不变质.石灰水是用新烧制的生石灰配制成的,写出下列变化的化学方程式:
①烧制生石灰: ;
②配制石灰水 .
③石灰水可使鸡蛋不变质的原因是(用化学方程式表示) .
④浸泡一段时间后,鸡蛋的表面形成一层白色的覆盖物,白色覆盖物可以用稀盐酸除去,反应原理是 .
上面四个化学反应中,属于化合反应的是 ,属于分解反应的是 ,属于复分解反应的是 .(填番号)
下列基本技能都是你必须具备的,你能作出正确回答吗?
(1)用下列字母序号填空:
| A.石墨 | B.氮气 | C.二氧化硫 | D.氧气 |
①会形成酸雨的是 ;②充入食品包装袋以防腐的是 ;
③可用于铅笔芯的是 ;④医疗上用于抢救危重病人的是 。
(2)用相应的化学用语回答:
①两个氢原子 ;②三个水分子 ;
③两个硝酸根离子 ;④地壳中最多金属元素的氧化物 ;
(3)下面是四种粒子的结构示意图,用字母序号填空。

①属于同种元素的是 ;
②表示阴离子的是 ;
③AD表示的粒子形成的化合物为 ;(用化学式填空)。
已知A~F都是初中化学中的常见物质, A为黑色固体单质,C是无色无味气体,能是澄清石灰水变浑浊, D是红色固体,C→E是自然界中最常见的转化。物质间的转化关系如图所示:
(1)写出下列物质的化学式:B _________, E _________;
(2)写出A与B反应的化学方程式:_________________________
(1)天然水受到污染后,净化时需要运用科学的方法,同时要爱护水资源。
①自来水生产过程中先用 的方法除去水中不溶性杂质,再进行消毒。在操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是 。(填序号).

②若发现滤纸和漏斗间有气泡,可能的影响是__ ___,处理的方法是___ ___。
③地下水硬度过大会影响生产和生活,应软化后使用。检验硬水常用的物质是 。
④我市不少村镇小型河沟中藻类疯长,说明水体富营养化,你认为造成该现象的原因可能有_ 。
A.化学肥料流失到河中 B.排放的生活污水中有含磷洗涤剂
C.人畜的粪便流失到河中 D.工业废水的排放
⑤爱护水资源从我做起,下列做法可行的有 。
A.洗脸、刷牙时随时关闭水龙头 B.用洗菜、洗衣的水冲厕所、拖地
C.用洗衣机洗一两件衬衫 D.用残茶水浇灌某些花卉
(2)质量守恒定律的定量研究对化学科学发展具有重大意义。
已知m1g镁条放在空气中完全燃烧,生成m2g氧化镁(不考虑其它反应),则m1 m2,其化学反应方程式为 。
小西在做该实验时,用 夹持镁条,点燃,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1>m2,其原因是 。
钠是一种非常活泼的金属,它可以和冷水直接反应生成氢气和一种碱,但它不与煤油反应.把一小块银白色的金属钠投入盛有蒸馏水的烧杯中(如图a),可以看到钠浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠和生成的氢气都发生燃烧.如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和水的界面上(如图b),同样与水发生剧烈的反应,但是不发生燃烧.则:

(1)写出钠和水反应的化学方程式 反应类型是
(2)在第二个实验中,钠也与水发生反应,但不发生燃烧,这是因为
(3)第一个实验中,钠浮在水面上;在第二个实验中,钠悬浮在煤油和水的界面上.这两个现象说明了金属钠具有的物理性质是
试题篮
()