如图是甲、乙两种固体物质的溶解度曲线。
(1)t2℃时,甲物质的溶解度为____________;
(2)从图中你还能获得哪些信息?(任填一条)______________________________________;
(3)分析t1℃时,将10g乙物质放入100g水中,充分溶
解后所得的溶液是________(填“饱和”或“不饱和”)溶液。欲使t2℃时乙物质的饱和溶液变为不饱和溶液,可采取的方法是______________(任填一种方法)。
溶液在生命活动和生产、生活中都起到十分重要的作用。
(1)将下面调味品加入水中,不能形成溶液的是 。
A.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶剂为 。(写出物质名称)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液。加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 |
a |
b |
cw |
d |
| 加入KNO3固体的质量 |
45 |
50 |
55 |
60 |
| 所得溶液的质量 |
95 |
100 |
105 |
105 |
①实验a、b、c、d中,有未被溶解的KNO3固体的实验是 (填写实验编号)。
②实验a、b、c、d所得溶液中,溶质质量分数大小关系为:a < b c d(填“<”、“>”或“=”)。
③取实验b所得溶液,若使其溶质质量分数变为20%,在不改变温度的情况下,可以采取的操作是 。
(4)向一定量澄清的石灰水中加入少量生石灰,溶液立即变浑浊,可能的原因是 。
A.原石灰水已经饱和,生石灰与水反应的产物不能继续溶解
B.生石灰与水反应放热,溶液温度升高,溶质的溶解度降低
C.空气中的二氧化碳与石灰水反应生成了难溶物质
D.生石灰与水反应消耗了水,溶剂减少,有溶质析出
某校进行中考化学实验考查,给出以下三个考题:①粗盐提纯;②二氧化碳的制取和收集;③氧气的制取和收集。考查规定由学生抽签确定考题。
I.甲同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
(1)上图中仪器A的名称是 ;甲同学抽到的考题是 (填序号);实验前甲同学发现其中缺少了一种药品,该药品是 ;写出该实验反应的化学方程式 ;
(2)若另选药品,也能完成另一个考题的气体制备,其中的化学方程式为 。
II.乙同学抽签并完成实验后,监考老师要他回答如下问题,请你帮他回答。
(3)粗盐中除混有泥沙等难溶性杂质外,通常还含有MgCl2等可溶性杂质,为了除去MgCl2.可以加入适量的试剂是 。
(4)如图是用托盘天平称量烧杯的质量时,天平平衡后的状态,错误操作是 ,烧杯的实际质量是 g。
下表为氯化钠和氯化铵在不同温度时的溶解度,回答下列问题:
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
|
溶解度 |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
|
溶解度 |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
(1)由表中数据可知,溶解度随温度变化较大的物质是。
(2)20℃时,100
水最多只能溶解
,氯化钠与氯化铵溶解度相等的温度在℃之间。
(3)向烧杯中加100
水和50.0
氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体为
。
实验室用浓盐酸(溶质质量分数为37%,密度为1.18g·mL-1)配制100g溶质质量分数为10%的稀盐酸。
(1)计算:需要浓盐酸 mL,水 mL。(结果保留小数点后一位)
(2)量取:用规格为 mL的量筒(从50mL、100 mL中选择)量取浓盐酸,倒入烧杯中,再用规格为 mL的量筒(从50mL、100 mL中选择)量取水。
(3)稀释:_ 。
0.2%~0.5%的过氧乙酸[化学式(
)]溶液是一种杀菌能力强的高效消毒剂。
(1)过氧乙酸分子中
、
、
原子的个数比为;
(2)欲配制0.4%的过氧乙酸溶液1000g,需用20%的过氧乙酸溶液克。
运用溶解度表与溶解度曲线回答下列问题:
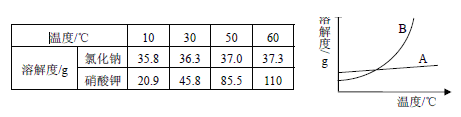
(1)氯化钠的溶解度曲线是(填"
"或"
")。
(2)
时,100
水中加入90
硝酸钾,充分溶解,所得溶液是(填"饱和"或"不饱和")溶液。当
的该溶液降温到
时,析出晶体的质量为
。
小明用一定量6%的氯化钠溶液配制50g 3%的氯化钠溶液。
(1)需要6%的氯化钠溶液的质量是 g;
(2)在配制过程中需要的主要玻璃仪器有:烧杯、量筒、胶头滴管、 ;
如图为KNO3和NaCl两种物质的溶解度曲线。
(1)两种物质的溶解度受温度的影响变化较大的是 (填KNO3或NaCl)。
(2)t1℃时,两种物质溶解度的大小关系为KNO3 NaCl。(填“>”、“=”、“<”)
(3)t2℃时,将25g KNO3固体投入50g水中,充分溶解后,所得溶液中溶质的质量分数为 。
溶液在生命活动和生产、生活中都起到十分重要的作用。
(1)将下面调味品加入水中,不能形成溶液的是 。
A.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶剂为 。(写出物质名称)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液。加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 |
a |
b |
c |
d |
| 加入KNO3固体的质量 |
45 |
50 |
55 |
60 |
| 所得溶液的质量 |
95 |
100 |
105 |
105 |
①实验a、b、c、d中,有未被溶解的KNO3固体的实验是 (填写实验编号)。
②实验a、b、c、d所得溶液中,溶质质量分数大小关系为:a<b c d(填“<”、“>”或“=”)。
③取实验b所得溶液,若使其溶质质量分数变为20%,在不改变温度的情况下,可以采取的操作是 。
(4)向一定量澄清的石灰水中加入少量生石灰,溶液立即变浑浊,可能的原因是 (2分,错选不得分、只选2项且正确得1分)。
A.原石灰水已经饱和,生石灰与水反应的产物不能继续溶解
B.生石灰与水反应放热,溶液温度升高,溶质的溶解度降低
C.空气中的二氧化碳与石灰水反应生成了难溶物质
D.生石灰与水反应消耗了水,溶剂减少,有溶质析出
(5分)下图是配制100g溶质质量分数为5%的NaCl溶液的实验操作示意图:
(1)上图中的玻璃仪器分别是广口瓶、量筒、________和玻璃棒,其中玻璃棒在此操作中的作用是______;
(2)图②中的一处错误操作是________________________;
(3)配制时应选择_____________(填10、50或100)ml的量筒量取所需要的水;
(4)用上述图示的序号表示配制溶液的操作顺序_______________。
配制50g6%的氢氧化钠溶液,有关操作如下图所示:
(1)需要氢氧化钠 g,水 mL(水的密度为1g/cm3)
(2)以上实验的正确操作顺序为 (用字母代号表示);C操作中出现的错误是 ;
(3)用pH试纸测定所配制溶液的酸碱度,操作方法为 。
请根据下列所示的实验过程和提供的数据,试回答下列问题:
(1)在滴入稀盐酸的过程中,观察到的明显现象是 .
(2)该反应过程中生成的CO2气体的质量 .
(3)求最终所得溶液中溶质的质量是多少?(请写出规范的计算过程,并且最后结果保留一位小数)
如图所示是A、B两种固体物质的溶解度曲线,根据曲线回答下列问题:
①在 ℃时,A、B两物质的溶解度相等。
②在t2℃时,将30g固体A加入50g水中,充分溶解后所得溶液的质量 g。
③在t2℃时,要使A得不饱和溶液变为饱和溶液,可采取得方法 (填一种)。
④在t2℃时,等质量的A、B两种固体物质分别加入水中,都完全溶解得到的饱和溶液质量A
B.(填 “>”,“=”,“<”)
宏观和微观相联系是化学独特的思维方式。
(1)微观探析化学反应的规律是化学科学的核心任务。根据下列微观示意图回答问题:

①从微粒的角度说明图A反应的实质是 ;
②图B所示反应中,参加反应的微粒是 (写出微粒的符号)。
(2)化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1摩尔任何物质中含有构成它的微粒个数都是6.02×10 23个,1摩尔任何物质的质量是以克为单位,数值上都等于该物质的化学式量。例如1摩尔水的各种量关系如图:

①1摩尔水中氢原子数目是 个;②1摩尔水中氧元素质量为 g。
试题篮
()