水是常用溶剂,某同学进行如图实验。
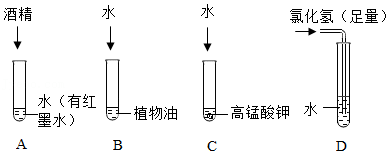
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是 。
(2)实验可知,溶质状态可以是 。
(3)实验结束后,用洗涤剂洗净B试管,原理是 。
(4)C、D试管的废液倒入废液缸中产生了黄绿色气体,查阅资料可知:2KMnO4+16HCl(浓)═2KCl+2X+5Cl2↑+8H2O,X的化学式为 。
(5)询问老师得知用2NaOH+Cl2═NaCl+NaClO+H2O可处理Cl2。根据化学方程式计算,处理0.142g Cl2至少需NaOH的质量是多少?
侯德榜成功研制了“侯氏制碱法”,打破了西方发达国家对我国制碱技术的封锁,为世界制碱工业做出了杰出贡献。某工厂为了测定用“侯氏制碱法”制得的纯碱样品中纯碱的质量分数,工厂技术员完成了如图所示的测定工作(不考虑其它因素对测定结果的影响),请根据图中数据计算:样品中纯碱的质量分数。(计算结果精确到0.1%)

戊二醛(C5H8O2)是新一代消毒剂,在防控新冠肺炎疫情的过程中被广泛使用。回答下列问题:
(1)戊二醛的相对分子质量为 。
(2)戊二醛中含碳的质量分数为 。
(3)10g戊二醛恰好完全燃烧需要 g氧气。
将12.9克NaCl和Na2CO3固体混合物完全溶于水中形成溶液,再将75克CaCl2溶液分5次加入到该溶液中,充分反应,测得的实验数据如下表。
实验序号 |
1 |
2 |
3 |
4 |
5 |
加入CaCl2溶液质量/克 |
15 |
15 |
15 |
15 |
15 |
生成沉淀的总质量/克 |
3 |
m |
9 |
10 |
10 |
求:(1)表格中m的数值是 。
(2)溶液中Na2CO3完全反应是在第 次实验。
(3)固体混合物中Na2CO3的质量分数。(精确到0.1%)
(4)请画出上述过程溶液中NaCl质量的变化图。
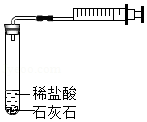
小科用如图所示的装置来测量某石灰石样品中碳酸钙的质量分数,注射器水平放置,夹持装置未画出。他在试管中加入lg石灰石样品和足量的稀盐酸(石灰石中其它成分不与稀盐酸反应产生气体),快速将连有注射器的橡皮塞塞紧试管口,实验结果如下表。(忽略活塞与筒壁之间的摩擦及温度变化对实验的影响)
反应时间/min |
0 |
1 |
2 |
3 |
4 |
活塞对应的刻度/mL |
0 |
98 |
152 |
176 |
176 |
(1)实验中判断石灰石和盐酸反应完的依据是 。
(2)当时实验条件下二氧化碳的密度约为2g/L.请利用表格中的数据,根据化学方程式计算该石灰石样品中碳酸钙的质量分数。
复方碳酸氢钠片是一种常用的抗酸剂药物,口服后能迅速中和或缓冲胃酸,减少疼痛等症状。复方碳酸氢钠片的主要成分是碳酸氢钠(与盐酸反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑)。
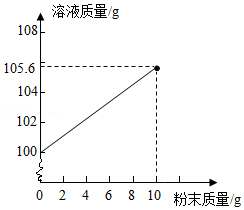
某科学兴趣小组为了测定药片中碳酸氢钠的含量做了以下实验:先将复方碳酸氢钠片制成粉末,取10克分多次放入盛有100克稀盐酸的烧杯中充分反应。测出加入的粉末质量和反应后的溶液质量,两者质量关系如图所示。
(1)实验后,兴趣小组又往烧杯中加入少量粉末,观察到 ,说明上述实验结束时稀盐酸过量。
(2)计算复方碳酸氢钠片中碳酸氢钠的含量。
(3)计算10克粉末与稀盐酸反应后所得氯化钠溶液的溶质质量分数。(计算结果精确到0.1%)
对金属材料的研究,在人类发展的历史长河中起着非常重要的作用。
(1)金属的化学性质。
完成下列反应的化学方程式:
①镁与氧气反应 。
②锌与盐酸反应 。
③铁与硫酸铜溶液反应 。
(2)金属的获得。
①金属氧化物加热分解。
加热氧化银得到银和氧气,写出该反应的化学方程式 。
②一定条件下,金属化合物与一些具有还原性的物质发生反应。在高炉内,把铁矿石冶炼成铁的主要反应原理是 。写出氢气还原氧化铜的化学方程式,并计算若80g氧化铜与氢气完全反应生成铜,理论上最多可得到铜的质量是多少?(在答题卡上写出计算过程)
③电解法冶炼。
工业上可以利用电解熔融氯化钠得到钠和氯气,该反应的基本反应类型是 。
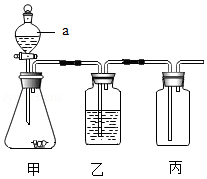
如图是初中化学常用实验装置(夹持装置已省略)。
(1)仪器a的名称是 。
(2)该装置用于实验室制取CO2:装置甲中发生反应的化学方程式为 。
(3)该装置用于实验室制取干燥的O2:乙中存放的试剂为 。检验丙中气体是否收集满的方法是 。
(4)该装置用于实验室制取干燥的H2:对装置所作的简单改动可以是 。
(5)该装置用于混合物中物质含量测定:在丙装置后连接量气装置,取10.0g黄铜(铜锌合金)粉末于锥形瓶中,加入足量稀硫酸,待完全反应后,根据气体体积换算得到生成的氢气质量为0.1g,则该混合物中铜的质量分数为多少?(写出计算过程)。
某含杂质的碳酸氢钠固体样品368g(杂质中不含钠元素且受热不分解),其中钠元素的质量分数为25%.加热一段时间,使NaHCO3部分分解,固体样品的质量变为275g。(已知:2NaHCO3 Na2CO3+CO2↑+H2O↑)试计算(写出计算过程):
(1)该固体样品中NaHCO3的质量为多少克?
(2)该固体样品中NaHCO3分解了多少克?
H2SO4是一种重要的化工原料。
(1)H2SO4溶液的pH 7(填“>”、“<”或“=”),请写出用pH试纸测定稀硫酸pH的正确方法 ;
(2)浓硫酸有吸水性,常用作某些气体的干燥剂,下列气体不能用浓硫酸干燥的是 (填写序号);
①H2
②CO2
③NH3
④HCl
(3)实验室常用亚硫酸钠固体(Na2SO3)和70%左右的硫酸溶液发生复分解反应制取SO2,请写出该反应的化学方程式: ;
(4)向160g含有H2SO4和CuSO4的混合溶液中逐滴加入NaOH溶液至过量,产生的沉淀质量与加入NaOH溶液质量的关系如图所示,请写出b点对应溶液的溶质 (填写化学式),原混合溶液中CuSO4的质量分数是 。

某实验小组的同学完成“二氧化碳的实验室制取与性质”实验活动后,测得实验产生的废液pH<6.5(已知:酸、碱废液pH在6.5~8.5之间达到排放标准)。为准确测得废液中氯化氢的质量分数,同学们取了200g废液,当加入1.48g熟石灰时,测得溶液pH=7。
(1)试计算废液中氯化氢的质量分数。
(2)实验室的这类废液不要倒入下水道,应该 (写一条)。
小文用如图所示实验测量粗锌中锌的质量分数(粗锌中的杂质既不溶于水,也不与稀硫酸反应)。试计算: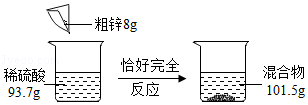
(1)生成氢气的质量;
(2)粗锌中锌的质量分数;
(3)恰好完全反应后所得溶液中溶质的质量分数。
氯气可与氢氧化钠溶液反应,其反应的化学方程式为:2NaOH+Cl 2═NaClO+NaCl+H 2O,其中生成的次氯酸钠(NaClO)易溶于水,为"84"消毒液的有效成分。现向某100g氢氧化钠溶液中通入一定量氯气,使之与氢氧化钠恰好完全反应,反应后的溶液质量为107.1g。请计算:
(1)参加反应的氯气质量为 g。
(2)反应生成次氯酸钠的质量(请写出计算过程)。
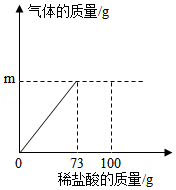
实验室用12.5g含碳酸钙80%的石灰石和一定质量的稀盐酸反应制取二氧化碳(石灰石中的杂质不溶于水,也不与稀盐酸反应),加入稀盐酸的质量与产生气体的质量关系如图所示,试计算该稀盐酸中溶质的质量分数。
试题篮
()