根据所示的实验和提供的数据、图象,回答下列问题:求:

(1)a的质量 g。
(2)b点溶液质量。(写出计算过程)
(3)恰好完全反应后所得溶液中溶质质量分数。(写出计算过程)
用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸碱度变化如图所示。请计算
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水 克。
(2)当a为80g时,所得溶液中溶质的质量分数是多少(结果精确到0.1%)?

家庭食用碱的主要成分是Na 2CO 3,为测定该食用碱中Na 2CO 3的质量分数,某同学进行了以下实验取40g食用碱,平均分为四份,然后分别加入一定质量分数的CaCl 2溶液,实验数据见下表(假设该食用碱中不含难溶性杂质且杂质均不与CaCl 2溶液产生沉淀)
| |
实验一 |
实验二 |
实验三 |
实验四 |
| 食用碱的质量 |
10g |
10g |
10g |
10g |
| 加入CaCl 2溶液的质量 |
20g |
40g |
60g |
80g |
| 生成沉淀的质量 |
3g |
m |
8g |
8g |
请分析表中数据回答并计算:
(1)m= g。
(2)40g该食用碱与足量CaCl 2溶液反应,最多生成沉淀质量为 g。
(3)该食用碱中Na 2CO 3的质量分数是多少?(写出计算过程,答案精确到0.1%)
某化学兴趣小组同学为回收一块质量为40g的铜锌合金中的铜,将该合金放入烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100g,烧杯内剩余固体27g。
请完成下列分析及计算。
(1)40g铜锌合金中锌的质量是 g。
(2)计算所用稀硫酸中溶质的质量分数。
已知:2Na 2O 2+2CO 2=2Na 2CO 3+O 2;2Na 2O 2+2H 2O=4NaOH+O 2↑.为了证明过氧化钠(Na 2O 2)固体可在呼吸面具和潜水艇中做供氧剂,某化学兴趣小组的同学利用如图所示实验装置进行探究活动。(铁架台等已略去)

(1)A装置中所发生反应的化学方程式为 。
(2)请将如图F方框中A装置的长颈漏斗和玻璃导管补画完整。
(3)D装置的作用是 。E装置中可能发生的有关反应的化学方程式为 。
(4)为了达到实验的目的, 以上装置导管接口正确的连接顺序为a接 、 接 、 接 、 接b。
(5)氧气可采用B装置收集并用带火星的木条检验,这是利用了氧气的哪些性质?
(6)实验结束后,取C装置中固体溶于水,无气泡产生。请设计实验,检验C装置中固体的成分。(简要写出实验步骤、现象和结论)。
(7)某潜水艇上有100人,如果每人每分钟消耗氧气为0.001kg,假如所需要的氧气全部由Na 2O 2与CO 2反应来提供,则该潜水艇一天所需要Na 2O 2的质量是多少?
某金属(用R表示)能与盐酸发生置换反应,其金属活动性弱于Zn,相对原子质量小于65.向一定质量的AgNO3、Cu(NO3)2和R(NO3)2混合溶液中加入Zn,充分反应后过滤,得到固体和溶液。向所得到的固体上滴加盐酸时有气泡产生。
(1)写出R与盐酸反应的化学方程式。
(2)所得到的固体中一定含有哪些金属?
(3)所得到的溶液的质量与原混合溶液的质量相比,可能增大,其原因是什么?
化学实验是科学探究的重要手段。
(1)某化学小组用图1装置制取氧气。
①A中发生反应的化学方程式为 。
②用A装置制取氧气时,长颈漏斗下端浸没在液面以下的原因是什么?
③若用B装置收集氧气,请将B装置中导管补画完整。若氧气已收集满,可观察到什么实验现象?
(2)已知甲酸(HCOOH)具有挥发性,在热的浓硫酸中分解生成一氧化碳和水。用图2微型实验装置制取CO,然后用CO还原Fe3O4,并检验气体产物。

①氢氧化钠固体的作用是 。
②写出B中Fe3O4发生反应的化学方程式。
③C中观察到的实验现象是什么?
(3)将20 g 碳酸钙加入到盛有100 g稀盐酸的烧杯中,反应后烧杯中有固体剩余物,且固体剩余物和溶液的总质量为115.6 g(气体的溶解忽略不计)。试计算反应前稀盐酸中溶质的质量分数。
向硫酸中滴加氢氧化钠溶液并不断搅拌,如图为反应时溶液pH变化的示意图。
(1)请写出该反应的化学方程式。
(2)加入NaOH溶液a mL时,溶液中含有哪些溶质?
(3)若将b mL该氢氧化钠溶液滴入到与硫酸相同质量、相同质量分数的盐酸中,请判断反应后溶液的酸碱性。

化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)某化学兴趣小组的同学利用下图微型实验装置进行探究实验。

①写出一个双球管中可能反应的化学方程式。
②挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,由此可说明燃烧需要什么条件?
③相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是 。
(2)实验室可利用如图实验装置制取纯净、干燥的CO,然后用CO还原Fe2O3并检验气体产物。已知CO发生装置中的反应为:H2C2O4 H2O+CO2↑+CO↑
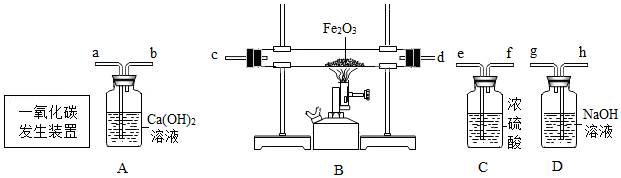
①A装置中能观察到什么现象?
②写出B装置中反应的化学方程式。
③要达到实验目的,装置中导管接口从左到右的连接顺序为: 一氧化碳发生装置接 、 接 、 接 、 接 。
④从环保角度考虑,还需对以上装置进行改进,请简述改进措施。
(3)将30.9g 氯酸钾(KClO3)和二氧化锰的固体混合物装入试管中,加热制取氧气,同时生成氯化钾。待反应完全后,将试管冷却,称量,可以得到21.3g 固体物质。请计算原固体混合物中氯酸钾的质量。
在一定质量Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中加入过量的Zn,充分反应后,过滤,可得到固体和溶液。
(1)请写出一个有关反应的化学方程式。
(2)向所得固体上滴加盐酸,能观察到什么现象。
(3)反应后所得溶液的质量与反应前溶液的质量相比,可能保持不变,为什么?
为测定某CuSO4溶液中溶质的质量分数,取150g CuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见下表。请计算:

实验1 |
实验2 |
实验3 |
|
样品质量/g |
50 |
50 |
50 |
NaOH溶液质量/g |
20 |
40 |
60 |
m/g |
42.45 |
44.9 |
44.9 |
(1)50g CuSO4溶液完全反应时,所得沉淀的质量为 g。
(2)CuSO4溶液中溶质的质量分数。
小明用某纯碱样品(含少量氯化钠)进行了图所示的实验。请计算:

(1)生成二氧化碳的总重量为 g。
(2)所用稀盐酸的溶质质量分数。
用图1所示装置制取氢气并测定稀硫酸中溶质的质量分数,将稀硫酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:

(1)共制取氢气 g;
(2)稀硫酸中溶质的质量分数。
科学家正致力于研究光催化分解水制氢气,反应方程式为2H2O 2H2↑+O2↑,用该方法制取12kg氢气至少需要分解多少千克的水?
试题篮
()