除去下列物质中所含的少量杂质,所选试剂及用量均正确的是( )
| 选项 |
物质 |
所含杂质 |
所选试剂及用量 |
| A |
碳酸钠 |
氯化钾 |
适量的水 |
| B |
盐酸 |
硫酸 |
适量氯化钡溶液 |
| C |
氧化钙 |
碳酸钙 |
过量稀盐酸 |
| D |
氯化钾溶液 |
稀盐酸 |
过量的碳酸钠溶液 |
学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑。在老师的帮助下,用金属钠来探究下列问题:
【提出问题】
1.金属钠能否置换出硫酸铜溶液中的铜?
2.金属钠能否在其他气体(如:CO2)中燃烧?
【查阅资料】金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠。金属钠还可以与水剧烈反应放出氢气。
【实验探究】
实验一:①在实验室中,金属钠保存在煤油中;
②用镊子从煤油中取出一小块金属钠,用滤纸吸干表面煤油后投入硫酸铜溶液中,观察到溶液中出现蓝色沉淀,但没有红色的物质析出;
③按照步骤②将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红。
实验二:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质。
【问题讨论】
(1)金属钠保存在煤油中的原因是: 。
(2)根据上述资料写出钠块投入水中发生反应的化学方程式: 。
(3)实验二中生成的黑色颗粒是 ,而白色物质可能是什么呢?
①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是氧化钠,乙认为是碳酸钠,丙认为是氧化钠和碳酸钠的混合物,丁认为是氢氧化钠。
我认为丁的猜想是错误的,理由是 。
②对白色物质是什么进行实验再探究,方案设计如下:
方案1:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质中一定有氧化钠。
方案2:取该样品少量于试管里,滴加足量盐酸,溶液中有气泡冒出,结论:白色物质中一定有 。
方案3:取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的 溶液(供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液),出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现。则 (在甲、乙、丙中选)的猜想成立。
③评价与反思:小娟同学认为实验方案1得出的结论不正确,其理由是 ;
【拓展应用】测定实验中使用的标有质量分数为16%的盐酸(图1)的实际质量分数。
为了测定,小明配制了20%的氢氧化钠溶液100g。然后在烧杯中加入一定量配得的氢氧化钠溶液,再逐滴加入该盐酸,恰好完全反应时测得剩余物总量为45 g。整个实验过程用pH测定仪测定滴加过程中溶液的pH。图2为测定仪打印出的滴加盐酸的质量与溶液pH的关系图。
请以此次测定的数据,列式计算该盐酸的实际质量分数?
(4)该盐酸的实际质量分数与标签上标出的质量分数不一致的可能原因 (不考虑误差)。
A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种;已知C在日常生活中常用来灭火。六种物质之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应。 回答下列问题:
(1)E与F反应的实验现象是 ________________。
(2)A与D反应的化学方程式为 ____________。
(3)B能转化成A,反应的化学方程式为 _________________。
科学兴趣小组在调查一化工厂时,发现有个车间排出的废水澄清透明,呈黄色.为测定该废水中所含的物质,他们进行如下实验(假设能发生的反应均恰好完全反应):
(1)用pH试纸测试,测得pH为2.
(2)取一定量废水溶液,加入Ba(NO3)2溶液,无现象.
(3)另取一定量废水溶液,加入AgNO3溶液后,过滤,得到白色沉淀A和滤液.
(4)向滤液中加入NaOH溶液,得到红褐色沉淀B.
由此可知:该废水溶液呈 性;所得的红褐色沉淀B为 ;废水溶液中肯定含有的盐是 .
下面图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,下表中符合图示关系的是
| |
甲 |
乙 |
丙 |
丁 |
| A |
Na2CO3 |
H2SO4 |
Ba(OH)2 |
石蕊 |
| B |
Na2CO3 |
HCl |
Ca(OH)2 |
CuSO4 |
| C |
Na2SO4 |
HCl |
Ba(OH)2 |
石蕊 |
| D |
HCl |
Na2CO3 |
Ca(OH)2 |
酚酞 |
小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与生产沉淀或气体的质量关系如图1所示;加入Na2CO3溶液的质量与溶液的pH变化关系如图2所示,下列说法中正确的是
| A.图1中b→c段表示生成气体的过程 |
| B.图1中b点的值为106 |
| C.图1中c点时,溶液中的溶质有两种 |
| D.图1中0→a段反应过程中溶液的PH变化情况可用图2中d→h段曲线表示 |
下列物质不能用酸与金属反应直接制取的物质是:
| A.FeCl3、CuCl2 | B.MgSO4、MgCl2 | C.AlCl3、Al2(SO4)3 | D.ZnSO4、ZnCl2 |
已知某固体混合物A中可能含有
、
、
、
、
五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所有发生的反应都恰好完全反应)。
I.取一定质量的该固体混合物A放入一洁净烧杯中,向其中加入适量
溶液,搅拌,待烧杯中物质充分反应后,过滤,得红褐色沉淀
和滤液
。
Ⅱ.另取一定质量的该固体混合物A放入另一洁净烧杯中,向其中加入适量
溶液,搅拌,待烧杯中物质充分反应后,过滤,得白色沉淀
和滤液
。
III.将所得滤液C和滤液E充分混合,再向混合后的溶液中加入适量
溶液,待充分反应后,过滤,得白色沉淀
和滤液
。
Ⅳ.根据上述实验过程和发生的现象做出相应推理,填写以下空白:
(1)在固体混合物A里,上述五种物质巾肯定存在的物质是(写化学式)
(2)写出步骤III中生成白色沉淀F的1个化学方程式
(3)在滤液
中,含有的金属阳离子共有种,该滤液中肯定存在的酸根离子。
(4)在混合物
里,上述五种物质中肯定不存在的物质是(写化学式)。得出此结论的理由是。
重结晶后的食盐中往往还含有少量的硫酸钠、氯化镁、氯化钙等杂质,它们在溶液中主要以SO2﹣4、Ca2+、Mg2+的形式存在,为将这些杂质除净,可向食盐溶液中加入过量的氢氧化钠、碳酸钠、氯化钡溶液,然后加入盐酸调至溶液pH=7,最后经过过滤、蒸发得到精盐.下列操作及加入溶液顺序错误的是( )
| A.BaCl2、NaOH、Na2CO3、过滤、HCl |
| B.BaCl2、Na2CO3、NaOH、过滤、HCl |
| C.NaOH、BaCl2、Na2CO3、过滤、HCl |
| D.Na2CO3、BaCl2、NaOH、过滤、HCl |
用盐酸可以清除铁锈(主要成分为Fe203),盐酸中主要含有H20分子、H+、c1﹣.某探究小组为探究稀盐酸中的哪种微粒能使氧化铁溶解,设计了如下实验方案,得出了初步结论.
(1)请填写下表中的实验结论:
| 实验过程 |
实验现象 |
实验结论 |
| 向盛有少量Fe2O3的试管中加入NaCl溶液振荡 |
固体不溶解 |
|
(2)是否需要做“向Fe2O3,中加入水”的对比实验?为什么?
为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动。
【探究活动一】检验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:__ _。
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水充分混合后静置, __ __ |
__ __ |
该样品还含有氢氧化钙 |
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数。实验装置(气密性良好)如图1所示。
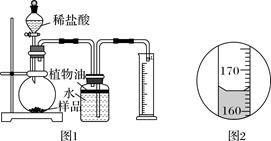
(3)将稀盐酸滴入样品中,产生气体的化学方程式为__ __,反应一段时间后,当观察到__ __(填实验现象),才停止滴加稀盐酸。
(4)实验中量筒的作用是_ _ _。
(5)实验结束后,量筒内进入水的体积如图2所示,其读数为__ __mL。已知在该实验条件下,生成气体的密度为2g·L-1,通过计算,样品中R的质量分数为__ _。
(6)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:_ _(写一个)。
如图所示,在粗玻璃管内壁上粘附湿润的石蕊试纸,向细玻璃管里滴入数滴浓醋酸后,立即封闭管口.10s后即观察到:仅有中下部的石蕊试纸从上往下逐渐变色.
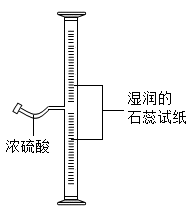
(1)本实验应选用 (填“红”或“蓝”)色石蕊试纸;
(2)本实验利用的醋酸性质包括:①酸性、② 性、③醋酸蒸气密度 (填“<”或“>”)空气密度;
(3)由实验现象可推知微粒具有的特征是 ;
(4)本实验用试剂Y代替浓醋酸也出现相似的现象,Y为 (填序号).
A.浓氨水 B.浓硫酸 C.浓盐酸.
由于二氧化碳与氢氧化钠反应无明显现象,对此同学们展开了探究,请你参与.
【提出问题】二氧化碳与氢氧化钠能否发生反应?
【查阅资料】常温下,氢氧化钠、碳酸钠在乙醇中的溶解性如下.
| 溶剂 |
乙醇 |
|
| 溶质 |
氢氧化钠 |
碳酸钠 |
| 溶解性 |
易溶 |
难溶 |
【方案设计】小明同学设计了如图所示装置进行探究。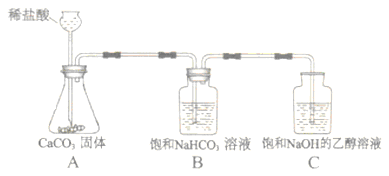
【实验探究】
(1)溶液配制.甲溶液:将一定质量的氢氧化钠固体加入到一定体积的乙醇中,用玻璃棒不断搅拌,使其成为饱和氢氧化钠的乙醇溶液.量取一定体积的乙醇要用到的仪器是,用玻璃棒搅拌的目的是。
乙溶液:将一定质量的氢氧化钠固体加入到一定体积的75%的乙醇溶液中,用玻璃棒不断搅拌,使其成为不饱和氢氧化钠的乙醇溶液.判断甲、乙溶液形成的现象是。
(2)进行实验,按图所示装置加入药品后进行实验.
中发生反应的化学方程式为,
装置的作用是,
中观察到的现象是。
【实验结论】
(3)由此小明得出二氧化碳与氢氧化钠发生了化学反应,反应的化学方程式为。
【反思交流】
(4)小刚同学认为小明的实验还足以证明二氧化碳与氢氧化钠发生了化学反应,还应补充的实验是。
(5)若将图
中甲溶液换成乙溶液进行实验,
中可能无明显现象发生,原因可能是。
下列选项符合图示从属关系的是
| |
X |
Y |
Z |
| A |
碱 |
酸 |
化合物 |
| B |
非金属单质 |
金属元素 |
元素 |
| C |
化合反应 |
氧化反应 |
化学反应 |
| D |
饱和溶液 |
不饱和溶液 |
浓溶液 |
试题篮
()