节假日或双休日,去郊游野炊实为一大快事。但野炊的过程中可能会遇到下面一些问题,你将如何处理呢?
(1)在“灶”上悬挂野炊锅时,应调节野炊锅到合适的高度.你觉得原因可能是
(2)野炊食谱如下:主食:馒头;配菜:烤火腿、鲫鱼汤、五香豆干。从营养角度来看,你可以再准备一样 (填字母序号);
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(3)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是(填字母)
A.食醋(pH<7) B.食盐水(pH=7) C.肥皂水(pH>7)
某化工厂排出的废水透明、澄清、略显蓝色。一同学取少量废水,加入过量的盐酸,有不溶于稀HNO3的白色沉淀生成。过滤,将所得滤液分成两份,一份滤液中加入少量稀H2SO4,也有不溶于稀HNO3的白色沉淀生成;另一份滤液中加入过量NaOH溶液,产生蓝色沉淀。试回答:
(1)用化学式回答:废水中加入过量的盐酸后,生成的白色沉淀是_____________。
滤液中加入过量NaOH溶液后,生成的蓝色沉淀是______________。
(2)废水中一定含有的物质是_____________(填编号):
| A.氯化物 | B.硝酸盐 | C.硫酸盐 | D.碳酸盐 |
请简述你做出选择的理由____________________。
用所学化学知识,回答下列问题:
(1)物质是由微粒构成的.构成物质的微粒保持了物质的化学性质,保持水银的化学性质的最小微粒是汞原子,保持氧气的化学性质的最小微粒是 .
(2)某金属元素原子的原子核外第四层电子层上有2个电子,则该电子失去2个电子后形成的阳离子的符号是 ,若该原子的原子核中的质子数与中子数相等,则该金属元素对应的氧化物的相对分子质量是 ;若老年人体内缺少该金属元素则可能发生 .
(3)将一定质量的Al加入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,所得滤液中一定含有的溶质是 (填化学式);铝的化学性质较活泼,但金属铝却有良好的抗腐蚀性能,原因是 ;飞机外壳用的主要材料是硬铝,硬铝属于 填序号.
①有机高分子化合物;
②合金;
③复合材料.
(4)地球是我们生存的家园,保护环境就是保护我们人类自己,而老式硫酸厂污染环境十分严重,其尾气中的二氧化硫和三氧化硫会造成酸雨,其废液中的硫酸会造成水体污染,我们可用烧碱溶液处理硫酸厂的尾气,烧碱与三氧化硫反应的化学方程式为: ;我们常用消石灰中和硫酸厂废液中的硫酸,请说出处理硫酸厂废液中的硫酸为什么用消石灰而不用烧碱的原因是 (答一点即可).
现有一包固体混合物A,其中可能含有硝酸铵、硫酸钾、硝酸铜、氯化钠四种物质中的一种或多种.现按图所示进行检验,出现的现象如图中所述(假设过程中所有发生的反应都恰好完全反应).请你依据实验过程和产生的现象做出分析与判断:
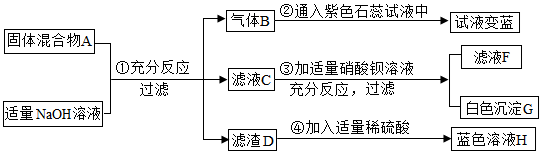
(1)气体B的化学式是 .
(2)步骤④发生反应的化学方程式 .
(3)通过上述现象判断,该固体混合物A中一定含有的物质是 ;不能确定是否含有的物质是 ,如果要证明混合物A中确实含有该物质,可用滤液F继续实验.请简要说出继续实验的操作步骤和现象 .
海洋中蕴含丰富的资源.
(1)海水淡化是解决淡水资源不足的重要方法.下列方法中,可以使海水变为淡水的是 (填字母序号).
A.滤纸过滤 B.吸附
C.沉降 D.蒸馏
(2)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和热传热介质.重水中重氢原子(D)的相对原子质量是2,则重水中氢元素的质量分数为 .
(3)从海水中制备纯碱和金属镁的流程如图所示:
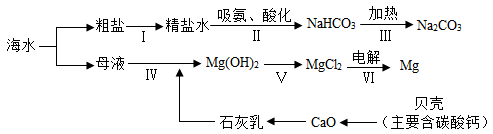
回答下列问题:
①步骤Ⅴ中所加试剂是 .
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下了物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为 (填字序号).
A.适量的盐酸
B.稍过量的Na2CO3溶液
C.稍过量的Ba(OH)2溶液
③第Ⅲ歩反应的化学方程式是 .
④在海边用贝壳作原料制生石灰,比用石灰石作原料的优点是 (写一条).
A与B有如下的反应:A+B→C+D
(1)若C为厨房内常用的调味品,A是人体胃液的主要成分,可帮助消化,则A是 ;若A、B两溶液恰好完全反应,则反应后溶液的pH 7(填“<”、“>”或“=”);写出A、B两溶液反应的化学方程式 .
(2)若B常用来改良酸性土壤;D是重要的化工原料且俗名叫苛性钠;B与CO2反应也能生成C;则A是 ,C的用途是 (只写一种).写出A溶液与B溶液反应的化学方程式
根据如图回答问题.

(1)图1锥形瓶中充满二氧化碳,将分液漏斗中的氢氧化钠溶液加入到瓶中,观察到的现象是 .
(2)配制一定质量10%的稀硫酸,若量取浓硫酸时仰视读数,得到溶液中溶质的质量分数会 (填“大于”、“小于”或“等于”)10%;图2操作中用玻璃棒搅拌的目的是 .
(3)图3实验中铜片上的白磷燃烧而红磷不燃烧,说明了可燃物燃烧满足的条件是 ;烧杯中热水的作用是 和提供热量.
海水是资源的宝库,海水淡化可获得淡水和浓海水.浓海水中主要离子的浓度如下:
| 离子 |
Na+ |
Mg2+ |
Cl﹣ |
SO42﹣ |
| 浓度/g/L |
63.7 |
28.8 |
144.6 |
46.4 |
从浓海水中提取金属镁的一段工艺流程如图所示:

(1)补全由贝壳生产石灰乳的相应转化中所需的条件或反应物:
贝壳 生石灰
生石灰 石灰乳
石灰乳
(2)写出反应1的化学方程式: .
(3)滤液X中溶质的主要成分有 (填化学式).
(4)物质Y的名称是 .
(5)将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为 g.
请从①氯化钠、②盐酸、③氮气、④氧气中,选择符合题意的物质,用序号填空.
(1)能供给呼吸的是 .
(2)能用做调味品的是 .
(3)能用于金属除锈的是 .
如图所示,在粗玻璃管内壁上粘附湿润的石蕊试纸,向细玻璃管里滴入数滴浓醋酸后,立即封闭管口.10s后即观察到:仅有中下部的石蕊试纸从上往下逐渐变色.
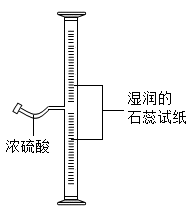
(1)本实验应选用 (填“红”或“蓝”)色石蕊试纸;
(2)本实验利用的醋酸性质包括:①酸性、② 性、③醋酸蒸气密度 (填“<”或“>”)空气密度;
(3)由实验现象可推知微粒具有的特征是 ;
(4)本实验用试剂Y代替浓醋酸也出现相似的现象,Y为 (填序号).
A.浓氨水 B.浓硫酸 C.浓盐酸.
某校举行了一次化学实验技能比赛,某参赛同学抽到的题目是:现有
、
、
、
四瓶无色溶液,它们分别是盐酸、氯化钙溶液、氢氧化钾溶液、碳酸钠溶液中的一种,要求不使用任何试剂将它们鉴别出来.该同学采用两两相互反应方法进行实验,其相互反应实验现象如下表:("↑"表示气体,"↓"表示沉淀,"﹣"表示无明显现象).
| \ |
A |
B |
C |
D |
| A |
\ |
↑ |
↓ |
﹣ |
| B |
↑ |
\ |
﹣ |
﹣ |
| C |
↓ |
﹣ |
\ |
﹣ |
| D |
﹣ |
﹣ |
﹣ |
\ |
请完成下列问题:
(1)
是,
是(填化学式)。
(2)写出
与
发生反应的化学方程式。
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 7(填“<”、“>”或“=”).
(2)当滴入溶液的体积为15mL时所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液呈 色.
(1)化学用语是最简明、国际通用的语言,请用化学符号填空。
①镁离子②2个氦原子
(2)请从下列我们熟悉的物质中选择相应物质的序号填空。
①烧碱 ②氯化钠 ③氢氧化钙 ④小苏打 ⑤石墨
A.可用于改良酸性土壤的是。
B.可用于制铅笔芯的是。
固体混合物A是由
、
、
、
、
、
中的几种混合而成为,为确定其成分,进行如图实验.(假设每步反应均恰好完全反应)

试推断:
(1)气体B是。
(2)固体A中一定没有的物质是。
(3)滤液D中一定有含有的溶质是。
(4)固体A的组成可能有种。
某化学小组向一定量
和
混合溶液中加入一定量的
粉,充分反应后过滤得溶液
和固体
.
对滤液
所含的溶质有以下几种猜想:
①
、
、
② 、
③ 、
④只有
经过讨论大家一致认为不合理的猜想是(填标号),其理由是.
【实验探究】若猜想④成立,通过以下实验可确定固体
的成分,请将下表填写完整.
| 实验步骤 |
现 象 |
固体
的成分 |
| 有气泡产生 |
试题篮
()