人类发现二氧化碳经历了多个世纪,下列是其历程中的部分资料。
资料一:1630年,海尔蒙特发现在一些洞穴处,有一种能使燃着的蜡烛熄灭的气体,后来被证实是CO 2。
资料二:1754年,布菜克将石灰石煅烧首次制得CO 2,并完成了如图1所示的物质转化研究。
资料三:1766年,卡文迪许通过实验测得,室温下1体积水大约能溶解1体积二氧化碳气体。
(1)根据海尔蒙特的发现,可推测二氧化碳的化学性质: 。
(2)写出布莱克实验中反应③的化学方程式: 。
(3)如图2,在室温下将容积为200毫升的广口瓶注满蒸馏水,通过导管a缓慢通入300毫升CO 2。如果卡文迪许的结论是正确的,则在量筒中收集到的水约为 毫升。

我国用新技术提纯了稀有金属铼(Re),为航空航天发动机核心部件的制造提供了重要原料。
(1)铼原子的相对原子质量为186,原子核内有75个质子,则其核外电子数为 。
(2)高铼酸钠(NaReO4)是铼的重要来源之一。高铼酸钠中铼元素的化合价为 。
《中国居民膳食指南》建议成人平均每天食盐摄入量应在6克以下。据调查,我国成人平均每天食盐摄入量为10.5克。
(1)高盐饮食容易引发 。
| A. |
传染病 |
B. |
遗传病 |
C. |
心血管疾病 |
(2)人体摄入食盐后,主要在 被吸收进入血被循环。
(3)某品牌低钠盐含氯化钠70%,氯化钾30%。若某人每天摄入食盐6克,现以该低钠盐代替食盐,则每天可减少多少克钠元素的摄入?(结果精确到0.1)
实验室有甲乙两瓶久置的氢氧化钠固体,某学习小组为了研究其变质情况,进行了如下实验:(电子秤示数单位为克)

(1)滴入紫色石蕊试液后溶液为红色,说明反应后溶液呈 性。
(2)上述实验中产生的二氧化碳气体质量为 克。
(3)计算甲瓶固体样品中碳酸钠的质量分数。
(4)某同学另取10克乙瓶中的固体样品,用100克15%的稀硫酸按同样方法进行实验,他认为不管固体样品变质程度如何,稀硫酸加入后,都不需要使用石蕊试液,请计算说明他做出此判断的原因。
饮食关系着人们的健康,许多人喜欢吃油炸食品,经检测,这些食品中含致癌物质﹣丙烯酰胺(C 3H 5NO)。
(1)丙烯酰胺属于 (填"无机物"或"有机物")
(2)丙烯酰胺中各元素的质量比C:H:N:O= 。
丁酸乙酯是无色有菠萝香味的液体,其密度为0.87g/cm 3,难溶于水,可与油类互溶。现取11.6g丁酸乙酯在氧气中完全燃烧,只产生26.4gCO 2和10.8gH 2O。
(1)含有丁酸乙酯的物品应远离火源。若丁酸乙酯燃烧, (填"能"或不能")用水来灭火。
(2)丁酸乙酯可与油类互溶,这种性质属于 性质。
(3)丁酸乙酯中碳元素和氢元素的质量比为 。
碳酸氢钠片是一种常用药,能用于治疗胃酸过多,这是因为人体的胃液中含有盐酸,已知:NaHCO 3+HCl═NaCl+H 2O+CO 2↑,为测定药片中碳酸氢钠的含量,小科进行了如下实验:
(1)小科认为,要测定药片中碳酸氢钠的含量,实验中需要采集两个数据:一是测出碳酸氢钠片样品的质量;二是根据碳酸氢钠与盐酸的反应原理,通过实验测出反应生成的 质量。
(2)小科按如图甲的实验方案,取药片和足量的稀盐酸进行实验,通过测量反应前后总质量的变化来采集实验数据,同学们认为,测得碳酸氢钠的质量分数会偏大,原因是 (答出一点即可)。

(3)为减小实验误差,小科又设计了如图乙的实验方案,取药片和足量的稀盐酸进行了三次实验,采集的实
验数据如表:
| 实验序号 |
1 |
2 |
3 |
| 碳酸氢钠样品质量/克 |
3.0 |
3.0 |
3.0 |
| 反应前总质量/克 |
193.8 |
194.6 |
193.6 |
| 反应后总质量/克 |
192.6 |
193.6 |
192.5 |
| 二氧化碳质量/克 |
|
|
|
请计算药片中碳酸氢钠的质量分数。
实验室有甲乙两瓶久置的氢氧化钠固体,某学习小组为了研究其变质情况,进行了如下实验:(电子秤示数单位为克)

(1)滴入紫色石蕊试液后溶液为红色,说明反应后溶液呈 性。
(2)上述实验中产生的二氧化碳气体质量为 克。
(3)计算甲瓶固体样品中碳酸钠的质量分数。
(4)某同学另取10克乙瓶中的固体样品,用100克15%的稀硫酸按同样方法进行实验,他认为不管固体样品变质程度如何,稀硫酸加入后,都不需要使用石蕊试液,请计算说明他做出此判断的原因。
大理石是含杂质的碳酸钙,因具有美丽花纹而被广泛用于建筑物外墙、内壁的贴面和地面铺设。某同学想测出大理石样品中碳酸钙的含量,进行了如下实验和分析。

(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑,杂质不参加反应),产生的气体用含有碱性物质的吸收装置充分吸收。分液漏斗中所加液体不选用硫酸,理由是 。
(2)反应前,测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为m克。实验后,根据实验数据绘制了图乙,曲线a、b分别表示锥形瓶内物质的总质量和吸收装置的总质量随反应时间变化的情况。请根据曲线b分析计算出大理石样品中碳酸钙的质量。
(3)请综合分析曲线a、b,计算出实验中所用盐酸的溶质质量分数。(结果精确到0.1%)
(4)计算后,该同学对上述实验进行了反思。他认为分液漏斗中选用的盐酸浓度偏大会对实验结果造成较大影响,其原因是 。
最近,国外研究人员发明了一种在锌原子周围聚合咪唑钠(C 3H 3N 2Na)和苯并咪唑(C 7H 6N 2)两种有机物的新型玻璃,与硅原子周围聚合各种无机物的传统玻璃相比,具有更好的透光性和延展性。
(1)硅元素与锌元素之间最根本的区别是 不同。
(2)新型玻璃具有更好的延展性,这属于物质的 (选填"物理"或"化学")性质。
(3)请列式计算咪唑钠(C 3H 3N 2Na)中碳元素的质量分数。
松材线虫病是危害松树植物的一种毁灭性流行病。病原线虫从松树的伤口进入,寄生在树脂道中,大量繁殖后遍及全株,造成水分输送受阻、蒸腾作用降低、树脂合成急剧减少。
目前,防治松材线虫主要措施是给松树"注射"一种有效成份是苦参碱的免疫激活剂。注药方法是在松树树干基部斜钻出一个小孔,在小孔上插入药剂瓶(如图),依靠树体自身的输导功能将药液运输到树体各个部位,达到防治松材线虫病的目的。
已知每瓶药剂的质量是50克,苦参碱的质量分数为0.3%.欲利用质量分数30%的苦参碱原液,配制这样的免疫激活剂50000瓶,需要原液的质量是多少?

化学反应的实质是构成物质分子的原子重新进行组合,形成新分子的过程。如图是在密闭容器中某化学反应过程的微观示意图。据图回答

(1)参加反应的"  "与"
"与" 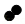 "的分子个数比为 ;
"的分子个数比为 ;
(2)该反应的基本反应类型是 。
从古代到现代,材料的种类越来越多,用途也越来越广泛。 请回答:
(1)早在西汉时期,我国就有湿法炼铜的记载,将铁置于硫酸铜溶液中得到铜单质,该反应属于 (填基本反应类型)。
(2)现代社会,玻璃是一种常见的非金属材料,SiO 2是生产玻璃的原料之一。SiO 2属于 (选填"酸"、"碱"、"盐"或"氧化物")。
(3)未来,人类在生产材料时会更注重环境保护,将二氧化碳作为原料应用于"绿色"化学可以更好地保护环境。人类每年因能源消费而向大气排放约200亿吨的CO 2,若这些 CO 2按化学方程式"CO 2+3H 2  CH 3OH+H 2O""进行反应,理论上可以转化为 亿吨甲醇[CH 3OH](结果保留一位小数)。
CH 3OH+H 2O""进行反应,理论上可以转化为 亿吨甲醇[CH 3OH](结果保留一位小数)。
某科学兴趣小组对"测定空气中氧气含量"的实验进行了改进:将数显设备、气体压强传感器和空气中氧气含量测量装置按如图连接。装置气密性良好,调节右边敞口容器和集气瓶里的水面相平,此时集气瓶内气体的体积为V 1.关闭活塞,点燃燃烧匙内的红磷,立即塞紧瓶塞,待火焰熄灭后,过一段时间打开活塞,观察到集气瓶中的水位上升。待集气瓶内的水面不再上升时,集气瓶内的气体体积为V 2. 然后向右边容器内加入一定量的水至两边水面再次相平,此时集气瓶内的气体体积为V 3.在点燃红磷至打开活塞这一过程中,观察到数显设备显示集气瓶内的气体压强先上升后下降,再趋于稳定。
请回答:
(1)数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的气压变化量 (选填"大于"、"等于"或"小于")氧气量减少导致的气压变化量。
(2)基于数显设备显示的气压变化,"过一段时间打开活塞"中的"一段时间"指的是火焰熄灭后到 所经历的时间。
(3)在整个实验过程中,集气瓶中减少的氧气体积为 (选填"V 1﹣V 2"、"V 1﹣V 3"或"V 2﹣V 3")。
试题篮
()