某同学设计的工业制备氢氧化钠的流程如图
1.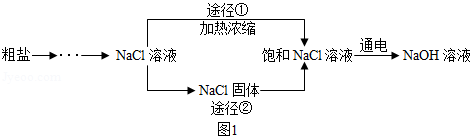
资料:2NaCl+2H2O 2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
(1)晾晒海水得到粗盐的原理是
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和______
(3)工业生产中应选择途径 (“①”或“②”),理由是
(4)Cl2可用于生产84消毒液(有效成分 NaClO),反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,反应前后氯元素的化合价有 种。
(5)图2实验测定水组成,不能加入NaCl增强水的导电性的理由是 。电解水的化学方程式为 。
(6)图3实验获得84消毒液,直流电源正极应与 (填a或b)连接,才能使 NaClO的含量更高。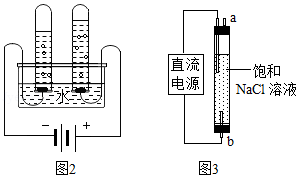
根据实验回答:
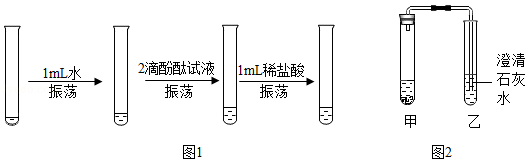
(1)图1实验,用药匙的柄把端挑起一点氢氧化钙粉末于试管中,依次进行实验。观察到现象为:
浑浊→变红→红色消失。
根据现象判断氢氧化钙的性质有 、 (物理和化学性质,各填一条)
(2)按图1实验完毕,所得溶液中除酚酞外一定有的溶质是 ,可能有的溶质是 。
(3)图2装置气密性良好。取0.5g碳酸氢钠于甲中,加入2mL盐酸, (填操作),并将导管伸入澄清石灰水中,观察到出现浑浊。乙中反应的化学方程式为 。
(4)图2中甲作为发生装置还可制得的气体是 (填一种)。
黑火药由硝酸钾、硫磺和木炭组成,爆炸时主要反应的化学反应方程式:
2KNO3+S+3C +N2↑+3CO2↑
+N2↑+3CO2↑
(1)反应涉及的物质中,属于空气主要成分的是
(2)横线上的物质由离子构成,阴离子的符号是
(3)黑火药制作的烟花燃放时,产生的空气污染物有 、 (固体和气体污染物,各填一种)
(4)硝酸钾分解的化学方程式为:2KNO3=2KNO2+O2↑.根据化学反应方程式计算,生成24g氧气需硝酸钾的质量是多少?
我国科学家屠呦呦发现并提纯抗疟疾药物青蒿素(C15H22O5)荣获2015年诺贝尔奖,请计算青蒿素中碳、氢、氧元素的质量比(直接写出结果)
请根据下列实验装置图,回答有关问题:

(1)若选择,A、D装置,连接导管口a、d可以制取某种气体,该反应的化学方程式为 。
(2)相对于B装置来说,C装置的优点是 。
(3)简述用D装置收集氧气时的验满方法: 。
根据下列实验装置或操作示意图回答问题:
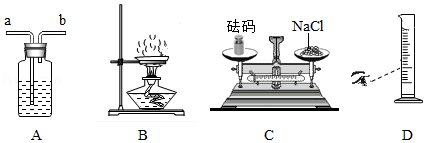
(1)用图A装置干燥O2,广口瓶内盛放的试剂是 ,气体应从 (填“a”或“b”)口进入.
(2)图B是蒸发食盐水操作,缺少的仪器是 ,组装该装置时,放置仪器的先后顺序是 (填数字序号).
①铁架台 ②铁圈 ③蒸发皿 ④酒精灯
(3)配制一定溶质质量分数的氯化钠溶液,图C中称量操作的错误之处是 .若其他操作均正确,按图D所示量取蒸馏水,则配制的氯化钠溶液浓度会 (填“偏大”“偏小”或“无影响”).
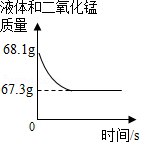
化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢质量分数。称量68g过氧化氢溶液和0.1g二氧化锰进行实验,反应前后质量随时间变化关系如图。计算:
(1)制得氧气的质量是 g。
(2)过氧化氢质量分数是多少?
实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量和反应时间关系如图。
(1)完全反应后,经过滤、烘干,得到固体的质量为 (不计操作过程中的损耗)
(2)产生气体的速度越来越慢的原因是 。
A.二氧化锰越来越少
B.过氧化氢溶液的溶质分数越来越小
C.温度越来越高
(3)计算所用过氧化氢溶液的溶质质量分数。(规范写出计算过程)

工业合成盐酸中通常溶有少量的FeCl 3.工业合成盐酸的国家质量标准规定:含HCl的质量分数<31.0%或含铁(以Fe计) 的质量分数>0.01%的产品均为不合格产品.某厂质检室对本厂生产的某一批次工业合成盐酸进行质量检验,方法是:取该批次产品l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示.请你计算产品中含HCl的质量分数和含铁(以Fe计) 的质量分数,并判断该批次产品是否合格.(写出计算过程,计算结果精确到0.1%)

施肥是农业增产的重要手段,CO(NH2)2、(NH4)2HPO4是常用的化学肥料。
回答下列问题:
(1)(NH4)2HPO4中N和H原子的个数比为 。
(2)CO(NH2)2的相对分子质量 。
(3)经农科所技术人员检测,某农户的农作物缺磷和氮。若需补充磷3.1kg和氮7.0kg,则至少需要施用 kg(NH4)2HPO4和 kg CO(NH2)2。
工业上常利用石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3的流程如下:

已知:①反应1为:6Cl2+6Ca(OH)2 Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如下:
物质 |
Ca(ClO3)2 |
CaCl2 |
KClO3 |
KCl |
溶解度/g |
209.0 |
74.5 |
7.3 |
34.0 |
回答下列问题:
(1)在实验中两次涉及过滤操作,完成此操作需要的玻璃仪器有烧杯、玻璃棒、 ,该操作中玻璃棒的作用是 .
(2)Ca(ClO3)2的名称是 .对于反应1,参加反应的Cl2中有一部分Cl的化合价升高,另一部分降低,则化合价升高的Cl与化合价降低的Cl 的个数比为 .
(3)反应2为KCl与Ca(ClO3)2发生的复分解反应,该反应能发生的主要原因是 .溶液A中含有的溶质为CaCl2和 (填化学式).
(4)上述流程中析出的KClO3晶体表面通常吸附有Ca2+、Cl﹣等杂质离子,过滤时洗涤KClO3晶体,应选用下列中的 饱和溶液(填编号).
A.KCl B.CaCl2 C.KClO3 D.Na2CO3.
小明将未经砂纸打磨的铝条放入盛有足量稀盐酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图所示.
回答下列问题:
(1)ab段发生反应的化学方程式是 .
(2)bc段发生反应的化学方程式是 .
(3)cd段压强变化的主要原因是 .

生活中处处有化学知识.回答下列问题:
(1)人们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有 作用.
(2)常用 检验水样是否属于硬水. 若为硬水,常采取 的方法降低硬度.
(3)炒菜时锅中的油起火燃烧,若向燃着的油锅里加水,不但不能灭火,还会使油滴飞溅出来燃烧更加剧烈,其原因是 .正确的方法是用锅盖盖灭,其原理是 .
根据图所示信息进行计算.

假设:稀硫酸转移完全且生成气体全部逸出.
(1)生成H2的质量为 g.
(2)反应后的溶液中溶质质量分数为多少?(写出解题过程,最后结果保留两位小数)
试题篮
()