根据如图回答问题。
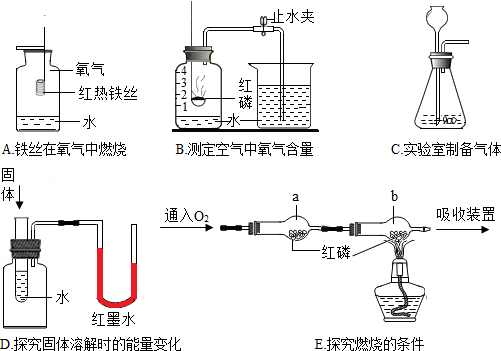
(1)A中集气瓶内水的作用是 。
(2)B中集气瓶内水位最终约在刻度 处。
(3)C中制备氧气的化学方程式是 。
(4)D中若加入的固体是NH 4NO 3,实验现象是 。
(5)E中探究可燃物燃烧的条件之一是 。
对知识的归纳和总结是学习好化学的重要方法。在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图所示),即氢氧化钙与图中四类物质能够发生化学反应。
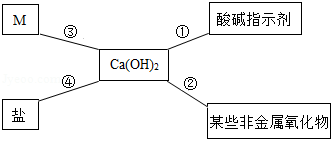
(1)图中M所属的物质类别是 。
(2)氢氧化钙可由生石灰和水反应制得,该放应能 (填"吸收"或"放出")热量。
(3)利用图中氢氧化钙能与 反应的性质,可以解释"用石灰浆粉刷墙壁,干燥后墙壁就变硬了"的现象。
(4)利用图中④氢氧化钙和盐反应的性质,除去氢氧化钠溶液中少量的氢氧化钙杂质。请写出该反应的化学方程式 。
从古至今,铁及其化合物一直被人类广泛应用。
(一)铁及其化合物的应用

(1)明代科学著作《天工开物》中记载:
①“其器冶铁锥,其尖使极刚利”,“铁锥”为开挖盐井的工具。所取盐井水“入于釜中煎炼顷刻结盐”,“金”指生铁制作的铁锅。生铁属于 材料。上述描述中利用铁的 (选填序号)。
| A. |
a.导热性 |
| B. |
b.导电性 |
| C. |
c.硬度大 |
②“泥固塞其孔,然后使水转釉”是指高温下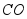 将红砖中的
将红砖中的 转化为
转化为 而形成青砖。该转化的化学方程式为 。
而形成青砖。该转化的化学方程式为 。
(2)铁的化合物在现代更多领域发挥着重要作用。
①碳酸亚铁( )不溶于水,可作补血剂,服用后与胃酸反应生成 被人体吸收,促进血红蛋白的生成。
)不溶于水,可作补血剂,服用后与胃酸反应生成 被人体吸收,促进血红蛋白的生成。
②火星探测器发回的信息表明,火星上存在 ,从而证明火星表面曾经存在过水,其理由为 。
,从而证明火星表面曾经存在过水,其理由为 。
③活性 可除去石油开采过程中的有害气体
可除去石油开采过程中的有害气体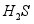 ,并获得
,并获得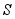 ,原理如下。
,原理如下。
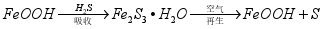
吸收中生成的另一种物质的化学式为 ,再生时发生反应的化学方程式为 。
(二) 的制备
的制备
用废铁屑(主要成分为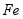 ,含少量
,含少量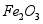 和
和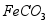 )制备
)制备 主要流程如下。
主要流程如下。
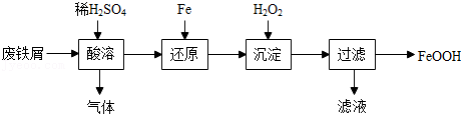
(1)酸溶时适当提高反应温度和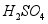 浓度,目的是 ,产生的气体为 。
浓度,目的是 ,产生的气体为 。
(2)还原发生的反应为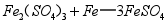 。
。
沉淀发生的反应为 。
。
沉淀时反应温度不宜太高,原因是 。
(3)沉淀时会有部分 与
与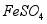 反应生成
反应生成 ,反应的化学方程式为 。
,反应的化学方程式为 。
(三) 的含量测定
的含量测定
已知: 及铁的氧化物加热分解的温度如下。
及铁的氧化物加热分解的温度如下。

称取含 的
的 样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量随温度的变化如图所示。
样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量随温度的变化如图所示。
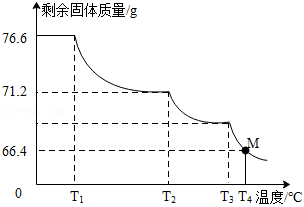
(1)样品中 的含量为 %(精确到0.1%)。
的含量为 %(精确到0.1%)。
(2)当加热到 时,M点固体的成分是 ,对应的质量比为 。
时,M点固体的成分是 ,对应的质量比为 。
通过一年的化学学习,我们学会了从微观角度认识物质。
(1)如图是部分原子的结构示意图请回答问题:
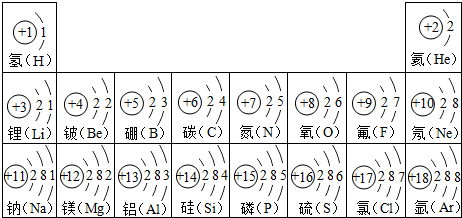
①化学上将质子数为 的所有氯原子统称为氯元素。
②8号元素和地壳中含量最多的金属元素组成的化合物中,金属元素的化合价为 。
③在化学反应中,11号元素的原子易 电子。
(2)如图是氢气在氯气中燃烧生成氯化氢的微粒示意图。
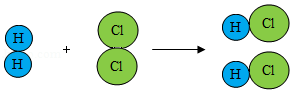
请据图回答:
①氢气可压缩储存于钢瓶中,因为受压时氢气分子之间的 减小。
②从微观的角度解释该化学变化的实质是 。
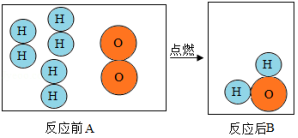
如图是氢气和氧气发生反应的微观模拟图,请回答下列问题:
(1)在B图中将相关粒子图形补充完整;
(2)A图所示物质属于 (填物质分类),从微观角度说明理由是 ;
(3)画出比氧元素多一个周期少一个族的元素的原子结构示意图 .
一班的同学在探究金属镁的化学性质时发现,将镁条放到盛有冷水的试管中,没有明显的现象,然后将试管放在酒精灯上加热,发现试管中有气泡产生。
(1)小明认为,据此现象可断定加热时镁能和水反应,小强认为小明的结论不正确,理由是 。
(2)小明向加热的试管中滴入酚酞溶液,溶液显红色,证明镁在加热时 (填“能”或“不能”)与水发生反应
(3)小明将加热后的试管放置在空气中一段时间后,同学们发现溶液中的红色消失了。
在确定酚酞溶液没有变质的情况下,请你根据初中所学化学知识,对溶液中红色消失的原因做出合理猜想。
猜想一:
猜想二:
请设计实验方案,对其中一种猜想进行验证 。(只需答出实验方案,不需要回答现象和结论)
绵阳西北部山区石灰石资源非常丰富,大量用于生产水泥。用石灰石和砂岩黏土高温煅烧得到一种新型水泥熟料,主要反应为: 。
(1)上述反应涉及四类化合物中的哪几类? 。
(2) 的化学式可表示为 ,含 44.8%的水泥熟料中含 的质量分数为 。
(3)在实验室用如图所示方法粗略测定石灰石中 的质量分数,无需测定的数据是 (填序号)。
| A. |
取用石灰石样品的质量 |
| B. |
倒入的过量稀盐酸的质量 |
| C. |
盐酸接触样品前电子秤的读数 |
| D. |
反应停止后电子秤的读数 |
(4)用含 90%的石灰石1000t生产新型水泥熟料,理论上会排放 多少吨?(无计算过程不给分)

是化学实验中常见试剂。
(1)验证质量守恒定律。
步骤1:在锥形瓶中加入适量的 溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净,将盛有 溶液的锥形瓶和铁钉一起放在托盘天平上称量,记录所称质量为 。
步骤2:将铁钉浸入到 溶液中,塞好橡胶塞。观察实验现象,待反应有明显现象后,将盛有 溶液和铁钉的锥形瓶一起放在托盘天平上称量,记录所称质量为 。
①用砂纸将铁钉打磨干净的作用是 。
②步骤2中可观察到明显的实验现象是 。该变化可说明 和 的金属活动性由强到弱的顺序是 。
③若 ,可证明参加反应的 和 的质量总和等于 。
(2)探究 溶液对 分解具有催化作用。
①若要证明 溶液对 分解具有催化作用,除需证明 在反应前后化学性质和质量不发生改变外,还需证明的是 。
②为探究 在反应前后质量是否发生改变,某同学设计如下实验:
向 溶液中滴入10g a%的 溶液,待反应完全后,向试管中加入足量的 溶液,产生沉淀,过滤、洗涤、干燥,称量沉淀物为 。
上述实验步骤中若缺少“洗涤、干燥”,则通过沉淀物 计算出溶液中 的质量 。(填“大于”或“小于”或“等于”)
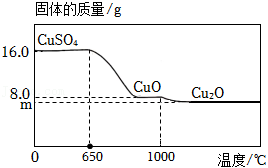
(3)将16.0g 置于坩埚中加热,固体质量与成分随温度变化的曲线如图所示。
①650℃时, 开始发生分解反应,生成 和另一种氧化物 , 的化学式为 。
②1000℃时, 开始发生分解反应,生成 和 。计算图中 的值。(写出计算过程,否则不得分)
某化学小组从理论上初步探究“已知质量比的硝酸钾和氯化钠的混合物中提纯硝酸钾”。
【分析提纯方法】
表一:常温下(20℃)溶解度和溶解性的关系
溶解度S |
S≥10g |
1g≤S<10g |
0.01g≤S<1g |
S<0.01g |
溶解性 |
易溶 |
可溶 |
微溶 |
难溶 |
表二:硝酸钾和氯化钠在不同温度时的溶解度
温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
溶解度/g |
3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
246 |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
|
3和NaCl的溶解性均为 。
3的溶解度曲线。
33在70℃时的溶解度约为 g。
【设计提纯步骤】
3和5gNaCl的混合物)
3﹣1)
(3)降温至20℃
(4)得到晶体
【设计提纯方案】
3,该小组同学结合已有知识,从理论上初步设计了以下方案;(不考虑不同溶质对溶解度的相互影响及实验过程中水和固体的损失等影响因素)
方案一 通过化学实验进行检验,取少量(4)中得到的晶体于试管中,加水配成溶液,滴加 ,观察实验现象。
3晶体的质量约为 g(精确到0.1g)与(4)中得到晶体的质量进行比较
方案三 与95%进行比较。
方案四 。

根据表中信息,请回答下列问题。
| 测试类别 S化合价 |
氢化物 |
单质 |
① |
酸 |
盐 |
| +6 |
﹣ |
﹣ |
SO 3 |
H 2SO 4 |
Na 2SO 4CuSO 4FeSO 4(NH 4) 2SO 4 |
| ② |
﹣ |
﹣ |
SO 2 |
H 2SO 3 |
Na 2SO 3 |
| 0 |
﹣ |
S |
﹣ |
|
|
| ﹣2 |
H 2S |
﹣ |
﹣ |
H 2S |
Na 2S |
(1)填写表中内容:① ;② 。
(2)物质可以按照一定规律发生转化,请按要求各写出一个对应的化学方程式。
①置换反应 ;②复分解反应 。
(3)(NH 4) 2SO 4是农业上常用的铵态氮肥,在实验室检验其为铵态氮肥的实验操作是______(写出一种即可)
(4)2H 2S+SO 2═2S+2H 2O,反应前后硫元素化合价发生的变化是
(5)在实验室中,可用热的碱液除去试管内壁上附着的硫,请完成该反应的化学方程式: S+ NaOH═ Na 2SO 3+ + H 2O。
化学变化的本质特征是有新物质生成,化学变化中的一些现象有助于我们判断物质是否发生了化学变化,
分析一:化学变化中的现象
实验内容 |
实验现象 |
实验分析 |
(1) 木炭在氧气中燃烧 |
发出白光,发出热量 |
燃烧是 的剧烈的化学反应 |
(2) |
镁表面 铜无明显变化 |
镁与稀盐酸反应,铜不与稀盐酸反应 |
(3) |
产生白色沉淀 |
该反应的化学方程式
|
(4) |
玻璃管内的固体由红棕色变为 色 |
发生了化学变化 |
22444244的混合溶液)结合已有知识,进行大胆猜想:
(1)现象及可能产生该现象的依据
(2)现象及可能产生该现象的依据 。
根据表中信息,请回答下列问题。
测试类别 S化合价 |
氢化物 |
单质 |
① |
酸 |
盐 |
+6 |
﹣ |
﹣ |
3 |
24 |
2444424 |
② |
﹣ |
﹣ |
2 |
23 |
23 |
0 |
﹣ |
S |
﹣ |
||
﹣2 |
2S |
﹣ |
﹣ |
2S |
2S |
(1)填写表中内容:① ;② 。
(2)物质可以按照一定规律发生转化,请按要求各写出一个对应的化学方程式。
①置换反应 ;②复分解反应 。
424是农业上常用的铵态氮肥,在实验室检验其为铵态氮肥的实验操作是______(写出一种即可)
222O,反应前后硫元素化合价发生的变化是
(5)在实验室中,可用热的碱液除去试管内壁上附着的硫,请完成该反应的化学方程式: S+ NaOH═ 23+ + 2O。
我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。
(1)日常生活中,适合制作电缆的金属是______(填标号)。
| A. |
金 |
B. |
铜 |
C. |
汞 |
D. |
钨 |
(2)明代《天工开物》描述了锡的冶炼方法,如图a。
①原料锡砂中的 和木炭反应得到锡和二氧化碳,化学方程式为______。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是______。
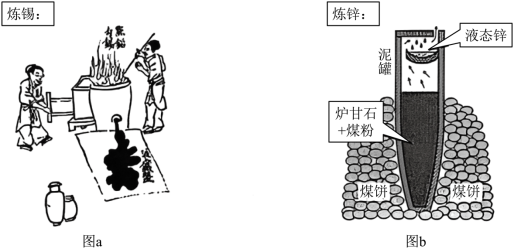
(3)图b为古代炼锌工艺原理示意图。炉甘石成分是 ,高温易分解生成 。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是______。
②已知锌的沸点为 。泥罐下部温度可达 ,上部约为 ,该工艺从反应混合物中收集液态锌的方法属于______(填标号)。
| A. |
结晶 |
B. |
蒸发 |
C. |
蒸馏 |
D. |
升华 |
③必须冷却后才能取锌,是为了防止发生反应:______(写化学方程式)。
(4)湿法冶金利用置换反应。向 混合液中加入 粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是______。
某同学以金泥(含有 等)为原料制备( )和 的流程如图所示:
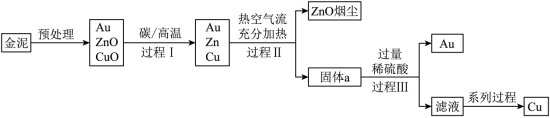
琴琴同学查阅资料已知:
①预处理的主要目的是将含硫化合物转化为氧化物。
②热空气流充分加热的目的是将 转化为氧化物,并完全分离出 烟尘。
(1)“预处理”中会产生 ,若 直接排放会导致______。
(2)“过程Ⅱ”产生的固体 中,除 外一定还有的物质是______。
(3)“过程Ⅲ”分离 的操作是______,加入过量稀硫酸的目的是______。
(4)“系列进程”中有一步是向滤液中加入过量铁粉,这一步生成气体的化学方程式为______,该反应属于______反应(填写基本反应类型)。
(5) 烟尘可用 溶液吸收,该反应生成偏锌酸钠( )和 的化学方程式为______。
试题篮
()