下列叙述正确的是( )
| A.95℃纯水的pH﹤7,说明加热可导致水呈酸性 |
| B.pH=3的醋酸溶液,稀释至10倍后pH=4 |
| C.0.2 mol/L的盐酸与等体积水混合后pH=1 |
| D.pH=3的醋酸与pH=11的氢氧化钠溶液等体积混合后pH=7 |
下列溶液中Cl-浓度最小的是
| A.200mL 2mol/L MgCl2溶液 | B.1000mL 2.5mol/L NaCl溶液 |
| C.250mL 1mol/L AlCl3溶液 | D.300mL 5mol/L KClO3溶液 |
下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.在0.1mol·L-1NaHCO3溶液中:c(Na+)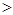 c(HCO3-) c(HCO3-)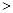 c(CO32-) c(CO32-)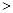 c(H2CO3) c(H2CO3) |
| B.在0.1mol·L-1Na2CO3溶液中:c(OH-)= c(HCO3-)+c(H2CO3)+ c(H+) |
| C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1mol·L-1NaOH溶液: c(CO32-)> c(HCO3-)> c(OH-)> c(H+) |
| D.常温下,CH3COONa和CH3COOH混合溶液呈中性, c(Na+)=0.1mol·L-1: |
c(Na+)= c(CH3COO-)> c(CH3COOH)> c(H+)= c(OH-)
下图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是( )
| A.盐酸的物质的量浓度为 1 mol/L |
| B.P 点时反应恰好完全中和,溶液呈中性 |
| C.曲线 a 是盐酸滴定氢氧化钠的滴定曲线 |
| D.酚酞不能用做本实验的指示剂 |
下列叙述正确的是( )
| A.水的离子积Kw随温度.外加酸(碱)浓度的改变而改变 |
| B.能自发进行的化学反应,一定是ΔH<0.ΔS>0 |
| C.当弱电解质电离成离子的速率与离子结合成分子的速率相等时达到电离平衡状态 |
| D.Ksp不仅与难溶电解质的性质和温度有关,还与溶液中的离子浓度有关 |
下列溶液中有关物质的量浓度关系和计算不正确的是
A.pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有
c(NaOH) < c(NaHCO3) < c(CH3COONa)
B.已知25℃时Ksp(AgCl)=1.8×10-10,则在0.1mol/LA1C13溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol/L
C.25℃时,0.1mol/LNa2CO3溶液中水电离出来的OH-浓度大于0.1mol/L NaOH溶液中水电离出来的OH-浓度
D.室温下,0.1mol/LNaHA溶液的pH=4,则有c(HA-)>c(H+)>c(H2A)>c(A2-)
(6分)某课外活动小组同学用如图装置进行实验,试回答下列问题。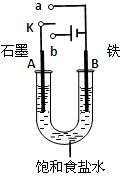
(1)若开始时开关K与b连接,则B极的电极反应式为 。
总反应的离子方程式为 。
有关上述实验,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质相同的状态(质量和浓度均相同)
④若标准状况下B极产生2.24 L气体,则电路中转移0.2 mol电子
(2)若开始时开关K与a连接,则B极的电极反应式为
。
36.5gHCl溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,NA表示阿伏加德罗常数,则下列叙述中正确的是( )
| A.所得溶液的物质的量浓度:HCl=1mol/L |
| B.所得溶液中含有NA个HCl分子 |
| C.常温下,36.5g HCl气体占有的体积一定为22.4L |
| D.所得溶液的质量分数:ω=36.5c/(1000ρ) |
已知H2A在水中存在以下平衡:H2A H++HA-,HA
H++HA-,HA H++A2-。回答以下问题:
H++A2-。回答以下问题:
(1)NaHA溶液________(填“显酸性”、“显碱性”、“显中性”或“酸碱性无法确定”),原因是_____________________________ ___。
(2)某温度下,向0.1 mol·L-1的NaHA溶液中滴入0.1 mol·L-1KOH溶液至中性,此时溶液中以下关系一定正确的是________(填字母)。
A.c(H+)·c(OH-)=1×10-14 mol2·L-2 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c (Na+)+c(K+)=0.05 mol·L-1
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)  Ca2+(aq)+A2-(aq);ΔH>0。
Ca2+(aq)+A2-(aq);ΔH>0。
①温度升高时,Ksp________(填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+)________,原因是
__________________________________________(用文字和离子方程式说明)。
(4)若向CaA悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式___________________________________________
将pH=3的盐酸和pH=11的氨水等体积混合,完全反应后,溶液中离子浓度关系正确的是 ( )
| A.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B.c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
标准状况下, VL氨气溶解在1L水中(水的密度近似为1g/cm3),所得溶液的密度为ρg/ cm3, 质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是( )
| A.ω=17c/(1000ρ) | B.c=1000Vρ/(17V+22400) |
| C.ω=17V/(17V+22400) | D.ρ=(17V+22400)/(22.4+22.4V) |
已知25℃时,下列酸的电离常数:
醋酸(CH3COOH):1.75×10-5 氢氰酸(HCN):4.93×10-10
氢氟酸(HF):7.2×10-4 甲酸(HCOOH):1.77×10-4
物质的量浓度均为0.1mol?L-1的上述溶液,酸性最强的是
| A.醋酸 | B.氢氰酸 | C.氢氟酸 | D.甲酸 |
下列各种溶液中,粒子物质的量浓度关系正确的是( )
| A.0.1mol·L-1的NH4Cl溶液与0.1mol·L-1氨水等体积混合: c(Cl-)> c(NH4+)>c(H+)>c(OH-) |
| B.0.2mol·L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C.0.1mol·L-1(NH4)2SO4溶液:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D.0.2mol·L-1NaHCO3溶液:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) |
试题篮
()