高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
| A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。下列说法不正确的是
| A.通入N2的电极发生的电极反应式为:N2+6e-+8H+=2NH4+ |
| B.反应过程中溶液的pH会变大,故需要加入盐酸 |
| C.该电池外电路电流从通入H2的电极流向通入N2的电极 |
| D.通入H2的电极为负极,A为NH4Cl |
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为
Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论正确的是
| A.Pb为正极被氧化 |
| B.溶液的pH不断减小 |
| C.放电时负极反应式是PbO2 +4H++ SO42-+2e-= PbSO4 +2H2O |
| D.溶液pH不断增大 |
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池以空气中的氧气为氧化剂,以KOH溶液为电解质溶液。下列关于该电池的叙述错误的是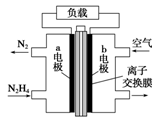
| A.b极发生还原反应 |
| B.a极的反应式为N2H4 - 4e-===N2↑+4H+ |
| C.放电时,电流从b极经过负载流向a极 |
| D.其中的离子交换膜需选用阴离子交换膜 |
用酸性氢氧燃料电池为电源电解CuSO4溶液的实验装置如下图所示。下列说法中正确的是( )
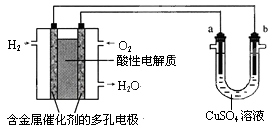
| A.燃料电池工作时,正极反应为:O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,负极反应为:Zn+2OH--—2e-==ZnO+H2O;正极反应为:Ag2O+H2O+2e-==2Ag+2OH-,根据反应式,判断下列叙述正确的是
| A.在使用过程中,电池正极区溶液的pH增大 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是正极,Ag2O是负极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为O2+2H2O+4e-===4OH- |
| C.每转移0.2 mol电子,消耗标准状况下1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
A.反应CH4+H2O 3H2+CO,每消耗1molCH4转移12mol电子 3H2+CO,每消耗1molCH4转移12mol电子 |
| B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O |
| C.电池工作时,CO32-向电极B移动 |
| D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。如图为“镁一次氯酸盐”燃料电池示意图,电极为镁合金和铂合金。关于该电池的叙述正确的是
| A.E为该燃料电池的正极 |
| B.负极发生的电极反应式为ClO—+2e—+H2O=Cl—+2OH— |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.镁燃料电池负极能发生自腐蚀产生氢气,使负极利用率降低 |
下列有相关说法不正确的是
| A.某吸热反应能自发进行,因此该反应是熵增反应 |
| B.在任何条件下,纯水都呈中性 |
| C.水的离子积常数Kw随温度、外加酸(碱)浓度的改变而改变 |
| D.铅蓄电池充电时,标有“—”的电极应与电源的负极相连 |
下列有关说法正确的是
| A.铅蓄电池放电时,正极和负极的电极质量均增大 |
| B.反应Cl2(g)+H2O(1)=HCl(aq)+HClO(aq)在常温下能自发进行,则该反应的△H>0 |
| C.加热Fe2(SO4)3溶液,Fe3+的水解程度和溶液的pH均增大 |
| D.C2H5Br水解生成乙醇(△H>0),加入少量NaOH浓溶液并加热,该化学反应速率增大其平衡常数不变 |
下列说法不正确的是
| A.多孔碳可用氢氧燃料电池的电极材料 |
| B.pH计不能用于酸碱中和滴定终点的判断 |
| C.科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通DNA链中的P元素 |
D.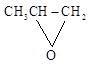 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物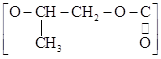 n,该反应符合绿色化学的原则 n,该反应符合绿色化学的原则 |
TESLA电动汽车的电池采用了松下提供的NCA系列(镍钴铝体系)的18650A型钴酸锂(LiCoO2)锂离子电池。电池正极材料为钴酸锂(LiCoO2),负极材料是石墨(C6)。电池反应为:
LiCoO2+C6 C6Lix+Li1-xCoO2。下列有关说法不正确的是
C6Lix+Li1-xCoO2。下列有关说法不正确的是
| A.锂离子电池与传统铅蓄电池相比,具有高比能量(比能量指的是单位重量或单位体积的能量)的特点 |
| B.废旧锂离子电池先进行“放电处理”让Li+进入石墨(C6)中而利于回收 |
| C.放电时,正极锂的化合价未发生改变 |
| D.充电时电池标有(+)的极上发生的反应为:LiCoO2—x e-=== Li1-x CoO2+xLi+ |
试题篮
()