TESLA电动汽车的电池采用了松下提供的NCA系列(镍钴铝体系)的18650A型钴酸锂(LiCoO2)锂离子电池。电池正极材料为钴酸锂(LiCoO2),负极材料是石墨(C6)。电池反应为:
LiCoO2+C6 C6Lix+Li1-xCoO2。下列有关说法不正确的是
C6Lix+Li1-xCoO2。下列有关说法不正确的是
| A.锂离子电池与传统铅蓄电池相比,具有高比能量(比能量指的是单位重量或单位体积的能量)的特点 |
| B.废旧锂离子电池先进行“放电处理”让Li+进入石墨(C6)中而利于回收 |
| C.放电时,正极锂的化合价未发生改变 |
| D.充电时电池标有(+)的极上发生的反应为:LiCoO2—x e-=== Li1-x CoO2+xLi+ |
右图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是
| A.分子组成为Cm(H2O)n的物质一定是糖类 |
| B.微生物所在电极区放电时发生还原反应 |
| C.放电过程中,H+从正极区移向负极区 |
| D.正极反应式为:MnO2+4H++2e—=Mn2++2H2O |
在下列各反应的离子方程式书写中,正确的是
| A.将Na2O2放入水中发生的反应:Na2O2+2H2O=2Na++2OH-+O2↑ |
| B.除去CuSO4溶液中的Fe3+:2 Fe3++3Cu=2Fe+3Cu2+ |
| C.在KOH溶液中,甲烷-氧气燃料电池放电时的反应:CH4+2O2+2OH-=CO32-+ 3H2O |
D.电解饱和食盐水制备H2和Cl2:2Cl-+2H+ Cl2↑+H2↑ Cl2↑+H2↑ |
近年来AIST报告正在研制一种“高容量、低成本”锂一铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O = 2Cu+2Li++2OH-,下列说法不正确的是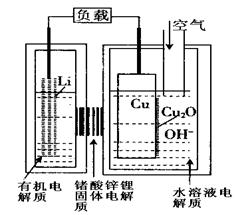
| A.放电时,Li+透过固体电解质向Cu极移动 |
| B.放电时,正极的电极反应式为Cu2O+H2O-2e-=Cu+2OH- |
| C.通空气时,铜被腐蚀,表面产生Cu2O |
| D.整个反应过程中,铜相当于催化剂 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为 CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则消耗氧气的体积2.24L |
| C.电池反应的化学方程式为:CH3CHO+O2=CH3COOH+H2O |
| D.正极上发生的反应是:O+4e-+2H2O=4OH- |
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是
| A.通入N2的电极发生的电极反应式为:N2 + 6e- + 8H+="=" 2NH4+ |
| B.反应过程中溶液的pH会变大,故需要加入盐酸 |
| C.该电池外电路电流从通入H2的电极流向通入N2的电极 |
| D.通入H2的电极为负极,A为NH4Cl |
全钒液流电池是一种新型的绿色环保储能电池。其电池总反应为:
V3++ VO2++H2O VO2++2H++V2+ 下列说法正确的是
VO2++2H++V2+ 下列说法正确的是
| A.放电时每转移2mol电子时,消耗1mol氧化剂 |
| B.放电时正极反应为:VO+2+2H++e—=VO2++H2O |
| C.放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极 |
| D.充电过程中,H+由阴极区移向阳极区迁移 |
钠离子电池具有资源广泛、价格低廉、环境友好、安全可靠的特点,特别适合于固定式大规模储能应用的需求。一种以Na2SO4水溶液为电解液的钠离子电池总反应为:NaTi2(PO4)3 +2Na2NiFeII (CN)6 Na3Ti2(PO4)3 +2NaNiFeIII(CN)6(注:其中P的化合价为+5,Fe的上标II、III代表其价态)。下列说法不正确的是
Na3Ti2(PO4)3 +2NaNiFeIII(CN)6(注:其中P的化合价为+5,Fe的上标II、III代表其价态)。下列说法不正确的是
| A.放电时NaTi2(PO4)3在正极发生还原反应 |
| B.放电时负极材料中的Na+脱离电极进入溶液,同时溶液中的Na+嵌入到正极材料中 |
| C.充电过程中阳极反应式为:2NaNiFeIII(CN)6+2Na++2e-=2Na2NiFeII (CN)6 |
| D.该电池在较长时间的使用过程中电解质溶液中Na+的浓度基本保持不变 |
NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
| A.O2在石墨Ⅱ附近发生氧化反应 |
| B.该电池放电时NO3-向石墨Ⅱ电极迁移 |
C.石墨Ⅰ附近发生的反应:3NO2 +2e- NO+ 2NO3- NO+ 2NO3- |
| D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1 |
镍镉(Ni—Cd)可充电电池在现代生活中有着广泛的应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
| A.Cd(OH)2 | B.Ni(OH)2 | C.Cd | D.NiO(OH) |
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是
| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |
一种碳纳米管能够吸附氢气,用这种材料吸氢后制备的二次电池(充放电电池)工作原理如下图所示,该电池的电解质为6 mol·L-1KOH溶液,下列说法中正确的是
| A.放电时K+移向碳电极 |
| B.放电时电池负极的电极反应为H2-2e-= 2H+ |
| C.充电时镍电极的电极反应为Ni(OH)2 + OH――e-= NiO(OH) + H2O |
| D.该电池充电时将碳电极与电源的正极相连,发生氧化反应 |
试题篮
()