常温下溶液中可发生如下反应:①16H++10Z-+2XO4-=2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-,由此判断下列说法错误的是( )
| A.反应Z2+2A2+=2A3++2Z-可以进行 |
| B.Z元素在①③反应中均被还原 |
| C.氧化性由强到弱的顺序是XO4-、Z2、B2、A3+ |
| D.还原性由强到弱顺序是A2+、B-、Z-、X2+ |
某学生做如下实验:第一步,在淀粉-KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列叙述中该同学对实验原理的解释和所得结论不正确的是
| A.氧化性:ClO->I2>SO42- |
| B.若将Na2SO3溶液加入氯水中,氯水褪色 |
| C.淀粉-KI溶液变蓝是因为I-被ClO-氧化为I2,I2遇淀粉变蓝 |
| D.蓝色消失的原因是Na2SO3溶液具有漂白性 |
常温下在下列溶液中发生如下反应:由此判断下列说法正确的是( )
①16H++10Z-+2XO4-==2X2++5Z2+8H2O ②2A2++B2===2A3++2B- ③2B-+Z2==B2+2Z-
| A.反应Z2+2A2+==2A3++2Z-不能进行 |
| B.Z元素在①③反应中均被氧化 |
| C.还原性由强到弱的顺序是A2+、B-、Z-、X2+ |
| D.氧化性由弱到强的顺序是XO4-、Z2、B2、A3+ |
已知反应:①MnO2+4HCl PbCl2+Cl2↑+2H2O, ②Cu+2Fe3+=Cu2++2Fe2+, ③Cl2+2Fe2+=2Cl-+2Fe3+。则有关物质(离子)的氧化性由强到弱的顺序为
PbCl2+Cl2↑+2H2O, ②Cu+2Fe3+=Cu2++2Fe2+, ③Cl2+2Fe2+=2Cl-+2Fe3+。则有关物质(离子)的氧化性由强到弱的顺序为
| A.Cl2>Fe3+>Cu2+>MnO2 | B.MnO2>Cl2>Fe3+>Cu2+ |
| C.Fe3+>Cu2+>MnO2>Cl2 | D.Cu2+>Fe3+>Cl2>MnO2 |
已知有如下反应:
①ClO3-+5Cl-+6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,
③2FeCl2+Cl2=2FeCl3,判断下列各微粒氧化能力由强到弱的顺序正确的是( )
| A.Cl2>ClO3->Fe3+>I2 | B.Cl2>ClO3-> I2 > Fe3+ |
| C.ClO3- > Cl2 >Fe3+>I2 | D.ClO3->Fe3+ Cl2>I2 |
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M,关于该反应的说法中不正确的是
| A.M为H2O |
| B.SnCl62-是氧化产物 |
| C.还原性:As>SnCl2 |
| D.每生成1molAs,反应中转移电子的物质的量为3mol |
已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3+6HCl=KCl+3Cl2↑+3H2O,③2KBrO3+Cl2=Br2+2KClO3,下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
| C.反应②中还原剂与氧化剂的物质的量之比为6:1 |
| D.反应③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
根据表中信息判断,下列选项正确的是( )
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4… |
| ② |
C12、FeBr2 |
FeC13、FeBr3 |
| ③ |
MnO4-… |
Cl2、Mn2+… |
A.第①组反应的其余产物为H2O
B.第②组反应中Cl2与FeBr2的物质的量之比小于或等于1:2
C.第③组反应中生成1mol Cl2,转移电子5mol
D.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色。下列判断正确的是( )
| A.上述实验证明氧化性:MnO4->Cl2>Fe3+ |
| B.上述实验中,有一个氧化还原反应 |
| C.实验①生成的气体不需要进行尾气处理 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。下列分析正确的是
| A.上述实验条件下,物质的氧化性:Cu2+ > I2 > SO2 |
| B.通入SO2时,SO2与I2反应,I2作还原剂 |
| C.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
| D.滴加KI溶液,转移2 mol e-时生成1 mol白色沉淀 |
下列实验均发生了化学反应:①将铁钉放入CuSO4溶液中;②向FeSO4溶液中滴加浓HNO3;③将铜丝放入FeCl3溶液中。下列判断中,正确的是
| A.上述实验证明了氧化性:Fe3+>Fe2+>Cu2+ |
| B.上述实验证明了Fe2+既有氧化性又有还原性 |
| C.实验①、③中的化学反应都是置换反应 |
| D.向三个实验后的溶液中加入足量NaOH溶液,最终都有Fe(OH)3生成 |
已知氧化性顺序是:Cl2>Br2>Fe3+>I2,在FeI2和FeBr2混合溶液中,通入一定量Cl2,溶液中存在的离子组不合理的是( )
| A.Fe3+ Br— Cl— | B.Fe2+ Br— Cl— |
| C.Fe2+ Cl— I— | D.Fe2+ Br— Cl— I— |
有下列反应(其中A、B、C、D各代表一种元素)其中还原性强弱顺序为 ( )
① 2A-+B2 = 2B-+A2 ② 2A-+C2 = 2C-+A2
③ 2B-+C2 = 2C-+B2 ④ 2C-+D2 = 2D-+C2
A.A-> B-> C-> D- B.D->C->B-> A- C.D-> B-> A-> C- D.A-> C->D-> B-
已知某温度时发生如下反应:①C+CO2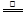 2CO;②C+H2O
2CO;②C+H2O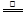 CO+H2③CO+H2O
CO+H2③CO+H2O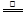 CO2+H2。由此可以判断,在该温度下,C、CO、H2的还原性强弱的顺序是( )
CO2+H2。由此可以判断,在该温度下,C、CO、H2的还原性强弱的顺序是( )
A.C>CO>H2 B.CO>C>H2 C.C>H2>CO D.CO>H2>C
试题篮
()