某次酸雨的分析数据如下:c(NH4+)=2.0×10-5 mol·L-1,c(Cl-)=6.0×10-5 mol·L-1,c(Na+)=1.9×10-5 mol·L-1,c(NO3—)=2.3×10-5 mol·L-1,c(SO42—)=2.8×10-5 mol·L-1,则此次酸雨的pH大约为
| A.3 | B.4 | C.5 | D.6 |
84消毒液的pH为10.2,可采用的适宜测定方法是 ( )
| A.使用广泛pH试纸 | B.使用精密pH试纸 |
| C.使用pH计 | D.以酚酞为指示剂进行酸碱中和滴定 |
用NaOH溶液滴定盐酸时,由于滴定速度太快,当混合溶液变红时不知NaOH是否过量,判断它是否过量的方法是
| A.加入5mL盐酸再进行滴定 | B.返滴一滴待测盐酸 |
| C.重新进行滴定 | D.以上方法均不适用 |
下列说法正确的是
| A.100℃时,pH=10的NaOH溶液与pH=2的H2SO4溶液等体积混合,则两者恰好中和,溶液的pH=7 |
| B.室温下,将pH=2的盐酸与pH=12的氨水等体积混合后,溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C.室温下,pH=3的盐酸与pH=12的NaOH溶液按体积比1:10混合后,溶液pH=7 |
| D.室温下,在pH=11的某溶液中,由水电离出的c(H+)可能为10-3mol/L或10-11mol/L |
某温度下向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中不正确的是
| A.该温度高于25℃ |
| B.由水电离出来的H+的浓度是1.0×10-10mol/L |
| C.NaHSO4晶体的加入抑制了水的电离 |
| D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性 |
下列叙述正确的是( )
| A.中和热测定实验用的小烧杯和物质的量浓度溶液配制用的容量瓶都必须干燥 |
| B.用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液终点时仰视读数,氢氧化钠浓度偏低 |
| C.配制2.0 mol·L-1的硫酸,若定容时俯视,则所得溶液浓度偏高(其他操作均正确) |
| D.用铜电极电解2.0 mol·L-1的硫酸,阴阳两极生成气体的体积之比为2∶1 |
常温下,向含有H2SO4的CuSO4溶液中逐滴加入含a mol溶质的NaOH溶液,恰好使溶液的pH=7,下列叙述错误的是( )
| A.反应后溶液中c(Na+)=2c(SO) | B.a/2 mol>沉淀的物质的量>0 |
| C.沉淀的质量为49a g | D.溶液中n(SO)=a/2 mol |
下图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述正确的是
| A.NaOH溶液的浓度为0.1 mol·L-1 |
| B.P点时可能未完全反应,溶液呈可能呈酸性 也可能呈碱性 |
| C.曲线a是盐酸滴定氢氧化钠溶液的测定曲线 |
| D.本实验的指示剂不能用甲基橙,只能用酚酞 |
室温下某强酸溶液pH=a,某强碱溶液pH=b,已知a+b=12,酸碱溶液混合后pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的正确关系为( )
| A.V(碱)=V(酸) | B.V(酸)=100V(碱) |
| C.V(碱)=100V(酸) | D.V(碱)=1000V(酸) |
水是最宝贵的资源之一。下列表述正确的是( )
| A.4℃时,纯水的pH=7 |
| B.温度升高,纯水中的c(H+) 增大,c(OH﹣)减小 |
| C.水的电离程度很小,纯水中主要存在形态是水分子 |
| D.向水中加入酸或碱,都可抑制水的电离,使水的离子积减小 |
HM和HR的溶液分别加水稀释时pH变化如下图。下列叙述中正确的是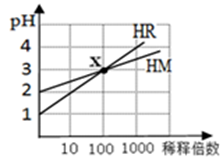
| A.HR可能是弱酸 |
| B.x点时c(R-)=c(M-) |
| C.HM是一种强酸 |
| D.稀释前,c(HR)=10c(HM) |
常温下,某未知溶液中c(H+)/c(OH-)=1×1012,且含有大量Al3+和NO3﹣,检验此溶液中是否大量存在以下6种离子:①SiO32﹣、②NH4+、③Fe2+、④Na+、⑤HCO3﹣、⑥Cl﹣,其中不必检验就能加以否定的离子是
| A.①③⑤ | B.②③④ | C.①②⑥ | D.④⑤⑥ |
室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)
| |
① |
② |
③ |
④ |
| pH |
12 |
12 |
2 |
2 |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
A.在①、②中分别加入氯化铵晶体,两溶液的pH值均增大
B.分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>②
C.把①、④两溶液等体积混合后所得溶液显酸性
D.将溶液②和溶液③等体积混合,混合后所得溶液pH=7
试题篮
()