在铝制易拉罐中收集一满罐CO2,加入过量浓NaOH 溶液,立即把口封闭。发现易拉罐“咔咔”作响,并变瘪了;过一会儿后,易拉罐又会作响并鼓起来。则下列说法错误的是
| A.导致易拉罐变瘪的反应是:CO2 + 2OH- = CO32- + H2O |
| B.导致易拉罐又鼓起来的反应是:2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑ |
| C.反应结束后,溶液中的离子浓度关系是:c(Na+) + c(H+) = c(OH-) +c(AlO2-) + c(CO32-) |
| D.如果将CO2换为NH3,浓NaOH溶液换为浓盐酸,易拉罐也会出现先瘪后鼓的现象 |
常温下,0.1mol/L HX的pH=1,0.1 mol/LCH3COOH的pH=2.9。下列说法中不正确的是
| A.HX和CH3COOH均可抑制水的电离 |
| B.将HCl与HX各0.1mol溶于水配成1L混合溶液,则溶液的c(H+)="0.2" mol/L |
| C.等物质的量浓度等体积的HX与CH3COONa两溶液混合后所得溶液中: c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| D.向等浓度等体积的HX和CH3COOH溶液中,分别加入同浓度的NaOH溶液,欲使两者pH均等于7,则消耗氢氧化钠溶液的体积前者大于后者 |
在常温下,0.1000mol·L-1Na2CO3溶液25mL 用0.1000mol·L-1盐酸滴定,其滴定曲线如图6。对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是
| A.a点:c(CO2-3)>c(HCO-3)>c(OH-) |
| B.b点:5c(Cl-)>4c(HCO-3)+4c(CO2-3) |
| C.c点:c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3) |
| D.d点:c(H+)=2c(CO2-3)+c(HCO-3)+c(OH-) |
下列有关离子的各种说法中,正确的是
| A.金属钠溶于足量水中的离子方程式:Na+2H2O=Na++H2↑+2OH- |
| B.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、Cl-可以大量共存 |
| C.等物质的量浓度、等体积的氨水与盐酸混和,溶液中离子浓度关系为 c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D.等物质的量的二元弱酸H2X与其钾盐K2X的混合溶液中c(K+)=c(H2X)+c(HX-)+c(X2-) |
25℃时,在20 mL 0.1 mol·L-1盐酸中逐滴加入0.2 mol·L-1的氨水,溶液的pH与所加氨水的体积关系如图所示,下列有关粒子浓度的关系不正确的是
| A.在b点,盐酸与氨水恰好完全中和 |
| B.在b点:c(H+)=c(OH-),c(NH4+)=c(Cl-) |
| C.在a点:c(Cl-)> c(NH4+)> c(H+)> c(OH-) |
| D.在c点:c(NH4+)+ c(NH3·H2O)="2" c(Cl-) |
常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是
| A.KHC2O4溶液呈弱碱性 |
| B.B点时:c(K+)>c(HC2O4-)>c(H+)>c(OH-) |
| C.C点时:c(HC2O4-)+c(C2O42-)+c(H2C2O4)<c(K+)< c(HC2O4-)+2c(C2O42-)+c(H2C2O4) |
| D.D点时:c(H+)+ c(HC2O4-)+ c(H2C2O4)= c(OH-) |
常温下,向20.00 mL 0.100 mol/LCH3COONa溶液中逐滴加入0.1 000 mol/L盐酸,溶液的pH与所加盐酸体积的关系如右下图所示(不考虑挥发)。下列说法正确的是

常温时,用0.1000 mol/L NaOH 滴定 25.00 mL 0.1000 mol/L某一元酸HX ,滴定过程中pH 变化曲线如图所示。下列说法正确的是
| A.滴定前,酸中c(H+) 等于碱中c(OH-) |
| B.在A点,c(Na+) > c(X-)> c(HX)> c(H+)> c(OH-) |
| C.在B点,两者恰好完全反应 |
| D.在C点,c(X-) + c(HX) ="0.05" mol/L |
25℃时,下列各项分别由等体积0.1 mol·L-1的两种溶液混合,有关混合后的溶液说法不正确的是( )
| A.Ba(OH)2溶液与Na2SO4溶液:pH="13" |
| B.醋酸与CH3COONa溶液:c(Na+)+c(H+)= c(CH3COO-)+c(OH-) |
| C.Na2CO3溶液与NaHCO3溶液:2c(Na+) = 3c(CO32-)+3c(HCO3-)+3c(H2CO3) |
| D.Na2CO3溶液与NaOH溶液: c(Na+)>c(CO32-)>c(OH-)>c(H+) |
向20mL0.5mol L
L 的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法错误的是
的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法错误的是
| A.醋酸的电离平衡常数:b点>a点 |
| B.由水电离出的c(OH-):b点>a点 |
| C.从a点到b点,混合溶液中可能存在:c(Na+)=c(CH3COO-) |
| D.b点到c点,混合溶液中一直存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
常温下,用Na2SO3溶液吸收SO2时,溶液pH随n(SO32-):n(HSO3-)变化的关系如下表:
| n(SO32-):n(HSO3-) |
91:1 |
1:1 |
9:91 |
| pH |
8.2 |
7.2 |
6.2 |
以下离子浓度关系的判断正确的是
A.NaHSO3溶液中c(H+)<c(OH-)
B.Na2SO3溶液中c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
C.当吸收液呈中性时,c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)=c(H+)
D.当吸收液呈中性时,c(Na+)= c(HSO3-)+2 c(SO32-)
某碱性溶液中只含有Na+、CH3COO-、H+、OH- 4种离子。下列描述正确的是
| A.该溶液可能由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| B.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
| C.该溶液中离子浓度一定为c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.加入一定量冰醋酸,c(CH3COO-)可能大于、等于或小于c(Na+) |
已知在相同条件下酸性强弱顺序为:CH3COOH>H2CO3>HCN>HCO3—。下列表述不正确的是
| A.25℃时,等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)>pH(CH3COONa) |
| B.a mol·L-1 HCN溶液与bmol·L-1 NaOH溶液等体积混合后,所得溶液中:c(Na+)=c(CN-),则a一定大于b |
| C.0.1mol·L-1的Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) |
D.25℃时,pH=4.75,浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液:c(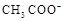 )+c( )+c(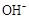 )<c(CH3COOH)+c(H+) )<c(CH3COOH)+c(H+) |
下列溶液中有关微粒的物质的量浓度关系正确的是
| A.pH=4的0.1 mol·L-1的NaHC2O4溶液中:c(HC2O4-)>c (H2C2O4)>c(C2O42-) |
| B.0.1 mol·L-1的NaHCO3溶液中:c(OH-)=c(H+)+ c(HCO3-)+2c(H2CO3) |
| C.常温下,将醋酸钠、盐酸两溶液混合呈中性的溶液中:c(Na+)>c(Cl—)=c(CH3COOH) |
| D.常温下,等物质的量浓度的三种溶液:①(NH4)2SO4②NH4Cl③(NH4)2Fe(SO4)2中c(NH4+):①<②<③ |
在0.1 mol·L-1的NaHS溶液中,下列关系式正确的是
| A.c(Na+)=c(HS-)+2c(S2-)+c(H2S) |
| B.c(HS-)=c(Na+)+c(H+)-c(OH-)-c(S2-) |
| C.c(OH-)=c(H+)+c(H2S)+c(S2-) |
| D.c(H+)=c(OH-)+c(S2-)-c(H2S) |
试题篮
()