根据下列化合物:①NaCl ②NaOH ③HCl ④NH4Cl ⑤CH3COONa ⑥CH3COOH ⑦NH3·H2O ⑧H2O,回答下列问题。
(1)NH4Cl溶液显_______性,用离子方程式表示原因 。其溶液中离子浓度大小顺序为 。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH–)=__________,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_____________。
(3)已知纯水中存在如下平衡:H2O+H2O H3O++OH– ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是____________(填字母序号)。
H3O++OH– ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是____________(填字母序号)。
| A.向水中加入NaHSO4固体 | B.向水中加Na2CO3固体 |
| C.加热至100℃[其中c(H+)=1×10–6 mol·L–1] | D.向水中加入(NH4)2SO4固体 |
(4)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m______n(填“<”、“>”或“=”)。
(5)除⑧H2O外,若其余7种溶液的物质的量浓度相同,则这7种溶液按pH由大到小的顺序为 。
(8分)取0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因是 (用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+) 0.1 mol/L NaOH溶液中由水电离出的c(H+) (填“>”、“<”或“=”)。
(3)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH 7(填“>”、“<”或“=”)。
(4)有相同温度下相同浓度的四种盐溶液:
| A.NH4HCO3; | B.NH4A; | C.(NH4)2SO4; | D.NH4Cl,按pH由大到小的顺序排列(填序号)。 |
I.25℃时,三种酸的电离常数为:
| 化学式 |
CH3COOH |
H2CO3 |
HClO |
| 电离平衡常数 |
1.8×10-5 |
K1=4.3×10-7 K2=5.6×10-11 |
3.0×10-8 |
请回答下列问题:
(1)物质的量浓度为0.1mol/L的下列物质:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3;pH由大到小的顺序是: ;(填编号)
(2)常温下将0.1mol/L的CH3COOH溶液加蒸馏水稀释,在稀释过程中,下列表达式的数据变大的是: ;
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-) D.c(OH-)/c(H+)
Ⅱ.在一个容积固定不变的密闭容器中进行反应2X(g)+Y(g)  2Z(g),已知将2molX,1molY充入该容器中反应在绝热条件下达到平衡时,Z的物质的量为pmol。回答问题:
2Z(g),已知将2molX,1molY充入该容器中反应在绝热条件下达到平衡时,Z的物质的量为pmol。回答问题:
若把2molX,1molY充入该容器时处于状态I,达到平衡时处于状态Ⅱ,
则该反应的焓变△H 0(填“〉” “〈”或“=”,下同〉,熵变△S 0,该反应在 (填“高温”、“低温”)条件下能自发进行。
Ⅲ. 在容积可变的密闭容器中发生可逆反应 m A(g) + n B(g)  pC(g) ,在一定温度和不同压强下达到平衡,分别得到A的物质的量浓度如表:
pC(g) ,在一定温度和不同压强下达到平衡,分别得到A的物质的量浓度如表:
| 压强p(Pa) |
2x105 |
5x105 |
1x106 |
| c(A)mol/L |
0.08 |
0.20 |
0.44 |
当压强从2x105Pa增加到5x105Pa时,平衡 (填“向左”、“向右”或“不”)移动。维持压强2x105Pa,反应达到平衡时,体系共amol气体,再向体系充入bmolB气体,重新达到平衡时,体系中气体总的物质的量为 。当压强从5x105Pa增加到1x106 Pa时,平衡 (填“向左”、“向右”或“不”)移动,原因是 。
有X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下图所示变化: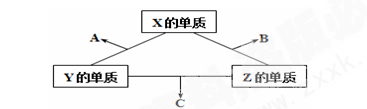
已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数的少1个。
请回答下列问题:
(1)X元素在周期表中的位置是 。
(2)用X的单质与Z的单质可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入 (填物质名称);负极的电极反应式为 。
(3)C与X的单质反应生成A的化学方程式为 。
(4)X、Y、Z三种元素可组成一种强酸W,C与W完全反应生成一种盐。该盐的水溶液pH 7(填“>”、“=”或“<”),原因是 (用离子方程式表示)。
(5)已知Y的单质与Z的单质生成C的反应是可逆反应,ΔH<0。将3molY单质、5molZ单质充入体积为2L的密闭容器中,平衡后C的浓度为1 mol·L-1。下列说法中正确的是 。(填写代号)
a.Y单质、Z单质与C三者化学反应速率之比为1:3:2时,达到化学平衡
b.达到化学平衡时,Y、Z的物质的量之比为1:1
c.该反应的化学平衡常数为1 L2·mol-2
d.达到化学平衡后,再升高温度,C的体积分数增大
(6)已知:① Y2(g)+2X2(g) ==2YX2(g) △H= +67.7 kJ•mol-1。
② Y2Z4(g)+X2(g) ="=" Y2(g) +2Z2X (g) △H=-534kJ•mol-1。
则2Y2Z4(g)+ 2YX2(g) === 3Y2(g) + 4Z2X (g) △H = kJ•mol-1。
(12分)现有常温条件下甲、乙、丙三种溶液,甲为0.1mol·L-1的NaOH溶液,乙为0.1mol·L-1的盐酸,丙为未知浓度的FeCl2溶液,试回答下列问题:
(1)甲溶液的pH= 。
(2)丙溶液中存在的化学平衡有 (用离子方程式表示)。
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为 。
(4)某化学兴趣小组认为在隔绝空气的环境中,用酸性KMnO4溶液能测定丙溶液的浓度(已知:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、钥匙、玻璃棒、烧杯、量筒外,还需 (填写仪器名称)。
②滴定实验要用到酸式滴定管或碱式滴定管,使用该仪器的第一步操作是
。
③某同学设计的下列滴定方式中,最合理的是 (夹持部分略去,填字母序号),达到滴定终点的现象是 。
25 ℃时,电离平衡常数:
| 化学式 |
CH3COOH |
H2CO3 |
HClO |
| 电离平衡常数 |
1.8×10-5 |
K1:4.3×10-7 K2:5.6×10-11 |
3.2×10-8 |
回答下列问题:
(1)物质的量浓度为0.1 mol·L-1的下列四种物质:
a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,pH由大到小的顺序是___; (填编号)
(2)常温下0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变大的是________;
A.c(H+) B. C.c(H+)·c(OH-) D.
C.c(H+)·c(OH-) D.
(3)写出次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25 ℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=________________。(填准确数值)
(5)25℃时,将amol·L-1的醋酸与bmol·L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为 。
(1)常温时向水中加入少量固体MgCl2, ______(填“促进”或“抑制”)了水的电离;与纯水相比,所得溶液中KW (填“变大”、“变小”或“不变”)。
(2)已知某溶液中只存在OH-、H+、NH 、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
A.c(Cl-)>c(NH )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
B.c(Cl-)>c(NH )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
C.c(NH )>c(Cl-)>c(OH-)>c(H+) )>c(Cl-)>c(OH-)>c(H+) |
D.c(Cl-)>c(H+)>c(NH )>c(OH-) )>c(OH-) |
①上述关系一定不正确的是__________(填序号)。
②若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为______________(填序号)。
③若四种离子浓度关系有c(NH )=c(Cl-),则该溶液显__ __(填“酸性”、“碱性”或“中性”)。
)=c(Cl-),则该溶液显__ __(填“酸性”、“碱性”或“中性”)。
(12 分)常温下有浓度均为0.5mol/L的四种溶液:①Na2CO3溶液 ②NaHCO3溶液 ③HCl ④NH3·H2O。请根据题目要求回答下列问题:
(1)上述溶液中,可发生水解反应的 (填序号,下同),在发生水解反应的溶液中pH最大的是 。
(2)上述溶液中,既能与氢氧化钠溶液反应,又能与硫酸溶液反应的溶液中离子浓度由大到小的顺序为 。
(3)取适量溶液④,加入少量氯化铵固体,此时溶液中c(NH4+)/ c(OH-)的值 (填
"增大"或"减小"或"不变")
(4)将等体积的③和④的溶液混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填"大于"或"小于"或"等于"),此时溶液中离子浓度由大到小的顺序是 。
(5)取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出的c(H+)= mol/L。
某校化学研究性学习小组查阅资料了解到以下内容:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为___________________________________。
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有_____________(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:
____ MnO4– + ____ H2C2O4 + ____ H+ =" ____" Mn2+ + ____ CO2↑ + ____ H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(注:忽略草酸的升华,且夹持装置未标出):
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末有黑色变为红色。据此回答:
上述装置中,D的作用是__________________.
乙二酸分解的化学方程式为______________________________________.
(4)该小组同学将2.52 g草酸晶体(H2C2O4·2H2O)加入到100 mL 0.2 mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性(忽略溶液体积变化)。则下列关系合理的是
A.c(Na+)+c(H+)=c(HC2O4—)+c(OH—)+c(C2O42-)
B.c(HC2O4-)+c(C2O42-)="0.2" mol·L-1
C. c(HC2O4-)>c(C2O42—)>c(H2C2O4)
D.c(Na+)=c(H2C2O4)+c(HC2O4-)+c(C2O42—)
【化学—选修2化学与技术】
某电镀铜厂有两种废水需要处理,一种废水中含有CN-离子,另一种废水中含有Cr2O72-离子。该厂拟定如图所示的废水处理流程。
回答以下问题:
(1)上述处理废水的流程中主要使用的方法是_________________________________
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因_____________________。
(3)②中反应后无气体放出,该反应的离子方程式为____________________________。
(4)③中反应时,每0.4 mol Cr2O72-转移2.4 mol的电子,该反应的离子方程式为______________。
(5)取少量待检水样于试管中,先加入NaOH溶液,观察到有蓝色沉淀生成,继续加入NaOH溶液,直到不再产生蓝色沉淀为止,再加入Na2S溶液,有黑色沉淀生成,且蓝色沉淀逐渐减少,请你使用化学用语,结合必要的文字解释其原因
用化学术语回答下列问题:
(1)书写电离方程式:氢氟酸 ;
(2)书写水解离子方程式:硫酸铝 ;
(3)电解硝酸银溶液电极反应式(惰性电极)①阳极: ;②阴极: .
CuSO4溶液是中学化学及工农业生产中常见的一种试剂.
(1)某同学配制CuSO4溶液时,需加入一定量的硫酸溶液,用离子方程式说明其原因是 .
(2)该同学利用制得的CuSO4溶液,进行以下实验探究.
①图一是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池.电解质溶液甲是 (填“ZnSO4”或“CuSO4”)溶液;Cu极的电极反应式是 .
②图二中,I是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在II中实现铁上镀铜,则b处通入的是 (填“CH4”或“O2”),a处电极上发生的电极反应式是 .若把II中电极均换为惰性电极,电解时的化学反应方程式为 .若把II中电极均换为惰性电极,电解液换为含有0.04molCuSO4和0.04molNaCl的混合溶液400mL,当阳极产生的气体为672mL(标准状况下)时,溶液的pH= (假设电解后溶液体积不变).
(3)将蓝矾(CuSO4•5H2O)、生石灰和水按一定比例混合,即可得到波尔多液(杀菌剂),其有效成分为难溶的碱式硫酸铜[xCuSO4•yCu(OH)2].为测定某碱式硫酸铜的组成进行了如下实验:取等质量的碱式硫酸铜样品两份,一份滴加稀盐酸至恰好完全溶解,另一份高温灼烧后只得到CuO固体.所得数据显示n(HCl):n(CuO)=3:2,则该碱式硫酸铜的化学式中x:y= .
物质在水溶液中存在的电离平衡、水解平衡和沉淀溶解平衡,都可看作化学平衡。请根据所学知识回答:
(1)在0.1mo1·L-1的NaHSO3溶液中存在的各种平衡体系为(用离子方程式表示):
、 、
已知该溶液中有关微粒浓度由大到小的顺序为:c(Na+)>c(HSO )>c(SO
)>c(SO )>c(H2SO3)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由:____________________________.
)>c(H2SO3)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由:____________________________.
(2)常温下,某水溶液中存在的离子有:Na+、A—、H+、OH—,若该溶液由0.1mo1.L-1的HA溶液和0.1mol.L-1的NaOH溶液等体积混合而得,则溶液的pH _________(填“大于”、“小于”或“等于”)7,理由是 。
已知某溶液中只存在OH-.H+.NH4+.Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种,请回答后面问题:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)上述关系一定不正确的是 (填序号)
(2)若溶液中只有一种溶质,则该溶质为 ,该溶液中离子浓度的大小关系为 (填序号)
(3)若关系③正确,则溶液中溶质为 。
(4)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显 (填“酸性”、“碱性”、“中性”)。
(5)25℃,pH="a" 的盐酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则Va Vb(填>、<、=、无法确定)
(1)NO2有较强的氧化性,能将SO2氧化生成SO3,本身被还原为NO,已知下列两反应过程中能量变化如图所示:
则NO2氧化SO2的热化学方程式为_________________________________。
(2)在2L密闭容器中放入1mol氨气,在一定温度进行如下反应:2NH3(g) N2(g)+3H2(g),
N2(g)+3H2(g),
反应时间(t)与容器内气体总压强(p)的数据见下表
| 时间t/min |
0 |
1 |
2 |
3 |
4 |
5 |
| 总压强p 100 kPa |
5 |
5.6 |
6.4 |
6.8 |
7 |
7 |
则平衡时氨气的转化率为___________。
(3)25℃,某二元弱酸H2A与NaOH溶液反应可生成NaHA、Na2A,溶液中含A各微粒的分布分数(平衡时某含A微粒的浓度占各含A微粒浓度之和的分数)随溶液变化的情况如下图所示:
已知:103.04=1.1×103,104.37=2.3×104 25℃,Ka1(H2CO3)= 4.4×10-7 Ka2(H2CO3) = 4.7×10-11
①若向0.1NaHAmol·L-1溶液中加入少量NaOH溶液,c(A2-)/c(HA-)的值 (填“增大”、“减小”或“不变”,下同),c(H+)/c(OH-) 的值 。
②若向0.1NaHAmol·L-1溶液中加入氨水至溶液呈中性,则c(H2A)+c(NH4+) c(A2-) (填“大于”、“小于”或“等于”)。
③计算HA-二级电离平衡常数Ka2= 。
④将过量H2A加入Na2CO3溶液中反应的离子方程式为: 。
试题篮
()