某浅绿色晶体X[x(NH4)2SO4·yFeSO4·zH2O]在分析化学上常用作还原剂。为确定其组成,某小组同学进行如下实验。
I.NH4+的测定
采用蒸馏法,蒸馏装置如图所示,实验步骤如下: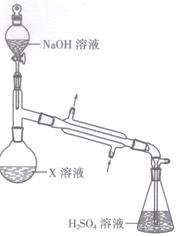
①准确称取19.60 g晶体X,加水溶解,注入圆底烧瓶中;
②准确量取50.00 mL l.0100 mol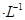 H2SO4溶液于锥形瓶中;
H2SO4溶液于锥形瓶中;
③向圆底烧瓶中加入足量NaOH溶液,加热蒸馏;
④用0.0400 mol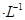 NaOH标准溶液滴定锥形瓶中过剩的酸,到终点时消耗NaOH标准溶液25.00 mL。
NaOH标准溶液滴定锥形瓶中过剩的酸,到终点时消耗NaOH标准溶液25.00 mL。
(1)步骤②中,准确量取H2SO4溶液所用的玻璃仪器为________.
(2)步骤③中,加热蒸馏时间需长达30分钟,其目的为________.
(3)步骤④中,若滴定前滴定管尖嘴有气泡,滴定后气泡消失,则所测n(NH4+)的值将________(填“偏大”、“偏小”或“不变”)。
Ⅱ.SO42-的测定
采用重量分析法,实验步骤如下:
①另准确称取19.60 g晶体X于烧杯中,加水溶解,边搅拌边加入过量的 BaCl2溶液;
②用无灰滤纸(灰分质量很小,可忽略)过滤,洗涤沉淀3~4次;
③用滤纸包裹好沉淀取出,灼烧滤纸包至滤纸完全灰化;
④继续灼烧沉淀至恒重.得沉淀质量23.30 g。
(4)步骤①中,判断 BaCl2溶液已过量的实验操作和现象是________。
(5)步骤②中,所用洗涤剂最合适的是________(填选项字母)。
A.冷水 B.稀硫酸 C.滤液
(6)步骤③灼烧操作中,除三脚架外,还需要用到下列仪器中的____(填选项字母)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.蒸发皿
F.酒精灯
(7)综合实验I、Ⅱ,通过计算得出晶体X的化学式为________。
(12分)亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组拟制备NaNO2并测定产品纯度。
I【查阅资料】
①2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。
②NO能被酸性高锰酸钾氧化成NO2。
③酸性条件下MnO4-被还原为Mn2+。
Ⅱ【制备产品】
用如下装置制NaNO2(夹持和加热装置已省略)。
(1)装置A烧瓶中发生反应的化学方程式为_______________________。
(2)B装置的作用是_________________________。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为排除干扰应在B、C装置间增加装置E,E中盛放的试剂可能是_________。(填字母编号)
A.浓H2SO4 B.碱石灰 C.无水CaCl2 D.生石灰
Ⅲ【测定纯度】.
设计如下方案测定产品的纯度。
(4)溶液A到溶液B发生反应的离子方程式为____________________________。
(5)取样品2.3g经一系列操作后得到溶液A100mL,准确量取10.00mL A与24.00mL 0.05mol/L的酸性KMnO4溶液在锥形瓶中充分反应。反应后溶液用0.1 mol/L(NH4)2Fe(SO4)2标准溶液滴定至紫色刚好褪去;重复上述实验2次,平均消耗(NH4)2 Fe(SO4)2溶液10.00ml,则样品中NaNO2的纯度为__________。
Ⅳ【探究反思】
(6)NaNO2的纯度偏低,该小组讨论提出的原因中可能正确的是________。(填字母编号)
A.滴定至溶液紫色刚好褪去就立刻停止滴加
B.加入A与KMnO4溶液前锥形瓶未经干燥
C.实验中使用的(NH4)2 Fe(SO4)2溶液暴露在空气中时间过长
某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置

请回答下列问题:
(1)装置F中发生反应的化学方程式为_________________________;
(2)B装置的名称是_____________________;
(3)E装置的作用_______________________;
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应 的化学方程式:___________________________;
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?(用离子方程式表示)______________________________.
(6)实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:(要求有计算过程)
①质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为多少?
②若要制取Cl2 2.24L(标准状况),理论上需要消耗MnO2多少克?
某化学兴趣小组用下图所示装置进行实验,探究硝酸与铁反应的产物。
查阅资料得知:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、﹣3价等氮的化合物。
II.常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4的晶体存在。
请回答下列问题:
(1)装置中各仪器装入试剂后,接下来由先至后的操作顺序为 。
| A.通入N2 | B.滴入浓HNO3 | C.打开活塞K1 | D.关闭活塞K1 |
(2)装置A中,滴入浓硝酸加热前没有明显现象的原因是 。
(3)反应结束后,打开装置D中的活塞K2,并通入氧气,铁完全溶解于浓硝酸后生成的NO2气体中含有NO的现象为 。
装置D中发生的反应的化学方程式为 。
(4)C装置的作用是 。
(5)反应停止后,装置A中无固体剩余。证明装置A的溶液中是否含有Fe2+,选择的药品是 (填序号)。
a.铁粉 b.氯水 c.KMnO4溶液 d.硫氰化钾溶液
(6)检验是否生成﹣3价氮的化合物,应进行的实验操作、现象及结论是 。
(16分)甲、乙、丙三位同学在实验室用不同方法制取氮气。
(1)甲同学让空气通过右图所示装置,以除去氧气制得氮气。硬质玻璃管中所盛固体可选用 (填下列选项标号)
A.铁粉 B.碳粉 C.过氧化钠 D.碱石灰
(2)收集氮气可选用 (填下列选项标号)
(3)乙同学设计用氨气和炽热的氧化铜反应制取氮气,反应方程式为 。
(4)制取氨气可选用 (填下列选项标号)
A.加热硫酸铵与氢氧化钙混合物
B.加热分解氯化铵晶体
C.浓氨水滴入氢氧化钠固体
D.加热浓氨水使氨气化
(5)丙同学用加热两种含氮溶液制氮气:NaNO2+NH4Cl  NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
该实验装置需要 、分液漏斗、酒精灯等玻璃仪器。
(6)氮气助燃金属镁,反应方程式 ;燃烧3.6 g镁将消耗标准状况下氮气 mL.
某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2
于是提出猜想,NO2和碱性的NaHCO3溶液也能发生类似反应。该小组利用如图所示装置,使NO2和NaHCO3溶液充分反应后,获得溶液X。

(1)Cu与浓硝酸反应的现象是_______________________。
(2)该小组同学为了对猜想进行探究,进行如下讨论和实验。
①甲同学认为,可通过检验X中是否存在NO3—的方法验证猜想。但经讨论后认为不可行,你认为其原因是 。
②乙同学在X中加入少量K2Cr2O7溶液,结果溶液褪色,则证明X中含有NaNO2。根据以上信息,写出NO2与NaHCO3溶液反应的离子方程式_________________ 。
(3)已知在酸性条件下NO2— 能将I— 氧化为I2。你认为能否用KI淀粉溶液检验X中存在NaNO2: ___________(填“能”或“不能”),原因是____________________________。
(4)已知5NO2— + 2MnO4—+6H+= 5NO3—+ 2Mn2+ +3H2O。称取a g KMnO4固体,加蒸馏水和少量稀硫酸溶解,配成250 mL溶液。移取20.00mL X于锥形瓶,用所配的酸性KMnO4溶液进行滴定,消耗b mL KMnO4溶液。滴点终点的现象是 ,则X中NaNO2的浓度是______________(用含a、b的式子表示)。
某化学学习小组发现在碱性溶液中,NO2会发生如下反应: 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2
于是提出猜想,NO2和碱性的NaHCO3溶液也能发生类似反应。该小组利用如图所示装置,使NO2和NaHCO3溶液充分反应并获得反应液X。
(1)①NaHCO3溶液呈碱性的原因是 。
②Cu与浓硝酸反应的现象是 。
③欲从反应后的溶液中得到硝酸铜晶体,操作步骤是:蒸发浓缩、 、过滤。
(2)该小组同学为了对猜想进行探究,进行如下讨论和实验。
④甲同学认为,可通过检验X中是否存在NO3-的方法验证猜想。但经讨论后认为不可行,你认为其原因是 。
⑤乙同学在X中加入少量K2Cr2O7溶液,结果溶液褪色,则产物中含有NaNO2。根据以上信息,写出NO2与NaHCO3溶液反应的离子方程式 。
⑥已知在酸性条件下NO2-能将I-氧化为I2。你认为能否用KI淀粉溶液检验X中是否存在NaNO2:_______(填“能”或“不能”),原因是 。
⑦已知5NO2-+ 2MnO4-+6H+= 5NO3-+ 2Mn2+ +3H2O。称取a gKMnO4固体,加蒸馏水和少量稀硫酸溶解,配成250mL溶液。移取20.00mL X于锥形瓶,用所配的酸性KMnO4溶液进行滴定,消耗b mL KMnO4溶液。滴点终点的现象是 ,则X中NaNO2的浓度是 (用含a、b的式子表示)。
化学是一门以实验为基础的学科,试回答以下问题。
(1)实验室中制取并收集少量氨气,可选用上述_____(填装置序号)装置,氨气应从收集装置的_____(填字母序号)导管进气。
(2)选用装置乙、丙、戊制备、收集一氧化氮气体,乙中塑料板上若放置石灰石,戊中盛满稀NaOH溶液,正确的连接顺序为___________________(用接口字母表示),装置乙的作用是____________,丙中产生NO的离子方程式为______________________。
(3)二氧化氯(C1O2)是一种常用高效消毒剂,某研究小组利用丁装置制备C1O2。
①在烧瓶中放入KClO3和草酸(H2C2O4),然后加入足量的稀硫酸,水浴加热。反应生成ClO2、CO2和K2SO4,则该反应中氧化产物与还原产物物质的量之比为_________。
②温度过高时,二氧化氯的水溶液有可能发生爆炸。在反应开始前将烧杯中的水加热到80%,然后停止加热,并使其保持在60℃~80℃之间,丁装置中缺少的一种必需的玻璃仪器名称是____________。
③将二氧化氯溶液加入到硫化氢溶液中,然后加入少量的稀盐酸酸化过的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式________________。
亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒。某学习小组针对亚硝酸钠设计了如下实验:
【实验一】制取NaNO2
该小组先查阅资料知:①2NO+Na2O2 →2NaNO2;2NO2+Na2O2 →2NaNO3;②NO能被酸性高锰酸钾氧化为NO3-,然后设计制取装置如下图(夹持装置略去):
36.装置D的作用是 ;如果没有B装置,C中发生的副反应有 。
37.就算在装置气密性良好的情况下进行实验,该小组发现制得的NaNO2的纯度也不高,可能的原因是 ;设计一种提高NaNO2纯度的改进措施 。
【实验二】测定NaNO2样品(含NaNO3杂质)的纯度
先查阅资料知:①5NO2-+ 2MnO4-+ 6H+ → 5NO3-+ 3Mn2+ + 3H2O;
②MnO4-+5Fe2++8H+→Mn2++5Fe3++4H2O
然后,设计如下方案测定样品的纯度。
38.取样品2.3g经溶解后得到溶液A 100 mL,准确量取10.00 mL A与24.00 mL 0.0500mol/L的酸性高锰酸钾溶液在锥形瓶中充分反应。反应后的溶液用0.1000mol/L (NH4)2Fe(SO4)2标准溶液滴定至紫色刚好褪去;重复上述实验3次,平均消耗(NH4)2Fe(SO4)2溶液10.00 mL,则样品中NaNO2的纯度为_________。
39.通过上述实验测得样品中NaNO2的纯度偏高,该小组讨论的原因错误的是 (填字母编号)。
a.滴定至溶液紫色刚好褪去,立即停止滴定
b.加入A与KMnO4溶液前的锥形瓶未经干燥
c.实验中使用的(NH4)2Fe(SO4)2溶液暴露在空气中的时间过长
铵明矾【NH4Al(SO4)2·12H2O】是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备。用芒硝(Na2SO4·10H2O)制备纯碱和铵明矾的生产工艺流程图如图1:

完成下列填空:
31.铵明矾溶液呈 性,它可用于净水,原因是 ;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是 。
32.写出过程Ⅰ的化学反应方程式 。
33.若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是 。
34.已知铵明矾的溶解度随温度升高明显增大。加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、 、过滤洗涤、干燥。
35.某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份。
(1)夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是 ;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是 (任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式 。
(2)该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)= 。
是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
[查阅资料]在260
和400
时分解产物不同。
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)

实验1:连接装置,检查气密性,按图示加入试剂(装置
盛0.5000
盐酸70.00
)。通入
排尽空气后,于260
加热装置
一段时间,停止加热,冷却,停止通入
。品红溶液不褪色,取下装置
,加入指示剂,用0.2000
溶液滴定剩余盐酸,终点时消耗
溶液25.00
。经检验滴定后的溶液中无
。
(1)仪器的名称是。
(2)滴定前,下列操作的正确顺序是(填字母编号)。
a.盛装0.2000溶液
b.用0.2000溶液润洗
c.读数、记录
d.查漏、清洗
e.排尽滴定管尖嘴的气泡并调整液面
(3)装置内溶液吸收气体的物质的量是
实验2:连接装置
,检查气密性,按图示重新加入试剂。通入
排尽空气后,于400
加热装置
至
完全分解无残留物,停止加热,冷却,停止通入
。观察到装置
、
之间的导气管内有少量白色固体。经检验,该白色固体和装置
内溶液中有
,无
。进一步研究发现,气体产物中无氮氧化物。
(4)检验装置内溶液中有
,无
的实验操作和现象是.
(5)装置内溶液吸收的气体是.
(6)在400
分解的化学方程式是.
某化学课外活动小组设计实验探究氨气的化学性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取: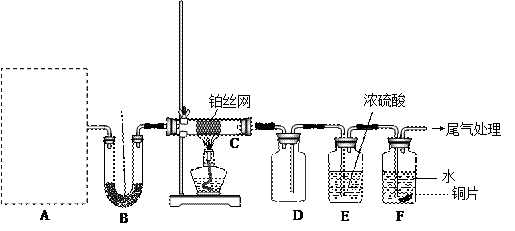
a. NH4HCO3 b. NH4Cl c. Ca(OH)2 d. NaOH 检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
(1)实验室制取A中气体时若只用一种试剂,该试剂是_______(填代表备选试剂的字母);此时A中反应的化学方程式_______ ,A中主要的玻璃仪器有_______(填名称)。
(2)C中发生反应的化学方程式为_______,该反应是_________反应(填“吸热”或“放热”)。
(3)浓硫酸的作用____________________;铜片溶解的化学方程式_________________.
(4)待实验结束后,将B中固体混合物溶于500 mL 1 mol·L-1的盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是_______ mol。
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。
CO(NH2)+2NaOH+NaClO═Na2CO3+N2H4•H2O+NaCl
NaClO过量时,易发生N2H4•H2O+2NaClO═N2↑+2NaCl+3H2O
实验一:制备NaClO溶液.(实验装置如图1所示)
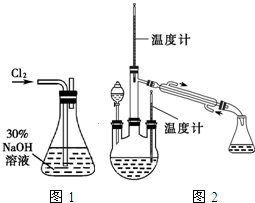
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有______________(填标号);
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的化学方程式是______________;
实验二:制取水合肼.(实验装置如图2所示)
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应.加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(已知:N2H4•H2O+2NaClO═N2↑+3H2O+2NaCl)
(3)分液漏斗中的溶液是_______(填标号);
A.CO(NH2)2溶液
B.NaOH和NaClO混合溶液
选择的理由是______________;
实验三:测定馏分中肼含量
称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL,用0.1000mol•L-1的I2溶液滴定.滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4•H2O+2I2═N2↑+4HI+H2O)
(4)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,用离子方程式解释其原因______________;
(5)实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4•H2O)的质量分数为___________;
某课外活动小组设计了以下实验验证Ag与浓硝酸反应的过程中可能产生NO,其实验流程图如下:
(1)测定硝酸的物质的量反应结束后,从如图装置B中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如上图所示。在B容器中生成硝酸的物质的量为__________________________mol,则Ag与浓硝酸反应过程中生成的NO2在标准状况下的体积为_________________________mL。
(2)测定NO的体积
①从如图所示的装置中,你认为应选用________装置进行Ag与浓硝酸反应实验,选用的理由是_______。
②选用如图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是______________(填各导管口编号)。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置___________(填“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
(3)气体成分分析
若实验测得NO的体积为112.0 mL(已折算到标准状况),则Ag与浓硝酸反应的过程中____________(填“有”或“没有”)NO产生,作此判断的依据是_____________。
某研究小组将纯净的气体通入0.1
的
溶液中,得到了
沉淀,为探究上述溶液中何种微粒能氧化通入的
,该小组突出了如下假设:
假设一:溶液中的
假设二:溶液中溶解的
(1)验证假设一
该小组涉及实验验证了假设一,请在下表空白处填写相关实验现象
| 实验步骤 |
实验现象 |
结论 |
| 实验1:在盛有不含 |
假设一成立 |
|
| 实验2:在盛有不含 |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的随通入
积的变化曲线入下图

实验1中溶液变小的原因是;
时,实验2中溶液
小于实验1的原因是(用离子方程式表示)。
(3)验证假设二
请设计实验验证假设二,写出实验步骤,预期现象和结论。
| 实验步骤、预期现象和结论(不要求写具体操作过程) |
(4)若假设二成立,请预测:在相同条件下,分别通入足量的和
,氧化相同的
溶液(溶液体积变化忽略不计),充分反映后两溶液的
前者(填大于或小于)后者,理由是
试题篮
()