下列实验可实现鉴别目的的是
| A.用NaOH溶液鉴别(NH4)2SO4和NH4Cl |
| B.用AgNO3溶液鉴别NaBr溶液和KI溶液 |
| C.用焰色反应鉴别NaCl和NaNO3 |
| D.用澄清石灰水鉴别CO2和SO2 |
某混合物的水溶液中可能含有以下离子中的若干种:Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-,现分别取100 mL的两份溶液进行如下实验。
①第一份加过量NaOH溶液后加热,收集到0.03 mol气体,无沉淀生成,同时得到溶液甲。
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02 g固体。
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到23.3g固体,向滤液中加入AgNO3溶液又有白色沉淀产生。下列有关叙述正确的是
| A.由①可知原溶液存在离子为NH4+,其浓度为0.03mol/L |
| B.原溶液肯定没有Fe3+、Mg2+,一定含有Na+ |
| C.n(NH4+):n(Al3+):n(SO42-)=3:1:10 |
| D.原溶液一定存在Cl- |
下列说法不正确的是
| A.用小苏打(NaHCO3)发酵面团制作馒头 |
| B.干燥的氯气和液氯均能使干燥的有色布条褪色 |
| C.用Al(OH)3治疗胃酸过多 |
| D.光导纤维的主要成分是SiO2 |
下列说法中不正确的是
| A.Al2O3可用作耐火材料,硅酸钠是制备木材防火剂的原料 |
| B.碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜合金 |
| C.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化 |
| D.绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物 |
下面是有关厨房中的常见操作或常见现象,其中不属于氧化还原反应的是
| A.烧菜用过的铁锅,经放置常出现红棕色斑迹 |
| B.用气灶燃烧沼气(主要成分为甲烷)为炒菜提供热量 |
| C.牛奶久置变质腐败 |
| D.氧化铜固体加入稀盐酸中,完全溶解 |
下列由实验现象得出的结论正确的是:( )
| A.向某无色液中加BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有Ag+ |
| B.向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32﹣ |
| C.加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,说明NH4Cl固体可以升华 |
| D.向NaBr溶液中滴入少量氯水和CCl4,振荡、静置,溶液下层呈橙红色,说明Br-还原性强于Cl- |
如图:烧瓶中充满a气体,滴管和烧杯中盛放足量b溶液,将滴管中溶液挤入烧瓶,打开止水夹f,能形成喷泉的是( )

| A.a是Cl2,b是饱和NaCl溶液 | B.a是NO,b是H2O |
| C.a是CO2,b是饱和NaHCO3溶液 | D.a是HCl,b是AgNO3溶液 |
为了确定(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分,下列实验操作及叙述中正确的是
| A.取少量样品放入试管中,加热,试管口放一团蘸有无水硫酸铜粉末的棉花团,变蓝则可证明晶体的成分中一定含有结晶水 |
| B.取少量样品溶于水,向溶液中滴入几滴新制氯水,再滴入2滴KSCN溶液,溶液变为红色,则可证明晶体的成分中含有Fe2+ |
| C.取少量样品溶于水,滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取少量样品放入试管中,加入少量浓NaOH溶液并加热,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |
除去下列物质中的杂质(括号内为杂质),所选用的试剂不正确的一组是
| 选项 |
待提纯的物质 |
选用试剂 |
| A |
FeCl3溶液(FeCl2溶液) |
Cl2 |
| B |
NaCl溶液(Na2SO4溶液) |
Ba(NO3)2溶液 |
| C |
Cl2(HCl) |
饱和食盐水 |
| D |
CO2(SO2) |
酸性KMnO4溶液 |
下列实验方法或操作能达到实验目的的是
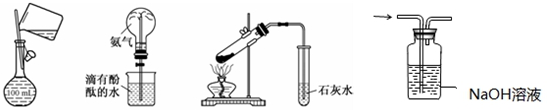
图1 图2 图3 图4
| A.图1:配制150 mL 0.1 mol/L盐酸 |
| B.图2:验证氨水呈碱性 |
| C.图3:探究NaHCO3的热稳定性 |
| D.图4:除去二氧化碳中的氯化氢 |
下列试剂的保存方法中不正确的是
| A.少量的钠保存在煤油中 |
| B.浓硝酸保存在无色玻璃瓶中 |
| C.新制的氯水保存在棕色玻璃瓶中 |
| D.NaOH溶液保存在带橡皮塞的玻璃瓶中 |
下列关于物质的用途,叙述不正确的是
| A.过氧化钠可用作供氧剂 | B.三氧化二铁可用做漆料 |
| C.镁铝合金可用作制造飞机的材料 | D.高纯硅用来制造光导纤维 |
试题篮
()