平达喜是一种常用抗酸药,其主要成分是由短周期元素组成的化合物X,式量为602。甲同学欲探究X的组成。
查阅资料:①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、碱式碳酸镁铝(或结晶水合物)。②Al3+在pH=5.0时沉淀完全; Mg2+在p H=8.8时开始沉淀,在pH=11.4时沉淀完全。
H=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
I.向一定量的X粉末中加入45.0mL的2mol/L盐酸溶液中,恰好完全反应并收集到112mL(标准状况下)的A气体,A气体可使澄清石灰水变浑浊。
Ⅱ.用铂丝蘸取少量I中所得的溶液,在火焰上灼烧,无黄色火焰。
Ⅲ.向I中所得的溶液中滴加氨水,调 节pH至5~6,产生白色沉淀B,过滤。
节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。沉淀物进行洗涤干燥后重1.74g,
(1)A的电子式是 。
(2)由I可确定X中存在两种带负电荷的原子团及个数比
(3)由I判断X一定不含有的元素是 。
(4)Ⅲ中生成B的离子方程式是 。
(5)Ⅳ中B溶解的化学方程式是 。
(6)沉淀C的化学式是 。
(7)若X中n(B)∶n(C)=1∶3,则X的化学式是 。
各物质之间的转化关系如下图,图中部分生成物省略,有相关信息如下:
①X为红褐色沉淀;②A为单质,B为溶液,D和F为气体;③反应I的产物只有Y和H O;
O;
④B、D、F和Y中均含有同一元素。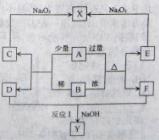
请回答下列问题:
(1)组成A的元素在周期表中属于 (选填序号)。
A.主族元素  B.副族元素 C.短周期元素 D.过渡元素
B.副族元素 C.短周期元素 D.过渡元素
(2)写出溶液B中溶质的化学式: 。
(3)写出反应I的化学反应方程式: 。
(4)以石墨为两极 材料,电解C的滴水溶液,写出电解初期阴极的电极反应式: 。
材料,电解C的滴水溶液,写出电解初期阴极的电极反应式: 。
(5)28g单质A与一定浓度的B溶液反应,当生成n(C):n(E)=2:3时,反应中转移电子 mol.
(6)给E溶液中加入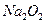 也能生成X,写出当n(E):n(
也能生成X,写出当n(E):n(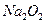 )=1:1时,反应的离子方程式 。
)=1:1时,反应的离子方程式 。
在下列物质转化关系中,反应的条件和部分产物已略去。其中A为常用的溶剂,B为常见的有色气体单质。
回答下列问题:
Ⅰ.若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的 反应。
反应。
(1)反应Ⅰ中,甲在通常条件下和A剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是 。
A.热分解法 B.热还原法 C.电解法
(2)反应Ⅱ中,乙与A在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是 。
(3)通过比较反应Ⅰ、Ⅱ的反应条件,可得出甲的金属性比乙的金属性 (填“强”或“弱”),比较二者金属性强弱的依据还可以是 (写出一种即可)。
(4)将2.5g甲的碳酸盐、碳酸氢盐和氢氧化物的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
①写出OA段所发生反应的离子方程式 。
②当加入35mL盐酸时,产生CO2的体积为 mL(标准状况)。
Ⅱ.若甲、乙是化合物,反应Ⅲ是工业制漂白液的反应,其中乙为非极性键的离子化合物,写出A与乙反应的化学方程式 ;
甲、乙为单质,丙、丁为化合物,它们之间存在如下的转化关系:
甲+丙→乙+丁
(1)若该转化关系为我国古代湿法冶炼金属乙的原理,写出此反应的离子方程式
,若该转化关系为高温火法冶炼金属乙(乙与湿法冶炼金属乙相同)的原理,且同时生成的丁是一种无色无味的有毒气体,则甲的化学式为
。
(2)若甲、乙均为非金属,丙为氧化物,则:
①乙为氧化产物时,乙可能是____(填一种物质的化学式,下同),按照元素周期表推出,此时反应物甲可能是____.
②乙为还原产物时,丁所属的物质类别是 , 发生的反应的化学方程式为 。
(4分)A、B、C、D四种气体,都是大气的污染物。国家环境保护法严格禁止把这类气体大量排入空气中,工业上通常都用碱液加以吸收。已知A的水溶液是一种无氧酸,A在空气中充分燃烧得到B;B是形成酸雨的主要污染物;C是一种单质,其水溶液具有漂白作用;D是硝酸工业尾气中有害物质之一,易溶于水。根据推断结果和下列要求写出有关的化学方程式。
(1) A在空气中完全燃烧: 。
(2) B的水溶液被空气氧化: 。
(3) C跟消石灰反应: 。
(4) D跟水反应: 。
写出下列反应的化学方程式
(1)铜和浓硫酸的反应 (2)铜和稀硝酸的反应
(3)非金属C和浓硝酸的反应 (4)氯化铁溶液中加入铜粉:
(5)氯化亚铁溶液中通入氯气 (6)氢氧化亚铁在空气中被氧化
下列是中学化学实验操作的内容:①碘的升华;②氢氧化钠溶解于水;③过氧化钠溶解于水;④氯化氢溶解于水。其中没有发生化学键断裂的是______________ ; 只发生离子键断裂的是____________ ; 只发生共价键断裂的是______________ ; 既发生离子键断裂, 又发生共价键断裂的是____________ .
材料是科学进步 的关键,不同的化学物质有不同的用途。现有①氯气、②氨气、③单质硅、④水玻璃四种物质。其中可以用作制冷剂的是
的关键,不同的化学物质有不同的用途。现有①氯气、②氨气、③单质硅、④水玻璃四种物质。其中可以用作制冷剂的是 ;常用作木材防火剂材料的是 ;可以用来消毒杀菌的是 。(填序号)
;常用作木材防火剂材料的是 ;可以用来消毒杀菌的是 。(填序号)
甲、乙分别是两种主族元素形成的氧化物,它们广泛存在于地壳中,均不溶于水,且都有如下相 同的转化关系,不同之处是乙对应的转化过程中需控制盐酸用量,若盐酸过量则得不到白色沉淀B。
同的转化关系,不同之处是乙对应的转化过程中需控制盐酸用量,若盐酸过量则得不到白色沉淀B。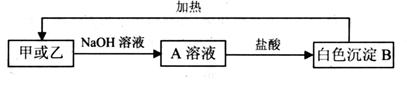
(1) 写出甲、乙的化学式:甲________,乙________;
(2) 写出下列反应的化学方程式:
甲+NaOH溶液____________________________________________,
乙+NaOH溶液____________________________________________;
(3) 分别写出甲、乙对应的A溶液与过量盐酸反应的离子方程式:
甲 ________________________________________
乙______________ ______________________________
______________________________
(4) 若将5.1g乙溶于适量的盐酸(二者恰好完全反应)后,再加入175 mL的2 mol.L-1 NH3H2O溶液,得到沉淀___________g
已知物质A、B、C、D、E、F有如下转化关系:
试根据上述变化,按要求写出两组C、D、E、F的可能化学式。
要求①C必须为不同的物质;②A、B、C、E的各元素原子序数不超过20;
| |
C |
D |
E |
F |
| 第一组 |
|
|
|
|
| 第二组 |
|
|
|
|
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:
其中: a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物。
(1)如果a是一种黄色粉末固体,试推断这五种物质(用名称表示):
a ; e 。
写出c→d的化学方程式 。
(2)如果a是一种常见气体,试推断这五种物质(用化学式表示):
a ; d 。
写出b→c的化学方程式  。
。
完成下反应的化学方程式或离子方程式(8分)
(1)铝与 氧化铁在高温下反应(铝热反应)
氧化铁在高温下反应(铝热反应)
______________________________________;
(2)医学上,用(胃舒平)氢氧化铝治疗胃酸过多,写出反应的离子方程式
____________________________________________________________
(3)工业上用焦炭和二氧化硅反应制得粗硅(Si)
____________________________________________________________
(4)装氢氧化钠溶液的试剂瓶不用玻璃塞,原因用化学方程式表示为_________________________________________________________
(8分)蛇纹石由MgO、A12O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸使之充分反应,过滤后,得沉淀X和溶液Y,分别向沉淀X和溶液Y中加 入NaOH溶液至过量。
入NaOH溶液至过量。
(1).蛇纹石成分中是碱性氧化物有__________,是两性氧化物的有_____。
(2) 沉淀X与NaOH溶液的离子方程式_______________________
(3)溶液Y中加入NaOH溶液有沉淀生成,再继续加NaOH溶液有部分沉淀溶解,沉淀溶解的离子方程式___________________
(4)检验蛇纹石固体成分中含有Fe2O3,应选择的试剂和方法_______
A、用NaOH溶液溶解,观察到红褐色沉淀
B、加入KSCN溶液溶解,能观察到红色沉淀生成
C、用稀硫酸溶解,加KSCN溶液后溶液变血红色
短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
(1)已知相关物质之间存在如下变化:
①丁与乙和水反应生成戊和丙的离子方程式为 ,由物质己电解得到单质D的化学方程式为 ;
②0.1mol/L的丙溶液中所含离子浓度由大到小排列顺序为 ;常温下,为使丙溶液中由丙电离的阴、阳离子浓度相等,应向溶液中加入一定量的乙的水溶液至 。
(2)已知E及其化合物有以下变化:
写出单质E与化合物Z在一定条件下反应生成X和水的化学方程式___ _,由A、B、C、D、E5种元素中的两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为 (任写一个即可)。
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2L的该无色气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的C的含氧酸盐的化学式是 。
试题篮
()