下列有关叙述正确的是
A. O和 O和 O中子数相同,质子数不同,互为同位素 O中子数相同,质子数不同,互为同位素 |
| B.H2O比H2S稳定,H-S键比H-O键更难断裂 |
| C.Na2O2晶体中阳离子与阴离子个数比为1:1 |
| D.Na2O晶体中存在离子键,是离子化合物 |
分子晶体的熔点通常都在200℃以下,下列数据是对应物质的熔点:据此做出的下列判断中正确的是
| 物质 |
Na2O |
NaCl |
AIF3 |
AlCl3 |
BCl2 |
Al2O3 |
CO2 |
SiO2 |
| 熔点/℃ |
920 |
801 |
1291 |
190 |
-107 |
2073 |
-57 |
1723 |
A.NaCl晶体熔化时,吸收的热量用于破坏离子键
B.表中只有BCl3和干冰是分子晶体
C.碳和硅是同一主族,故CO2和 SiO2的晶体类型相同
D.两种含钠化合物是离子晶体,三种含铝化合物也是离子晶体
A的化学式为NH5,常温下呈固态,构成它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构。则下列有关说法中,不正确的是
| A.1mol NH5中含有5NA个N—H键(NA为阿佛加德罗常数的数值) |
| B.NH5中既有共价键,又有离子键。 |
| C.它与水反应的化学方程式为:NH5+H2O==NH3·H2O +H2↑ |
D.NH5的电子式为: |
下列说法正确的是
①离子化合物含离子键,也可能含极性键或非极性键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物是离子化合物
| A.①③⑥ | B.②④⑥ | C.②③④ | D.①③⑤ |
氢化钠(NaH)是一种白色晶体,NaH与水反应放出H2,下列叙述正确的是
| A.NaH在水中显酸性 | B.NaH中氢离子电子层排布与氦相同 |
| C.NaH中氢离子半径比锂离子半径小 | D.NaH中氢离子被还原为H2 |
短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为32,原子最外层电子数之和为10。A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数。则下列叙述正确的是
A.一定条件下,B单质能置换出D单质,C单质能置换出A单质
B.D元素处于元素周期表中第3周期第IV族
C.C的最高价氧化物中含有共价键。
D.四种元素的原子半径:A>B>D>C
下列各组微粒的空间构型相同的是
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2
⑤CO2和BeCl2 ⑥SiO44-和SO42- ⑦BF3和Al2Cl6
| A.全部 | B.除④⑥⑦以外 | C.③④⑤⑥ | D.②⑤⑥ |
下列说法正确的是(NA为阿伏加德罗常数)
| A.124 g P4含有P—P键的个数为4NA |
| B.12 g石墨中含有C—C键的个数为3NA |
| C.12 g金刚石中含有C—C键的个数为2NA |
| D.60gSiO2中含Si—O键的个数为2NA |
短周期元素 W、X、 Y 和 Z 的原子序数依次增大。 其中 W 的阴离子的核外电子数与 X、 Y 原子的核外内层电子数相同。X 的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气方法来生产Y的单质,Z 与 X 同族。下列说法中正确的是
| A.以上四种元素的原子半径大小为 W<X<Y<Z |
| B.X 的氢化物与水分子之间可形成氢键 |
| C.已知 Z-Cl 键能比 X-Cl 键能小, 所以 Z 的最简单氯化物比 X 的简单氯化物沸点低。 |
| D.W 与 Y 可形成既含共价键又含离子键的化合物 |
X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次递增的同周期元素,最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的一半。下列说法正确的是
| A.原子半径W>Z>Y>X>M |
| B.将XZ2通入W单质与水反应后的溶液中,生成的盐一定只有一种 |
| C.由X、Y、Z、M四种元素共同形成的化合物中一定有共价健可能有离子键 |
| D.CaX2、CaM2、CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2 |
科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如图。下列有关推测肯定不正确的是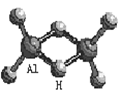
| A.Al2H6跟水的反应可能是氧化还原反应,产物之一可能是氢氧化铝 |
| B.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C.Al2H6分子是极性分子 |
| D.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
下列说法正确的是
①离子化合物一定含离子键,也可能含极性键或非极性键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物
| A.①③⑤ | B.②④⑥ | C.②③④ | D.①③⑥ |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且原子的最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键、又有共价键 |
液态氨中可电离出极少量的NH2-和NH4+。下列说法正确的是
| A.NH3属于离子化合物 | B.常温下,液氨的电离平衡常数为10-14 |
| C.液态氨与氨水的组成相同 | D.液氨中的微粒含相同的电子数 |
科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验。羟基硝酸铵的结构如图所示,下列说法不正确的是
| A.羟基硝酸铵中阳离子的各原子共平面 |
| B.羟基硝酸铵是离子化合物 |
| C.羟基硝酸铵中含有离子键和共价键 |
| D.9.6g羟基硝酸铵中含有0.2mol离子 |
试题篮
()