X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,则下列关于R的叙述正确的是
| A.R一定是共价化合物 |
| B.R一定是离子化合物 |
| C.R可能是共价化合物,也可能是离子化合物 |
| D.R可能是气态物质,也可能是固态物质 |
下列有关化学用语表示正确的是
A.NaCl的电子式: |
B.氟原子的结构示意图: |
| C.中子数为20的氯原子: 1720Cl |
| D.碳酸钠的电离方程式:Na2CO3=2Na++CO32- |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2杂化,而CH4是sp3杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
| D.氨气分子是极性分子而甲烷是非极性分子 |
(18分)Ⅰ.(7分)次磷酸(H3PO2)是一种一元中强酸,具有较强的还原性。试回答下列问题:
(1)P的原子结构示意图为 ;
(2)NaH2PO2为 (“正盐”或“酸式盐”),溶液中有关离子浓度从大到小的顺序为 。
(3)H3PO2可将溶液中的银离子还原为银单质,若氧化剂与还原剂的物质的量之比为4︰1,则该反应的氧化产物的化学式为 。
Ⅱ.(11分)某无机化合物A的相对分子质量为184。在一定条件下,SCl2与氨完全反应生成A和淡黄色单质B及离子化合物X,且X的水溶液的pH<7。将18.4gA隔绝空气加强热可得到12.8g B和气体单质C。请回答下列问题:
(1)A的化学式为 ,C的电子式为 。
(2)写出SCl2与氨反应的化学方程式 。
(3)亚硝酸钠和X固体在加热条件下 (填“可能”或“不能”)发生反应,判断理由是 。
(4)请设计检验物质X的实验方案 。
【原创】下列叙述正确的是
①元素的氢化物分子间能形成氢键,该元素非金属性一定是同一主族中最强,稳定性最好
②某离子晶体中含有非极性键,该晶体熔化时非极性键一定不被破坏
③电解质溶于水,是在电流作用下离解成自由移动的离子
④F2、C12、Br2、I2的熔沸点逐渐升高与分子间作用力有关
⑤干冰和氯化铵分别受热变为气体所克服的粒子间相互作用属于同种类型
⑥分子晶体中都存在范德华力,分子内都存在共价键
| A.①②④ | B.②④⑤ | C.①③⑥ | D.②⑤⑥ |
最近美国宇航局马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”——全氟丙烷(C3F8),并提出用其“温室化火星”使火星成为第二个地球的计划。下列有关全氟丙烷的说法正确的是
A.全氟丙烷的电子式为 |
| B.C3F8属于烃类物质 |
| C.全氟丙烷分子中存在极性键 |
| D.分子中三个碳原子可能处于同一直线上 |
【原创】有原子序数依次增大的A、B、C、D、E五种元素,A形成的单质是最轻的物质;B元素的一种核素常用于考古;D元素的价电子构型为nsnnpn+2; E是地壳中含量仅次于铝的金属元素。
(1)E元素在周期表中的位置 。
(2)BD2分子的电子式为 ,CA3分子的空间立体构型为 。
(3)A分别与B、C、D能形成电子数为10的化合物,它们的沸点由高到低的顺序是 (写分子式)。
(4)3g B2A6在足量氧气中燃烧并恢复到室温,放出Q kJ热量,则表示B2A6燃烧热的热化学方程式为
______ _ _____________。
(5)由E形成的某种化合物X (Na2ED4) 是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:在碱性条件下,利用NaClO氧化E(DA)3制得,则反应方程式为: __________。
(6)X也可以采用电解法制备:方法是用E电极电解NaOH溶液,则其阳极电极方程式为:__________。
【原创】已知:单质A +化合物 B →单质C +化合物D,则下列说法不正确的是
A.若A为Fe,C为氢气,则B可能是酸,也可能是水
B.若A、C为同族元素的单质,则B可能是光纤的原料,也可能具有臭鸡蛋气味
C.若B、D均为10电子微粒,则A可能是F2,也可能是O2
D.若B是金属氧化物,则A一定是非金属单质
北京大学和中国科学院的化学工作者合作已成功研制出碱金属与C60形成的球碳盐K3C60,实验测得该物质属于离子化合物,且具有良好的超导性,下列关于K3C60的组成和结构的分析正确的是
| A.K3C60中既有离子键,又有极性键 |
| B.K3C60中含有非极性共价键 |
| C.1 mol K3C60中含有的阴离子个数为3×6.02×1023 |
| D.该物质的化学式可写成KC20 |
神舟十号飞船是中国“神舟”号系列飞船之一,它是中国第五艘搭载太空人的飞船。神舟十号飞船发射成功后,将与2011年发射升空的天宫一号目标飞行器进行交会对接,开展相关空间科学试验。火箭推进器是成功发射的重要因素,事实上,推进器的发展经历了一个漫长的过程。
(1)20世纪前,黑火药是世界上唯一的火箭推进剂,黑火药是由硝酸钾、硫磺、木炭组成,黑火药爆炸的化学方程式为:S+3C+2KNO3=K2S+N2↑+3CO2↑。
①K2S的电子式为 ,CO2的结构式为 。
②已知S和氯水反应会生成两种强酸,其离子方程式为 。
③取黑火药爆炸后的残留固体,加水溶解过滤,得到滤液。写出检验此溶液中是否含有K+的实验操作方法 。
(2)20世纪60年代,火箭使用的是液体推进剂,常用的氧化剂有四氧化二氮、液氧等,可燃物有麟(N2 H4)、液氢等。
①肼(N2 H4)溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式: 。
②一种与N2 H4电子数相等的绿色氧化剂,能将油画表面黑色的PbS氧化成白色的PbSO4,使油画变白、翻新,化学方程式为: 。
(3)以上的火箭推进剂一般含有氮元素,含氮化合物种类丰富。有一含氮化合物,具有很强的爆炸性,86g该化合物爆炸分解会生成标况下N267. 2L和另一种气体单质H2。写出其爆炸的化学方程式 。
已知A、B、C、D、E五种主族元素分别位于第1、2、3周期,原子序数依次增大,其中A与C、B与D分别同主族,且B原子的最外层电子数等于A与C原子序数之和的一半,下列叙述正确的是
A.原子半径:A<B<C<D<E
B.D、E的气态氢化物的热稳定性:D>E
C.A与B、C与B均能形成X2Y2型化合物,且其中所含有的化学键类型相同
D.另外四种元素能够分别与C形成含单原子核阴离子的离子化合物
据报道,1995年化学家合成了一种分子式为C200H200的含多个碳碳叁键(-C≡C-)的链状烃,其分子中含碳碳叁键最多可以是( )
| A.49个 | B.50个 | C.51个 | D.100个 |
二茂铁[(C5H5)2Fe] 分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。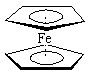
它的结构如右图所示,下列说法正确的是( )
| A.二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键 |
B.1mol环戊二烯(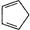 )中含有σ键的数目为5NA )中含有σ键的数目为5NA |
| C.分子中存在π键 |
| D.Fe2+的电子排布式为1s22s22p63s23p63d44s2 |
关于化学键的下列叙述中,正确的是
| A.离子化合物中可能含离子键 | B.共价化合物中可能含离子键 |
| C.离子化合物中不含共价键 | D.共价化合物中不含离子键 |
最近,科学家在甲烷的低温活化与二氧化碳加氢研究上取得了突破,其反应原理如下: 。下列说法错误的是
。下列说法错误的是
| A.CO2、CH3COOH均为共价化合物 |
| B.每生成1molCH3COOH,要消耗22.4LCO2 |
| C.CO2、CH3COOH分子中均含σ键和π键 |
D. 属于氧化反应 属于氧化反应 |
试题篮
()