A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,B与D形成的化合物BD与C的单质C2电子总数相等,CA3分子结构为三角锥形,D与E可形成E2D与E2D2两种离子化合物,D与F是同族元素。
根据以上信息,回答下列有关问题:
(1)写出基态时D的电子排布图 。
(2)写出化合物E2F2的电子式 ,化合物ABC的结构式 。
(3)根据题目要求完成以下填空:
BF32-中心原子杂化方式 ;D3中心原子杂化方式 ;
FD42-微粒中的键角 ;FD3分子的立体构型 。
(4)根据等电子原理,指出与BD2互为等电子体且含有C原子的微粒有 、 (要求写一种分子和一种离子)。
W、X、Y、Z四种元素的原子序数依次增大。其中Y原子的L电子层中,成对电子与未成对电子占据的轨道数相等,且无空轨道;X原子的L电子层中未成对电子数与Y相同,但还有空轨道;W、Z的原子序数相差10,且Z原子的第一电离能在同周期中最低。
(1)写出下列元素的元素符号:W ,X ,Y ,Z 。
(2)XW4分子中,中心原子属于 杂化,分子的空间构型为 ;
根据电子云重叠方式的不同,分子里共价键的主要类型为 。
(3)写出Y原子价层电子的排布图
(4)X的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
【化学-选修3:物质结构与性质】
(1)I.短周期某主族元素M的电离能情况如图(A)所示,则M元素位于周期表的第____族;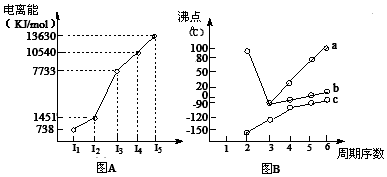
II.图B折线c可以表达出第_________族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:__________(填“a”或“b”);
III.部分有机物的熔沸点见下表: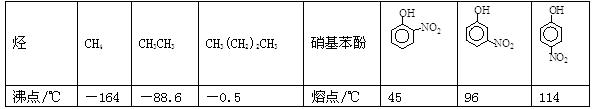
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):____________________;
(2)COCl2俗称光气,分子中C原子采取________杂化成键;其中碳氧原子之间共价键含有______(填字母):
a.2个σ键
b.2个π键
c.1个σ键.1个π键;
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为________________________________;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的2/3,
则绿色晶体配合物的化学式为_________________________。
(11分)元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素。Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,其空间构型为v形,W的基态原子3d轨道有8种运动状态不同的电子。请回答下列问题:
(1)Z在周期表中的位置 ;W基态原于的价电子排布图 。
(2)X、Y、Z、Q中,基态原子第一电离能最大的是 (填元素符号)。
(3)在XQ—中Q的杂化类型为 X的氧化物(X2O)晶体结构示意图如下,则1molX2O晶体含有 mol氢键。
(4)ZY3有较强的还原性,遇到NaClO溶液时有无污染的气体生成,其化学方程式为
(10分,每空1分).原子序数小于20的A.B.C.D.E.F.G七种元素,它们的原子序数依次增大,已知C元素是地壳中含量最多的元素;A和D的价电子数相同,C和E的价电子数也相同,且A和D两元素原子核外电子数之和是C.E两元素原子核内质子数之和的1/2;D.E.F三种元素的基态原子具有相同的电子层数,且F原子的p轨道上电子数比E原子的p轨道上多一个电子;B元素原子中未成对电子数与C相同;7种元素的基态原子中,G原子的电子层数最多且和A外于同一主族。
(1)用电子式表示D和E形成化合物的过程________________。
(2)写出基态G原子的简化核外电子排布式___________________________。
(3)A2C2分子中_____ (填“含”或“不含”,下同)σ键, π键,其电子式为:____________。
(4)在A―E.A―F两种共价键中,键的极性较强的是 ,键长较长的是 。
(5)7种元素中的一种或两种元素组成的分子,属于16电子的等电子体的有___________;(填两种,下同)属于18电子的等电子体的有___________;BC分子中,σ键和π键数目之比是________。
(8分,每空1分))有A、B、C、D、E五种短周期元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7∶8,E与B的质量比为1∶1。试回答:
(1)写出D元素基态原子的电子排布式:____________________________________。
(2)写出AB2的路易斯结构式:__________________。
(3)B、C两元素的第一电离能大小关系为________>________(填元素符号),
原因是_________________________________________________________________
根据VSEPR模型预测C的氢化物的立体结构为________,中心原子C的轨道杂化类型为________。
C的单质分子中π键的数目为________,B.D两元素的气态氢化物的稳定性大小关为________>________(填化学式)。
下表是元素周期表的一部分,表中所列字母分别代表一种化学元素。请用元素符号等化学用语回答下列有关问题:
(1)上述元素中第一电离能最大的元素是 ,C、D、E、F四种元素第一电离能由大到小的顺序 。
(2)由A、C、D形成的ACD分子中,σ键个数∶π键个数=________。
(3)要证明太阳上是否含有R 元素,可采用的方法是 。
(4)能够说明K、F两元素非金属性强弱的事实是 ;若欲用一个简单实验证明H、I两种元素金属性的强弱,其实验方法是 。
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。已知MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是_____(填“极性”或“非极性”)分子。
(6)C、D两种元素,C的气态氢化物难溶于水,而D的气态氢化物却极易溶于水,
其原因是 。
(7)在元素N的低价硫酸盐溶液中,加入少量由元素G、L、E组成的化合物(原子个数比为1:1:1),观察到的现象是 ;有关反应的离子方程式为 。
(每空1分,共8分)下列微粒:① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ 填写下列空白(填序号)
填写下列空白(填序号)
(1)呈正四面体的是 。
(2)中心原子轨道采取 杂化的化合物是 ,采取
杂化的化合物是 ,采取 杂化的化合物是 ,采取
杂化的化合物是 ,采取 杂化的化合物是 。
杂化的化合物是 。
(3)所有原子共平面的是 ,共线的是 。
(4)微粒存在的配位键的是 。
(5)含有极性键的极性分子是 。
根据要求回答下列问题:
①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧Al
(1)只含有离子键的是(用序号回答,下同)
(2)含有共价键的离子化合物是
(3)属于共价化合物的是
(4)熔融状态能导电的化合物是
(5)熔融状态时和固态时,都能导电的是
(14分)A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化关系如图所示(部分产物已略去)。
请按要求回答下列问题:
(1)若B、D为短周期同一主族的非金属单质,则反应(III)中氧化产物与还原产物的物质的量之比为___。
(2)若A、B、C均为短周期元素组成的化合物,且溶液都显碱性,D为植物光合作用必须吸收的气体,物质A中化学键的类型为______________________,相同温度下的溶解度B____________C(填“大于、小于、等于”)。
(3)若D为某金属单质,向C的溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则检验B溶液中阳离子的试剂为_________;C的溶液保存时,常加入D的目的是__________________。
(4)若D为强电解质溶液,A和C在溶液中反应生成白色沉淀B,写出反应(III)的离子方程式是_______________________________;符合条件的D物质可能是_______________(填序号)。
①硫酸 ②碳酸 ③氢氧化钠 ④一水合氨 ⑤氯化钡
(12分)根据已学知识,回答下列问题:
(1)具有(n-1)d10n s2电子构型的元素位于周期表中区和族。
(2)写出3P轨道上有2个未成对电子的元素名称:。
(3)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素X,该元素的价电子排布式为3d54s1,该元素可与氧元素形成离子X2O72-,K2X2O7氧化浓盐酸生成氯气的同时还生成了X3+,写出该反应的离子方程式 。
(4)键能是指气态基态原子形成1 mol化学键释放的最低能量。某些化学键的键能如下表
格所示(单位:kJ·mol-1):
| 键 |
H—H |
N N N |
O=O |
F—F |
H—Cl |
| 键能 |
436 |
946 |
498 |
157 |
431 |
| 键 |
N—N |
P—P |
P—O |
Cl—Cl |
Br—Br |
| 键能 |
193 |
198 |
360 |
242.7 |
193 |
①由表中所列化学键形成的单质分子中,最不稳定的是。
②通过表中键能数据,计算说明N2分子中的键比键稳定(填“ ”或“
”或“ ”)。
”)。
③化学反应的实质是旧化学键断裂和新化学键形成的过程。现有化学反应方程式 ,通过计算可以确定,1molP4(s)参加该反应, (填“吸收”或“放出”)的热量为kJ。
,通过计算可以确定,1molP4(s)参加该反应, (填“吸收”或“放出”)的热量为kJ。
A,B,C,D,E,F,G是元素周期表前四周期元素,原子序数依次增大,根据下表提供的有关信息,回答下列问题
| 元素 |
相关信息 |
| A |
所有单质中密度最小 |
| B |
形成化合物种类最多的元素 |
| D |
基态原子中只有3个能级,有2个未成对电子 |
| E |
短周期中原子半径最大 |
| F |
第三周期中电负性最大的元素 |
| G |
最外层只有一个电子,内层填满电子 |
(1)F元素原子的价电子排布式 ,B,C,D三元素第一电离能由大到小顺序为 (填元素符号)
(2)写出由A,B,C,D四种元素形成的一种简单的既能与酸反应又能与碱反应的化合物
(3)写出由元素E、F形成化合物的水溶液用惰性电极电解的离子方程式
(4)由A,B,C形成的三原子化合物中含有σ键 个,π键 个
(5)已知下列反应:
①G(s) + 1/2O2 (g) =" GO" (s) ; △H=-157.0 KJ/mol
②B(s) + O2 (g) = AO2(g) ; △H=-393.5 KJ/mol
写出单质B与足量GO 反应的热化学方程式
(12分)氮化钠(Na3N)是科学家制备的一种重要化合物,它与水作用可产生NH3,请回答:
(1)Na3N的电子式__________________,该化合物是由______________键形成。
(2)Na3N与水反应方程式为____________________________________________。
(3)Na3N放入足量盐酸中生成_______种盐,其化学式为__________________。
(4)比较Na3N中两种粒子的半径:r(Na+)___r(N3-)(填“>”“=”或“<” )
X、Y、Z三种短周期元素,两两之间能组成5种化合物A、B、C、D、E;X、Y、Z三种元素可组成化合物F。已知:化合物A、B、C中原子个数比都为1︰1;B为淡黄色固体,C、E常温下均为无色液体;A是化学式为XZ的离子化合物,A与E反应生成F和一种气体;D是化学式为X2Y的离子化合物,D的阴、阳离子具有相同的电子层结构且与E分子所含电子数相等。 请回答下列问题:
(1)X元素的名称是________________。
(2)X、Y、Z的原子半径从大到小的顺序是(用元素符号表示)____________________。
(3)写出F的电子式______________________________。
(4)已知X单质、A、B、D固体,分别与E反应都生成同一种物质,其中X单质、A、B分别与E的反应均是氧化还原反应。请写出X单质、B分别与E反应的化学方程式___________, ;
B中含有的化学键是 ;请举一例说明B的用途_____________。
(5)请写出由化合物C制取Y的单质反应的化学方程式_______________________________。
按要求回答下列问题:
(1) 用电子式表示H2O的形成过程________________________。
(2) 用电子式表示MgCl2的形成过程________________________。
试题篮
()