工业上常利用CO与SO2反应生成固态S单质和CO2,从而消除这两种气体对大气的污染:2CO(g)+SO2(g) 2CO2(g)+S(s)△H=﹣a kJ/mol(a>0),下列叙述正确的是
2CO2(g)+S(s)△H=﹣a kJ/mol(a>0),下列叙述正确的是
A.该反应的平衡常数表达式为K= |
| B.若反应开始时投入2 mol CO,则达平衡时,放出热量为a kJ |
| C.增大压强或升高温度都可以加快化学反应速率并提高SO2的转化率 |
| D.若单位时间内生成2 molCO2的同时,消耗1mol SO2,则说明反应达到平衡状态 |
已知:NO2(g)+SO2(g) SO3(g)+NO(g),现将体积之比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
SO3(g)+NO(g),现将体积之比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
| A.体系压强保持不变 |
| B.混合气体颜色保持不变 |
| C.SO3与NO的体积比保持不变 |
| D.每消耗1molSO2,同时生成1molNO |
对已达化学平衡的反应:2X(g)+Y(g) 2Z(g),减小压强后,对反应产生的影响是
2Z(g),减小压强后,对反应产生的影响是
| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正反应速率先减小后增大,逆反应速率减小,平衡向逆反应方向移动 |
| D.逆反应速率先减小后增大,正反应速率减小,平衡向逆反应方向移动 |
关于反应3A(g)+B(g) 2C(g)发生过程中的能量变化如图,下列说法中不正确的是
2C(g)发生过程中的能量变化如图,下列说法中不正确的是
| A.该反应为放热反应 |
| B.反应体系中加入催化剂,E1、E2减小,△H不变 |
| C.增大反应体系压强,化学平衡正向移动,气体B的浓度减少 |
| D.降低反应体系温度,反应速率减慢,A的转化率增大 |
某温度时,在2L容器中X、Y、Z三种物质的物质的量随时间的变化关系曲线如图所示。
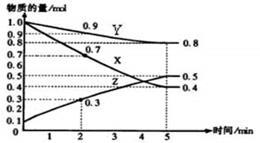
(1)由图中的数据分析,该反应的化学方程式为 ___________
(2)反应开始至2min、5minZ的平均反应速率为 、 ;
(3)5min后Z的生成速率比5min末Z的生成速率 (填写“大、小或相等”)。
已知2SO2(g) + O2(g) 2SO3(g)。若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法不正确的是
2SO3(g)。若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法不正确的是
| A.若升高温度,可以加快反应速率 |
| B.使用催化剂是为了加快反应速率 |
| C.在上述条件下,SO2不能完全转化为SO3 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)  2C (g) 达到平衡状态标志的是
2C (g) 达到平衡状态标志的是
(1)C生成速率与C分解速率相等
(2)单位时间内生成amolA,同时生成3amolB
(3)A、B、C的浓度不再变化
(4)A、B、C的物质的量不再变化
(5)混合气体的总压不再变化
(6)混合气体的物质的量不再变化
(7)单位时间内消耗a molA,同时生成3a molB
(8)A、B、C的分子数之比为1:3:2
A.(2) (8) B.(1) (6) C.(2) (4) D.(3) (8)
反应:A(气)+3B(气) 2C(气); ΔH < 0 达平衡后,将气体混合物的温度降低,下列叙述中正确的是
2C(气); ΔH < 0 达平衡后,将气体混合物的温度降低,下列叙述中正确的是
| A.正反应速率加大,逆反应速率变小,平衡向正反应方向移动 |
| B.正反应速率变小,逆反应速率加大,平衡向逆反应方向移动 |
| C.正反应速率和逆反应速率都变小,平衡向正反应方向移动 |
| D.正反应速率和逆反应速率都变小,平衡向逆反应方向移动 |
下列说法正确的是
A.用右图所示方法可保护钢闸门不被腐蚀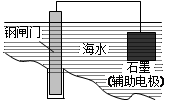 |
| B.SiO2(s)+2C(s)=Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0 |
C.常温下,NH4Cl溶液加水稀释,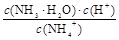 增大 增大 |
D.C(s)+H2O(g) CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 |
一定条件下,反应:C(s)+CO2(g) 2CO(g),ΔH>0在2L恒容密闭容器中进行,反应进行20s时,CO的物质的量增加了0.40 mol,则下列说法正确的是
2CO(g),ΔH>0在2L恒容密闭容器中进行,反应进行20s时,CO的物质的量增加了0.40 mol,则下列说法正确的是
A.反应20s,C的平均反应速率v (C) ="0." 005 mol·L-1·s-1
B.反应平衡时,v (CO2): v (CO) =1:2
C.升高温度时,正反应速率增大,逆反应速率减小
D.充入N2使体系压强增大,能提高反应速率
在密闭容中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
| A.A的转化率变大 | B.平衡向正反应方向移动 |
| C.D的体积分数变大 | D.a < c+d |
在密闭容器中进行反应:X2(g)+Y2(g)  2Z(g)已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.3mol•L-1、0.2mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g)已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.3mol•L-1、0.2mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
| A.Y2为0.15mol/L | B.Z为0.2mol/L |
| C.X2为0.3mol/L | D.Z为0.4mol/L |
在密闭容器中发生下列反应 aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原来的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原来的1.8倍,下列叙述正确的是
| A.A的转化率变大 |
| B.a<c+d |
| C.D的体积分数变大 |
| D.平衡向正反应方向移动 |
对于N2(g)+3H2(g) 2NH3(g),不能作为反应达到平衡状态的判断依据是
2NH3(g),不能作为反应达到平衡状态的判断依据是
| A.恒容密闭容器中总压强不变 |
| B.恒容密闭容器中混合气体的密度不变 |
| C.生成氨气的速率与氨气分解的速率相等 |
| D.N2、H2、NH3的浓度不再发生变化 |
下图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是
A.2SO2(g)+O2(g) 2SO3(g);△H<0 2SO3(g);△H<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g);△H<0 4NO(g)+6H2O(g);△H<0 |
C.H2(g)+I2(g) 2HI(g);△H>0 2HI(g);△H>0 |
D.N2(g) +3H2(g)  2 NH3(g) △H<0 2 NH3(g) △H<0 |
试题篮
()