已知反应X(g)+Y(g) R(g)+Q(g)的平衡常数与温度的关系如表.830℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005mol/(L•s).下列说法正确的是
R(g)+Q(g)的平衡常数与温度的关系如表.830℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005mol/(L•s).下列说法正确的是
| 温度/℃ |
700 |
800 |
830 |
1000 |
1200 |
| 平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
A.4s时容器内c(Y)="0.76" mol/L
B.830℃达平衡时,X的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应R(g)+Q(g) X(g)+Y(g)的平衡常数K=0.4
X(g)+Y(g)的平衡常数K=0.4
恒温恒容下,向2 L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)
MgO(s)+CO2(g)+SO2(g)
反应过程中测定的部分数据见下表:
| 反应时间/min |
n(MgSO4)/mol |
n(CO)/mol |
n(SO2) / mol |
| 0 |
2.0 |
2.0 |
0 |
| 2 |
|
0.8 |
|
| 4 |
|
|
1.2 |
| 6 |
|
1.2 |
2.8 |
下列说法正确的是
A.0~2 min内的平均速率为υ (CO)=0.6 mol/(L·min)
B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol的SO2
C.4 min后,若升高温度,SO2物质的量浓度变为0.7mol/L,则正反应为放热反应
D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)="0.6" mol
将一定量A、B装入容积为1 L的恒温密闭容器中,发生反应:2A(g)+mB(g)  nC(g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的1/2,达到新的平衡时C的浓度为1.8 x mol·L-1,下列说法正确的是
nC(g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的1/2,达到新的平衡时C的浓度为1.8 x mol·L-1,下列说法正确的是
A.化学计量数的关系为2+m>n
B.容器的容积缩小,正反应速率增大,逆反应速率减小
C.原容器中用B表示的该反应在1 min内的平均速率为 mol·(L·min)-1
mol·(L·min)-1
D.若保持温度和容器容积不变,充入氦气(不参与反应),平衡不发生移动
在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g) 2C(g);ΔH<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
2C(g);ΔH<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是

| |
X |
Y |
| A |
再加入B |
B的转化率 |
| B |
再加入C |
A的体积分数 |
| C |
增大压强 |
A的转化率 |
| D |
升高温度 |
混合气体平均摩尔质量 |
在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应:2R(气)+5Q(气) 4X(气)+nY(气)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是
4X(气)+nY(气)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是
| A.2 | B.3 | C.4 | D.5 |
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
下列判断不正确的是
| A.该反应的△S>0 | B.K(1000℃)>K(810℃) |
| C.b<f | D.915℃、2.0MPa时E的转化率为80% |
已知2SO2(g) + O2 (g)  2SO3(g),△H1=-414KJ·mol-1,向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,三个密闭容器中下列关系一定正确的是
2SO3(g),△H1=-414KJ·mol-1,向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,三个密闭容器中下列关系一定正确的是
| A.容器内压强p:p甲=p丙>2p乙 |
| B.c(SO2)与c(O2)之比k:k甲=k丙>k乙 |
| C.SO3的质量m:m甲=m丙>2m乙 |
| D.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙 |
一定温度下,在恒容密闭容器中发生如下反应:2A(g) + B(g)  3C(g),若反应开始时充入2molA和2molB,达平衡后A的体积分数为a%。其它条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%(不考虑无关气体的量)的是
3C(g),若反应开始时充入2molA和2molB,达平衡后A的体积分数为a%。其它条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%(不考虑无关气体的量)的是
A.1molB和1molC B.2molA、2molB和1molHe(不参加反应)
C.2mol C D.2molA、3molB和3molC
一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应,在t1时刻达平衡:A(g)+B(g)⇌xC(g)+D(g).在t2、t3时刻分别改变反应的一个条件,测得溶器中C(g)的浓度随时间变化如图所示.有关说法正确的是
| A.t1-t3间该反应的平衡常数相同,均为0.25 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量D |
| D.反应方程式中x=2 |
对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g),在673K、30MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是
2NH3(g),在673K、30MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是

| A.NH3在点a’的正反应速率比点b’的正反应速率更小 |
| B.点c反应达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D.点e处c(NH3)不再变化 |
在373K 时,把0.5 mol N2O4气体通入体积为5 L的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol/L。在60 s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法正确的是
| A.前2 s,以N2O4浓度变化表示的平均反应速率为0.01 mol·L-1·s-1 |
| B.在2 s时,体系内压强为反应前的1.1倍 |
| C.平衡时,体系内含N2O4 0.25 mol |
| D.平衡时,若往容器内充入氮气,则可提高N2O4的转化率 |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知
 kJ·mol
kJ·mol )
)
| 容器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
1mol N2、3mol H2 |
2mol NH3 |
4mol NH3 |
NH3的浓度(mol·L ) ) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
放出akJ |
吸收bkJ |
吸收ckJ |
| 体系压强(Pa) |
p1 |
p2 |
p3 |
| 反应物转化率 |
 |
 |
 |
下列说法正确的是
A. B.α1+α3="1" C.
B.α1+α3="1" C. D.
D.
在恒温、恒容下,发生如下反应:2A(g)+2B(g)  C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1和6 mol·L—1 ,以下叙述正确的是
C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1和6 mol·L—1 ,以下叙述正确的是
A、达到平衡时,途径I的反应速率等于途径Ⅱ的反应速率
B、达到平衡时,途径I所得混合气体的压强等于途径Ⅱ所得混合气体的压强
C、两途径最终达到平衡时,体系内各组分的百分含量相同
D、两途径最终达到平衡时,体系内各组分的百分含量不相同
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是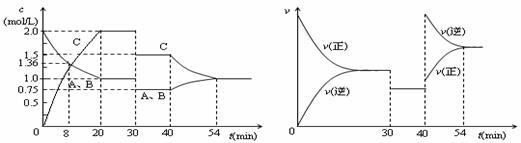
| A.第8min时 A的反应速率为0.08mol·L-1·min-1 |
| B.在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 |
| C.30min时改变的条件是降低温度,40min时改变的条件是升高温度 |
| D.反应方程式中的x=1,且正反应为放热反应 |
可逆反应N2(g)+3H2(g) 2NH3(g),△H=-Q KJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
2NH3(g),△H=-Q KJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
| A.达到平衡时,两容器中反应物的转化率不同 |
| B.达到平衡时,甲中NH3的体积分数与乙相等 |
| C.达到平衡后,再向乙中加入0.2moLN2、0.6molH2、1.6molNH3,平衡向生成NH3的方向移动 |
D.乙中的热化学反应方程式为2NH3(g) N2(g)+3H2(g);△H=+Q2KJ/mol N2(g)+3H2(g);△H=+Q2KJ/mol |
试题篮
()