下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是( )
| A.Cu能与浓HNO3反应,而不与浓盐酸反应 |
| B.Cu与浓HNO3反应比与稀HNO3反应快 |
| C.N2与O2在常温、常压下不反应,放电时可反应 |
| D.Cu与浓H2SO4反应,而不与稀H2SO4反应 |
在用盐酸跟碳酸钙进行化学反应时,能使反应的起始速率明显增大的是( )
| A.升高反应温度 |
| B.加入碳酸钙的量增大一倍 |
| C.加入盐酸的量增大一倍 |
| D.加入盐酸的量减半,但浓度增大一倍 |
甲、乙两个容器内都在进行A→B的反应,甲中每分钟减少4 mol A,乙中每分钟减少2 mol A,则两容器中的反应速率( )
| A.甲快 | B.乙快 | C.相等 | D.无法确定 |
下列四个数据都表示合成氨(N2+3H2 2NH3)的反应速率,其中速率代表同一反应的是( )
2NH3)的反应速率,其中速率代表同一反应的是( )
①v(N2)="0.2" mol·(L·min)-1 ②v(NH3)="0.45" mol·(L·min)-1 ③v(H2)="0.6" mol·(L·min)-1 ④v(H2)="0.225" mol·(L·min)-1
| A.①② | B.①③ | C.③④ | D.②④ |
某温度时,浓度均为1 mol·L-1的两种气体X2、Y2,在容积不变的密闭容器中发生反应,反应结束时,容器内各物质的浓度为:c(X2)="0.6" mol·L-1,c(Y2)="1.2" mol·L-1,c(Z)="0.4" mol·L-1。则该反应的化学方程式为( )
| A.2X2+Y2="===2Z" | B.X2+Y2====2Z |
C.2X2 Y2+2Z Y2+2Z |
D.3X2+6Y2====2Z |
可逆反应2SO2(g)+O2(g) 2SO3(g),在不同条件下测得化学反应速率最快的为( )
2SO3(g),在不同条件下测得化学反应速率最快的为( )
| A.v(O2)="3" mol·(L·min)-1 | B.v(SO2)="4" mol·(L·min)-1 |
| C.v(SO3)="0.1" mol·(L·s)-1 | D.v(O2)="0.1" mol·(L·s)-1 |
在N2+3H2 2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )
2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )
| A.v(H2)="0.7" mol·(L·min)–1 | B.v(NH3)="0.3" mol·(L·min)-1 |
| C.v(H2)="0.2" mol·(L·min)-1 | D.v(H2)="0.15" mol·(L·min)-1 |
反应2SO2+O22SO3经过一段时间后,SO2的浓度减小了0.4 mol·L-1,在这段时间内用氧气的浓度变化表示的速率为0.04 mol·(L·s)-1,则这段时间为( )
| A.1 s | B.2.5 s | C.5 s | D.10 s |
在密闭容器中进行如下反应:C(s)+ H2O(g)====CO(g)+H2(g),当改变下列条件时反应速率不会加快的是( )
| A.升温 | B.加压 | C.充入H2O(g) | D.充入N2 |
一定能使化学反应NaOH+HCl====NaCl+H2O速率加快的方法是( )
(a)升温 (b)减小生成物浓度 (c)增加反应物浓度 (d)加压
| A.(a)(b)和(c) | B.(a)和(c) | C.(b)和(d) | D.全部 |
已知:4NH3+5O2====4NO+6H2O,若反应的速率分别用v(NH3)、v(NO)、v(H2O)(mol·L-1·s-1)来表示,则正确的关系是( )
A. v(NH3)=v(O2) v(NH3)=v(O2) |
B.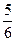 v(O2)=v(H2O) v(O2)=v(H2O) |
C.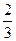 v(NH3)=v(O2) v(NH3)=v(O2) |
D. v(O2)=v(NO) v(O2)=v(NO) |
100 mL 6 mol·L-1 H2SO4与过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成H2的总质量,可向反应物中加适量的( )
| A.碳酸钠固体 | B.水 |
| C.硫酸锌溶液 | D.硫酸铵固体 |
下列各组溶液同时开始反应,出现浑浊最早的是( )
| A.10 ℃时5 mL 0.1 mol·L-1Na2S2O3与5 mL 0.1 mol·L-1H2SO4溶液混合 |
| B.10 ℃时50 mL 0.05 mol·L-1Na2S2O3与5 mL 0.1 mol·L-1H2SO4溶液混合 |
| C.20 ℃时5 mL 0.1 mol·L-1Na2S2O3与5 mL 0.1 mol·L-1H2SO4溶液混合 |
| D.20 ℃时50 mL 0.5 mol·L-1Na2S2O3与5 mL 0.1 mol·L-1H2SO4溶液混合 |
某温度下,反应2N2O5 4NO2+O2开始进行时c(N2O5)="0.048" mol·L-1,过1 min后c(N2O5)="0.03" mol·L-1,则该反应的反应速率正确的是( )
4NO2+O2开始进行时c(N2O5)="0.048" mol·L-1,过1 min后c(N2O5)="0.03" mol·L-1,则该反应的反应速率正确的是( )
| A.v(N2O5)=1.8×10-4 mol·L-1·s-1 | B.v(O2)=1.8×10-4 mol·L-1·s-1 |
| C.v(N2O5)=1.08×10-2 mol·L-1·s-1 | D.v(NO2)=2v(N2O5) |
试题篮
()