)将等物质的量的A、B混合于2L密闭容器中发生如下反应:
3A(g)+B(g)=xC(g)+2D(g) 经5分钟后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L·min) 求:
(1)此时A的浓度及反应开始前容器中A、B的物质的量分别为 、 、
(2)B的平均反应速率
(3)x=
在1.0密闭容器中放入0.10molA(g)
,在一定温度进行如下反应应:

反应时间()与容器内气体总压强(
)的数据见下表:
| 时间 |
0 |
1 |
2 |
4 |
8 |
16 |
20 |
25 |
30 |
| 总压强 |
4.91 |
5.58 |
6.32 |
7.31 |
8.54 |
9.50 |
9.52 |
9.53 |
9.53 |
回答下列问题:
(1)欲提高的平衡转化率,应采取的措施为。
(2)由总压强和起始压强
计算反应物
的转化率
的表达式为。
平衡时的转化率为,列式并计算反应的平衡常数
。
(3)①由总压强和起始压强
表示反应体系的总物质的量
总和反应物
的物质的量
,
总=
,
=
。
②下表为反应物浓度与反应时间的数据,计算
=
| 反应时间 |
0 |
4 |
8 |
16 |
| 0.10 |
a |
0.026 |
0.0065 |
分析该反应中反应反应物的浓度变化与时间间隔(
)的规律,得出的结论是,
由此规律推出反应在12时反应物的浓度
为
。
把0.6 mol X气体和0.6 mol Y气体混合于2 L体积不变的密闭容器中,使它们发生如下反应:2X(g)+ Y(g)=4Z(g)+2W(g)。2 min末生成0.2 mol W。计算:(1)前2min内用X的浓度变化表示的平均反应速率;(2)2min末Y的物质的量浓度。
在一定条件下,向体积为2 L的容器中加入2 mol O2和3 mol SO2使之反应生成SO3气体:2SO2+ O2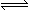 2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
(1)2min内,平均反应速率v(SO3)=
(2)2min时,SO2的浓度为
把0.2molX气体和0.5molY气体混合于1L密闭容器中,使它们发生如下反应:2X(g)+3Y(g)=nZ(g)+4W(g)。2min末已生成0.2molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L•min),试计算:
(1)前2min内用W的浓度变化表示的平均反应速率;
(2)2min末时Y的浓度;
(3)化学反应方程式中n的值是多少?
某一化学反应,若温度每升高10℃,反应速率提高到原来的3倍,如果在20℃时,该反应的速率为0.2mol/ (L·s),将温度升到60℃进行该反应,其反应速率应为多少?
将6 mol H2和3 molCO充入容积为0.5 L的密闭容器中,进行如下反应:
2H2(g)+CO(g)  CH3OH(g),6秒末时容器内压强为开始时的0.6倍。试计算:(写出计算过程)
CH3OH(g),6秒末时容器内压强为开始时的0.6倍。试计算:(写出计算过程)
(1)H2的反应速率是多少?
(2)CO的转化率为多少?
(8分)恒温下,将a mol N2与b mol H2的混合气体通入一个容积为2L的密闭容器中,发生如下反应: N2 (g) + 3 H2(g)  2NH3(g);若反应进行到5min时,测得n (N2) = 13mol,n (NH3) = 6mol,计算a值、N2的起始浓度及用H2表示的反应速率(要有计算过程)。
2NH3(g);若反应进行到5min时,测得n (N2) = 13mol,n (NH3) = 6mol,计算a值、N2的起始浓度及用H2表示的反应速率(要有计算过程)。
在2L的密闭容器中,充入1molSO2和1molO2,在一定条件下发生反应:2SO2+O2 2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:
2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:
(1)用SO2表示该化学反应速率为多少?
(2)若改用O2表示化学反应速率又为多少?
(3)若要提高反应速率你认为可采取的合理措施有哪些?
在一个容积为500mL的密闭容器中,充入5molH2和2molCO。在一定温度,一定压强下,发生如下反应:2H2(g)+CO(g)  CH3OH(g),经过5min后达到平衡状态。若此时测得CH3OH 蒸气的浓度为2mol/L,求
CH3OH(g),经过5min后达到平衡状态。若此时测得CH3OH 蒸气的浓度为2mol/L,求
(1) 以H2的浓度变化表示的该反应的速率;
(2) 到平衡时CO的转化率;
(3) 平衡混合气的密度与相同状况下的氢气密度之比。
将气体A、B置于固定容积为2L的密闭容器中,发生如下反应 :3A(g)+B(g) 2C(g)+2D(g)反应进行到10s末,达到平衡,测得A的物质的量为0.6mol,C的物质的量为0.8mol。
2C(g)+2D(g)反应进行到10s末,达到平衡,测得A的物质的量为0.6mol,C的物质的量为0.8mol。
(1)用C表示10s内正反应的化学反应速率。
(2)反应前A的物质的量浓度是多少?
把0.4 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:4X(g)+5Y(g)=nZ(g)+6W(g)。2 min时生成0.3 mol W,此时测知以Z的浓度变化表示的反应速率为0.05 mol·L-1·min-1。试计算:
(1)前2 min内用X的浓度变化表示的平均反应速率为 mol·L-1·min-1。
(2)计算n值和2 min末时Y的浓度(写出必要的计算过程)。
在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g)  4NO2(g)+ O2(g)。
4NO2(g)+ O2(g)。
反应5min后,测得N2O5转化了20%,求:
(1)5分钟内:υ(NO2)、υ(O2)分别为多少?
(2)5min时,N2O5占混合气体总体积的百分比是多少?
将等物质的量A、B混合于2L的密闭容器中,发生如下反应:3A(g)+ B(g) xC(g) + 2D(g),经5min后测得D的浓度为0.5mol/L,c (A)∶c(B)=3∶5,C的平均反应速率是0.1mol/(L·min)。
xC(g) + 2D(g),经5min后测得D的浓度为0.5mol/L,c (A)∶c(B)=3∶5,C的平均反应速率是0.1mol/(L·min)。
求:
(1)此时A的浓度及反应开始前放入容器中A、B物质的量;
(2)B的平均反应速率;
(3)x值是多少?
在一固定容积的密闭容器中,a mol/LN2和b mol/L H2反应,一定条件下经过2min达到平衡,生成c mol/L NH3.
求:(1)用H2表示的速率是多少?(2)N2的转化率是多少?
试题篮
()