在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g) A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
| A.平均反应速度:乙>甲 | B.平衡时C的物质的量甲>乙 |
| C.平衡时C的转化率:乙<甲 | D.平衡时A的物质的量甲>乙 |
一定条件下,可逆反应C(s)+ CO2(g) 2CO(g)△H>0,达到平衡状态,现进行如下操作:①升高反应体系的温度; ②增加反应物C的用量; ③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是
2CO(g)△H>0,达到平衡状态,现进行如下操作:①升高反应体系的温度; ②增加反应物C的用量; ③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是
| A.①②③④ | B.①③ | C.①②③ | D.①③④ |
可逆反应aA(s)+bB(g)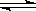 cC(g)+dD(g),当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是
cC(g)+dD(g),当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是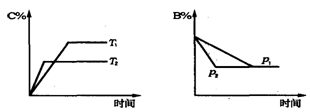
| A.T1>T2,正反应放热 |
| B.Tl<T2,正反应吸热 |
| C.P1>P2,a+b=c+d |
| D.Pl<P2,b=c+d |
下图曲线a表示放热反应X(g)+Y(g)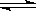 Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是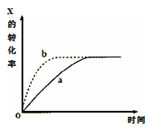
| A.减小体积 | B.加大X的投入量 |
| C.减压 | D.升高温度 |
已知分解1 mol H2O2 放出热量98kJ,在含少量I-的溶液中,H2O2的分解机理为:
H2O2+ I-→H2O +IO-(慢) H2O2+ IO-→H2O +O2+ I-(快)
下列有关反应的说法正确的是
| A.反应的速率与I-的浓度有关 | B.IO-也是该反应的催化剂 |
| C.反应活化能等于98kJ·mol-1 | D.v (H2O2)=" v" (H2O)=" v" (O2) |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2+3H2 2NH3 △H=-92.4kJ/mol)下列说法正确的是
2NH3 △H=-92.4kJ/mol)下列说法正确的是
| A.2c1>c3 | B.a1+a3<1 | C.2p2<p3 | D.a=b |
在一个容积固定的密闭容器中,发生反应:CO(g)+2H2(g) CH3OH(g)ΔH<0。第2 min时只改变一个条件,反应情况如下表:
CH3OH(g)ΔH<0。第2 min时只改变一个条件,反应情况如下表:
| 时间 |
c(CO)/mol/L |
c(H2)/mol/L |
c(CH3OH)/mol/L |
| 起始 |
1 |
3 |
0 |
| 第2 min |
0.8 |
2.6 |
0.2 |
| 第4 min |
0.4 |
1.8 |
0.6 |
| 第6 min |
0.4 |
1.8 |
0.6 |
下列说法不正确的是
A.第4 min至第6 min该化学反应处于平衡状态
B.第2 min时,如果只改变某一条件,则改变的条件可能是降低温度
C.第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂
D.第6 min时,其他条件不变,如果升高温度,正反应速率增大
合成氨反应:N2(g)+3H2(g) 2NH3(g)ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是( )
2NH3(g)ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是( )


| A.t1时增大了压强 | B.t2时充入了稀有气体 |
| C.t3时升高了温度 | D.t4时降低了温度 |
对于制氢气原理CH4(g)+H2O(g) CO(g)+3H2(g)ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
CO(g)+3H2(g)ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
| A.降低压强 | B.增大水蒸气浓度 | C.加入催化剂 | D.升高温度 |
0.1mol/LNa2S2O3溶液与0.1mol/LH2SO4溶液各5mL和10mL水混合,反应速率为v1mol/(L·s);0.2mol/L Na2S2O3溶液与0.2mol/LH2SO4溶液各5mL和20mL水混合,反应速率为v2 mol/(L·s);则v1和v2的关系是
| A.大于 | B.小于 | C.等于 | D.不能确定 |
下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是
| A.增大反应物的浓度,活化分子百分数增加,反应速率加快 |
| B.增大气体反应体系的压强,单位体积中活化分子数增多,气体反应速率加快 |
| C.升高反应的温度,活化分子百分数增加,有效碰撞的几率提高,反应速率增大 |
| D.催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大 |
下列有关化学反应速率的说法正确的是
| A.凡是能量达到活化能的分子发生的碰撞均为有效碰撞 |
| B.增大反应物浓度能加快正反应的反应速率,降低逆反应的反应速率 |
| C.温度升高使化学反应速率加快的主要原因是增加了反应物分子之间的碰撞次数 |
| D.决定化学反应速率的根本因素是参加反应的各物质的性质 |
在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)△H<0。
(1)保持容器容积不变,向其中加入1molH2,反应速率 理由是 。
(2)保持容器容积不变,向其中加入1molN2(N2不参加反应),反应速率 理由是 。
(3)保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率________________,理由是________________。
(4)保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),反应速率________________,理由是______________。
(5)提高反应的起始温度,反应速率______________,理由是______________。
如图是相同条件下做H2O2分解的对比实验时,放出O2的体积随时间的变化关系示意图,a为使用催化剂,b为不使用催化剂,其中正确的图象是
A. |
B. |
C. |
D. |
试题篮
()