在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s)  Ca(OH)2(aq)
Ca(OH)2(aq)  Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是
Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是
| A.n(Ca2+)减小 | B.c(Ca2+)不变 | C.n(OH-)增大 | D.c(OH-)减小 |
下列说法正确的是
| A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS) |
| B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大 |
| C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体 |
| D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀 |
已知25℃时BaSO4饱和溶液中存在BaSO4(s) Ba2+(aq)+SO(aq),
Ba2+(aq)+SO(aq),
Ksp=1.1025×10-10,下列有关BaSO4的溶度积和溶解平衡的叙述正确的是( )
| A.25℃时,向c(SO)=1.05×10-5mol/L的BaSO4溶液中,加入BaSO4固体,c(SO)增大 |
| B.向该饱和溶液中加入Ba(NO3)2固体,则BaSO4的溶度积常数增大 |
| C.向该饱和溶液中加入BaCl2固体,则该溶液中c(SO)减小 |
| D.向该饱和溶液中加入Na2SO4固体,则该溶液中c(Ba2+)>c(SO) |
下列说法正确的是
| A.难溶电解质的溶度积越小,溶解度越大 |
| B.可以通过沉淀反应使杂质离子完全沉淀 |
| C.难溶电解质的溶解平衡是一种动态平衡 |
| D.AgCl固体在等浓度的NaCl、CaCl2溶液中的溶解度相同 |
向5mLNaCl溶液里滴 入一滴AgNO3溶液,出现白色沉淀,继续加入一
入一滴AgNO3溶液,出现白色沉淀,继续加入一 滴KI溶液,沉淀变为黄色,再加入一滴Na2S溶液,沉淀又变为黑色,据此分析此三种沉淀物的KSP的一般关系为()
滴KI溶液,沉淀变为黄色,再加入一滴Na2S溶液,沉淀又变为黑色,据此分析此三种沉淀物的KSP的一般关系为()
| A.KSP(AgCl)=KSP(AgI)=KSP(Ag2S) | B.KSP(AgCl)<KSP(AgI)<KSP(Ag2S) |
| C.KSP(AgCl)>KSP(AgI)>KSP(Ag2S) | D.因发生特殊反应,无法判断 |
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S: Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是
| A.CuS<Cu(OH)2<CuCO3 | B.CuCO3<Cu(OH)2<CuS |
| C.CuS<CuCO3<Cu(OH)2 | D.Cu(OH)2<CuCO3<CuS |
下表是五种银盐的溶度积常数(25℃):
| 化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
| 溶度积 |
1.8×10-10 |
1.4×10-5 |
6.3×10-50 |
7.7×10-13 |
8.51×10-16 |
下列说法错误的是
| A.五种物质在常温下溶解度最大的是Ag2SO4 |
B.将氯化银溶解于水后 ,向其中加入Na2S,则可以生成黑色沉淀 ,向其中加入Na2S,则可以生成黑色沉淀 |
| C.对于氯化银、溴化银和碘化银三种物质在常温下的溶解度随着氯、溴、碘的顺序增大 |
| D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动 |
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13 ,Ksp(Ag2CrO4)=9×10-11。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010 mol/L,向该溶液中逐滴加入0.010 mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为 ( )
| A.Cl-、Br-、CrO42- | B.CrO42-、Br、Cl- |
| C.Br-、Cl-、CrO42- | D.Br、CrO42-、Cl- |
25℃时,水的电离达到平衡:H2O H+ + OH-,下列叙述正确的是
H+ + OH-,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| D.将水加热,Kw增大,pH不变 |
已知t ℃时的Ksp (AgC1) =1.6×10-10,Ksp (AgBr )=7.8×10-13;在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是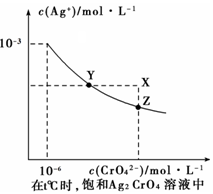
| A.t℃时,Ksp (Ag2CrO4 )=1×10-9 |
| B.t℃时,在饱和Ag2CrO4溶液中加入AgNO3可使溶液由Z点到X点 |
| C.t℃时,溶解度的大小顺序为AgC1 > Ag2CrO4>AgBr |
| D.t℃时,取一定量的KCl和KBr的混和溶液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,c(C1-)/c(Br-)= Ksp (AgC1)/ Ksp (AgBr) |
下列说法不正确的是( )
| A.Ksp只与难溶电解质的性质和温度有关 |
| B.由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C.其他条件不变,离子浓度改变时,Ksp不变 |
| D.两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是( )

提示:BaSO4(s) Ba2+(aq)+SO42-(aq)的平衡常数Ksp=c(Ba2+)·c(SO42-),称为溶度积常数。
Ba2+(aq)+SO42-(aq)的平衡常数Ksp=c(Ba2+)·c(SO42-),称为溶度积常数。
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
下列说法不正确的是
| A.化学反应是旧键断裂和新键形成的过程 |
| B.盖斯定律实质上是能量守恒定律的体现 |
| C.反应前后分子数不变遵循的是质量守恒定律 |
| D.溶解平衡、水解平衡和电离平衡均为动态平衡 |
某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:
①5 mL水
②20 mL 0.5 mol·L-1的Na2SO4溶液
③40 mL 0.2 mol·L-1的Ba(OH)2溶液
④40 mL 0.1 mol·L-1的H2SO4溶液中,溶解至饱和
以上各溶液中,c(Ba2+)的大小顺序正确的是( )
| A.③>①>④>② | B.③>①>②>④ |
| C.①>④>③>② | D.①>③>④>② |
试题篮
()