有关如下图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,正确的是
| A.铜棒上有气泡逸出 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.反应中,盐桥中的K+会移向CuSO4溶液 |
| D.反应前后铜棒质量不改变 |
磷酸燃料电池是目前较为成熟的燃料电池,其基本组成和反应原理如下。
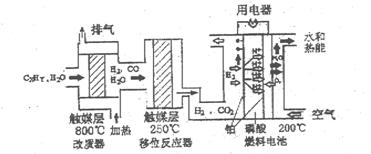
下列说法不正确的是 ( )
|
A.在改质器中主要发生的反应为CXHy+XH2O XCO+(X+Y/2)H2 XCO+(X+Y/2)H2 |
B.移位反应器中CO(g)+H2O(g)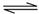 CO2(g)+H2(g) CO2(g)+H2(g)  。温度越高,CO转化率越大 。温度越高,CO转化率越大 |
| C.负极排出的气体主要是CO2 | |
| D.该电池正极的电极反应为O2+4H++4e-=2H2O |
纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:
Zn +2OH--2e-= Zn(OH)2 Ag2O+ H2O+ 2e-= 2Ag +2OH- 下列说法正确的是:( )
| A.溶液中OH-向正极移动,K+、H+向负极移动 |
| B.锌发生还原反应,氧化银发生氧化反应 |
| C.锌是负极,氧化银是正极 |
| D.在电池放电过程中,电解质溶液的酸碱性基本保持不变 |
在右图所示的原电池中,负极发生的反应是
| A.Cu2+ + 2e- ="=" Cu | B.Cu-2e- ="=" Cu2+ |
| C.2H+ + 2e- ="=" H2↑ | D.Zn-2e- ="=" Zn2+ |
在下图所示的柠檬电池中,外电路上的电子从电极Y流向电极X。若X为铁,则Y可能是
| A.锌 | B.石墨 | C.银 | D.铜 |
某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是
A正极为Cu,负极为Fe,电解质为FeCl3溶液
B正极为C,负极为Fe,电解质为Fe(NO3)3溶液
C正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液
D正极为Ag,负极为Fe,电解质为Fe2(SO4)3溶液
铜锌原电池的装置如下图所示,下列叙述不正确的是
| A.溶液中的H+定向移动到正极 |
| B.铜片逐渐溶解,质量减轻 |
| C.锌片为负极 |
| D.该装置可以将化学能转化为电能 |
铜锌原电池(如图)工作时,下列叙述正确的是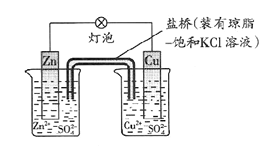
| A.一段时间后铜片增重,盐桥中K+移向CuSO4溶液 |
| B.正极反应为:Zn-2e-=Zn2+ |
| C.电子从铜片经导线流向锌片 |
| D.电池工作时Zn2+和Cu2+ 的浓度保持不变 |
下列关于电化学的理解正确的是
| A.原电池一定是负极材料失电子,发生氧化反应 |
| B.电解池的电极材料一定不参与电极反应 |
| C.原电池的负极和电解池的阳极一定发生氧化反应 |
| D.原电池中的阳离子移向负极,电解池中的阳离子则移向阴极 |
有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是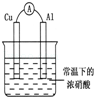
| A.Cu是原电池的负极 |
| B.Al是原电池的负极 |
| C.电子由Al沿导线流向铜 |
| D.铝片上的电极反应式为:Al﹣3e﹣═AL3+ |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。RFC工作原理如图所示,下列有关说法正确的是
A.当有0.1mol电子转移时,a电极产生2.24LH2
B.b极上发生的电极反应是:4H2O+4e- =2H2↑+4OH-
C.c极上进行还原反应,B池中的H+可以通过隔膜进入A 池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
下列关于铁电极的说法中,正确的是
| A.钢铁的吸氧腐蚀中铁是正极 | B.在铁片上镀铜时铁片作阳极 |
| C.电解饱和食盐水时可用铁作阴极 | D.镀锌铁板发生电化学腐蚀时铁是负极 |
右图是研究铁钉腐蚀的装置图,下列说法不正确的是
| A.铁钉在两处的腐蚀速率:a < b |
| B.a、b两处铁钉中碳均正极 |
| C.a、b两处铁钉中的铁均失电子被氧化 |
| D.a、b两处的正极反应式均为O2+4e-+4H+ ===2H2O |
试题篮
()