关于由锌片、铜片和稀硫酸组成的原电池的说法中,正确的是
| A.锌片质量逐渐减少,铜片上有气泡产生 | B.电流方向是由锌片流向铜片 |
| C.锌片作正极,发生还原反应 | D.电解质溶液的pH保持不变 |
某小组为研究电化学原理,设计如下图装置。下列叙述不正确的是
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-===Cu |
| C.a和b用导线连接时,电子由铜电极流向铁电极 |
| D.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 |
下图为番茄电池,下列说法正确的是
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 | D.锌电极是该电池的正极 |
汽车的启动电源常用铅蓄电池,放电时其电池反应如下:PbO2+Pb+2H2SO4="=" 2PbSO4+2H2O。根据此反应判断,下列叙述中正确的是
| A.Pb是正极 | B.PbO2得电子,被氧化 |
| C.负极反应是Pb+SO42——2e—="=" PbSO4 | D.电池放电时,溶液酸性增强 |
R、X、Y、Z四种金属,X、Y组成原电池,X是负极;把Y放在Z的硝酸盐溶液中,Y表面有Z析出,把Z、R投入少量盐酸反应后溶液中只有Z的阳离子。其活泼顺序是
| A.X>Y>Z>R | B.R>Z>Y>X | C.X>Z> R>Y | D.Y>X> R>Z |
下列各变化中属于原电池反应的是( )
| A.在空气中金属铝表面迅速氧化形成保护层 |
| B.镀锌铁表面有划损时,也能阻止铁被氧化 |
| C.红热的铁丝与冷水接触,表面形成蓝黑色保护层 |
| D.浓硝酸比稀硝酸更能氧化金属铜 |
在用锌片、铜片和稀硫酸组成的原电池装置中,经过一段时间后,下列说法正确的是( )
| A.铜片上有气泡产生,发生还原反应 |
| B.锌是负极,发生还原反应 |
| C.电流方向是从锌片沿导线流向铜片 |
| D.铜片逐渐溶解,被氧化 |
关于原电池说法不正确的是:( ) 
| A.如图所示原电池中,Cu为正极 |
| B.如图所示原电池中,开关闭合时,化学能主要转变为电能;断开时,化学能主要转变为热能 |
| C.在原电池中,负极上发生氧化反应,正极上发生还原反应 |
| D.在原电池中,电子从负极经过电解质溶液流向正极 |
用锂制造的电池性能优越,如心脏起搏器中使用的新型Li-I2电池,其使用寿命已超过10年,Li-I2电池在使用时要不断地充电、放电,其中发生的某一化学反应可简化为:2Li+I2=2LiI,下列说法正确的是( )
| A.负极反应是2I--2e-=I2 | B.该电池以LiI水溶液为电解质溶液 |
| C.以惰性非水有机溶剂为电解质 | D.这是电池放电的化学反应 |
下图是用来说明金属的吸氧腐蚀的简易装置,有关此装置的叙述中错误的是( )
| A.铁片为负极,碳棒为正极 |
| B.铁被腐蚀,碳棒上有氯气放出 |
| C.碳棒附近的溶液可使酚酞变红 |
| D.导线上有电流通过,电流方向是由碳极流向铁极 |
某小组为研究电化学原理,设计如下图装置。下列叙述不正确的是( )
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-===Cu |
| C.a和b用导线连接时,电子由铜电极流向铁电极 |
| D.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 |
一学生欲通过实验判断X,Y,Z,W四块金属的活泼性, 做了如下实验并得结论:当X,Y组成原电池时,Y为负极;当Z,W组成原电池时,W为正极;W能将Y从其盐溶液中置换出来,据此可知它们的活泼性顺序是
| A.Z>W> X > Y | B. Z>W> Y>X | C. X>Y>W>Z | D. X>Y>Z>W |
如图是氢氧燃料电池构造示意图。关于该电池的说法不正确的是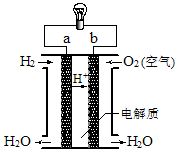
| A.a极是负极 |
| B.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
| C.电子由b通过灯泡流向a |
| D.氢氧燃料电池是环保电池 |
试题篮
()